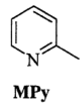
吡啶(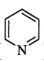 )是类似于苯的芳香化合物,工业上用作合成药品、消毒剂、染料等的原料。2—乙烯基吡啶(VPy)是合成治疗矽肺病药物的原料,可由如图路线合成。
)是类似于苯的芳香化合物,工业上用作合成药品、消毒剂、染料等的原料。2—乙烯基吡啶(VPy)是合成治疗矽肺病药物的原料,可由如图路线合成。
 +
+




请回答下列问题:
(1)毗啶分子呈___ 形,MPy分子中碳原子的杂化方式为___ 。
(2)EPy晶体中微粒间的作用力类型有___ (填标号)。
a.离子键b.金属键c.极性键d.非极性键e.配位键f.氢键
(3)反应①中每生成1molEPy,断裂__ 个π键,形成___ 个σ键。
(4)分子中的大π键可用Π 表示,其中m表示形成大Π键的原子个数,n表示参与形成大Π键的电子个数,则吡啶中大Π键表示为
表示,其中m表示形成大Π键的原子个数,n表示参与形成大Π键的电子个数,则吡啶中大Π键表示为__ 。
(5)吡啶、Cl-与Pt2+形成二氯二吡啶合铂配合物,有顺式和反式两种同分异构体。科学研究表明,顺式分子具有抗癌活性。
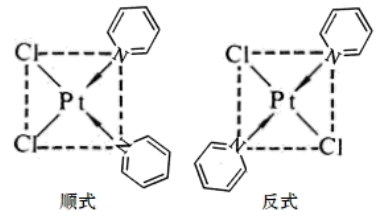
Pt2+的配位数为___ 。顺式二氯二吡啶合铂分子能否溶于水___ (填“能”或“否"),简述理由___ 。
 )是类似于苯的芳香化合物,工业上用作合成药品、消毒剂、染料等的原料。2—乙烯基吡啶(VPy)是合成治疗矽肺病药物的原料,可由如图路线合成。
)是类似于苯的芳香化合物,工业上用作合成药品、消毒剂、染料等的原料。2—乙烯基吡啶(VPy)是合成治疗矽肺病药物的原料,可由如图路线合成。 +
+




请回答下列问题:
(1)毗啶分子呈
(2)EPy晶体中微粒间的作用力类型有
a.离子键b.金属键c.极性键d.非极性键e.配位键f.氢键
(3)反应①中每生成1molEPy,断裂
(4)分子中的大π键可用Π
 表示,其中m表示形成大Π键的原子个数,n表示参与形成大Π键的电子个数,则吡啶中大Π键表示为
表示,其中m表示形成大Π键的原子个数,n表示参与形成大Π键的电子个数,则吡啶中大Π键表示为(5)吡啶、Cl-与Pt2+形成二氯二吡啶合铂配合物,有顺式和反式两种同分异构体。科学研究表明,顺式分子具有抗癌活性。

Pt2+的配位数为
更新时间:2021-05-19 10:53:34
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐1】化合物F是合成组蛋白甲基转移酶抑制剂Tazverik的中间体,其合成路线如图:
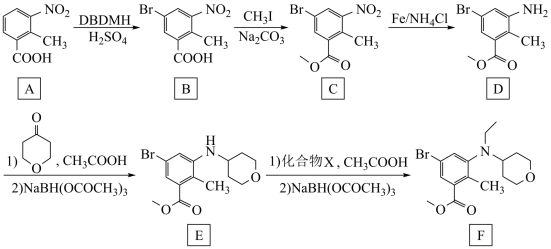
(1)A中碳原子的杂化轨道类型为_______ 。
(2)B→C的反应类型为_______ 。
(3)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式_______ 。
①分子中含有1个手性碳原子;
②在一定条件下完全水解,含苯环产物分子中不同化学环境的氢原子数目比为2:1。
(4)E→F的转化需要化合物X,化合物X的结构简式_______ 。
(5)已知 (R表示烃基)。写出以
(R表示烃基)。写出以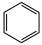 和
和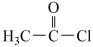 为原料制备
为原料制备 的合成路线流程图
的合成路线流程图________ (无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。

(1)A中碳原子的杂化轨道类型为
(2)B→C的反应类型为
(3)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式
①分子中含有1个手性碳原子;
②在一定条件下完全水解,含苯环产物分子中不同化学环境的氢原子数目比为2:1。
(4)E→F的转化需要化合物X,化合物X的结构简式
(5)已知
 (R表示烃基)。写出以
(R表示烃基)。写出以 和
和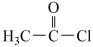 为原料制备
为原料制备 的合成路线流程图
的合成路线流程图
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
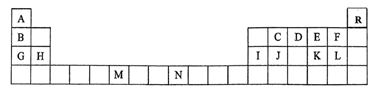
【推荐2】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
(1)请根据对角线规则写出Be与NaOH 溶液反应的化学方程式___________ 。
(2)D的气态氢化物的VSEPR模型为___________ ,其中心原子的杂化类型为___________ 。
(3)G、H和Ⅰ的第一电离能数值由大到小的顺序为:___________ (用元素符号作答)。
(4)C原子在形成化合物时,可采取多种杂化方式。杂化轨道中s轨道成分越多,C元素的电负性越强,连接在该C原子上的H原子越容易电离。下列化合物中,最有可能在碱性体系中形成阴离子的是___________(填编号)。
(5)要证明太阳上是否含有R元素,可采用的方法是___________ 。
(6)与M同周期的所有元素的基态原子中最外层电子数与M原子相同的元素还有___________ (填元素符号)。
(7)C元素是形成有机物的主要元素,下列分子中含有sp和 杂化方式的是
杂化方式的是___________ (填字母)。
(1)请根据对角线规则写出Be与NaOH 溶液反应的化学方程式
(2)D的气态氢化物的VSEPR模型为
(3)G、H和Ⅰ的第一电离能数值由大到小的顺序为:
(4)C原子在形成化合物时,可采取多种杂化方式。杂化轨道中s轨道成分越多,C元素的电负性越强,连接在该C原子上的H原子越容易电离。下列化合物中,最有可能在碱性体系中形成阴离子的是___________(填编号)。
A. | B. | C. | D.苯 |
(6)与M同周期的所有元素的基态原子中最外层电子数与M原子相同的元素还有
(7)C元素是形成有机物的主要元素,下列分子中含有sp和
 杂化方式的是
杂化方式的是a.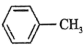 b.
b. c.
c. d.
d.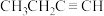
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
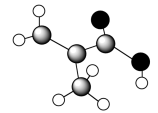
【推荐3】有机物M只含C、H、O三种元素,其分子模型如下图所示(图中球与球之间的连线代表化学键,如单键、双键等)。
(1)有机物M的结构简式为__________________________ ,用1H核磁共振谱可以证明该化合物的核磁共振氢谱中有________ 种吸收峰。
(2)下列物质中,与有机物M互为同分异构体的是___ (填序号),与有机物M互为同系物的是_______ (填序号)。
①CH3CH=CHCOOH ②CH2=CHCOOCH3 ③CH3CH2CH=CHCOOH ④CH3CH(CH3)COOH
(3)M分子中最多有_________ 个碳原子共面,其中碳原子的杂化类型有___________ 。
(4)由M分子聚合可得到只含一种官能团的高分子化合物,写出该反应方程式____________ 。
(1)有机物M的结构简式为
(2)下列物质中,与有机物M互为同分异构体的是
①CH3CH=CHCOOH ②CH2=CHCOOCH3 ③CH3CH2CH=CHCOOH ④CH3CH(CH3)COOH
(3)M分子中最多有
(4)由M分子聚合可得到只含一种官能团的高分子化合物,写出该反应方程式
您最近一年使用:0次
【推荐1】硼族元素(Boron group)指元素周期表中ⅢA 族所有元素,其中硼广泛应用于耐 高温合金工业。回答下列问题:
(1)铊(Tl)是位于第 6 周期的硼族元素,其价电子轨道表示式为___________ ,原子序数为___________ 。
(2)晶体硼单质的基本结构单元为正二十面体,能自发呈现多面体外形,晶体氮化硼结 构类似于金刚石,其熔沸点比晶体硼___________ (填“高”或“低”),解释原因 ___________ 。 第 2 周期元素中,第一电离能介于 N 和 B 之间的元素有___________ (填“元素符号”)。
(3)硼酸晶体是片层结构,其中一层的结构如图所示(图中虚线表示氢键)。
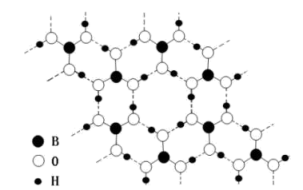
硼酸在冷水中的溶解度很小,在热水中较大,解释原因___________ , 1mol 硼酸晶体中含有氢键的数目为 ___________ 。
(4)硼氢化钠(NaBH4)是一种重要的储氢载体,该化合物中含有的化学键类型有___________ , 键角 H-B-H 为___________ ,其阴离子空间构型为 ___________ 。
(1)铊(Tl)是位于第 6 周期的硼族元素,其价电子轨道表示式为
(2)晶体硼单质的基本结构单元为正二十面体,能自发呈现多面体外形,晶体氮化硼结 构类似于金刚石,其熔沸点比晶体硼
(3)硼酸晶体是片层结构,其中一层的结构如图所示(图中虚线表示氢键)。

硼酸在冷水中的溶解度很小,在热水中较大,解释原因
(4)硼氢化钠(NaBH4)是一种重要的储氢载体,该化合物中含有的化学键类型有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】(1)下列物质中,只含有极性键的分子是___ ,既含离子键又含共价键的化合物是___ ;只存在σ键的分子是___ ,同时存在σ键和π键的分子是____ 。
A.H2 B.CO2 C.CH2Cl2 D.C3H6 E.C2H6 F.CaCl2 G.(NH4)2SO4
(2)根据等电子体原理,羰基硫(OCS)分子的结构式应为____ 。
(3)与CO互为等电子体的分子和离子分别为____ 和____ (各举一种即可,填化学式),CO分子的电子式为___ ,CO分子的结构式可表示成____ 。
(4)COCl2分子的结构式为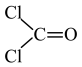 ,COCl2分子内含有
,COCl2分子内含有___ 个σ键、___ 个π键。
A.H2 B.CO2 C.CH2Cl2 D.C3H6 E.C2H6 F.CaCl2 G.(NH4)2SO4
(2)根据等电子体原理,羰基硫(OCS)分子的结构式应为
(3)与CO互为等电子体的分子和离子分别为
(4)COCl2分子的结构式为
 ,COCl2分子内含有
,COCl2分子内含有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】卤族元素单质及其化合物在工业生产中有重要应用。回答下列问题:
(1)卤素位于周期表____ 区,基态F的简化电子排布式为____ 。
(2)拟卤素氰(CN)2和硫氰(SCN)2性质与卤素相似,分子中每个原子最外层都达到8电子结构,已知(SCN)2中含有S-S键,则(SCN)2中σ键和π键的个数比为____ ,(CN)2的熔沸点低于(SCN)2的原因是_____ 。
(3)氯苯 分子中,C采取
分子中,C采取____ 杂化,杂化轨道分别与C、H(或Cl)形成σ键,并且Cl的3px,轨道与C未参与杂化的2px轨道形成大Π键,可表示为____ 。(已知m中心n电子的大Π键可表示为Π )
)
(4)卤化物钙钛矿因其优异的光电性能和高的色纯度被认为是下一代最具前景的光电材料之一。CsPbI3钙钛矿结构中,掺杂金属M2+取代晶胞中一个顶点的Pb2+,则M2+的配位数为____ ,已知晶胞棱长为anm,与M2+距离最近的I-中心构成的立体结构的体积为____ cm3。

(1)卤素位于周期表
(2)拟卤素氰(CN)2和硫氰(SCN)2性质与卤素相似,分子中每个原子最外层都达到8电子结构,已知(SCN)2中含有S-S键,则(SCN)2中σ键和π键的个数比为
(3)氯苯
 分子中,C采取
分子中,C采取 )
)(4)卤化物钙钛矿因其优异的光电性能和高的色纯度被认为是下一代最具前景的光电材料之一。CsPbI3钙钛矿结构中,掺杂金属M2+取代晶胞中一个顶点的Pb2+,则M2+的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】将过量的氨水加到硫酸铜溶液中,溶液最终变成深蓝色。
(1)Cu的价电子轨道表达式为_______ ;在周期表中,Cu元素属于_______ 区。
(2)将氨水逐滴加入硫酸铜溶液中,先生成蓝色沉淀,继续滴加氨水,沉淀溶解,写出沉淀溶解的离子方程式:_______ 。
(3)向深蓝色溶液继续加入_______ ,析出深蓝色的晶体[Cu(NH3)4]SO4·H2O。[Cu(NH3)4]SO4·H2O中,1mol[Cu(NH3)4] 2+含有σ键的数目为_______ 。
(4)_______ (填“H2O”或“NH3”)与Cu2+形成的配位键更稳定。
(5)SO 的VSEPR模型名称为
的VSEPR模型名称为_______ ,H3O+空间构型为_______ 。
(6)硫酸铜溶液中滴入氨基乙酸钠(H2NCH2COONa)即可得到配合物A,其结构如下图所示。

该结构中Cu2+的配位数是_______ 。
(1)Cu的价电子轨道表达式为
(2)将氨水逐滴加入硫酸铜溶液中,先生成蓝色沉淀,继续滴加氨水,沉淀溶解,写出沉淀溶解的离子方程式:
(3)向深蓝色溶液继续加入
(4)
(5)SO
 的VSEPR模型名称为
的VSEPR模型名称为(6)硫酸铜溶液中滴入氨基乙酸钠(H2NCH2COONa)即可得到配合物A,其结构如下图所示。

该结构中Cu2+的配位数是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】电极活性物质Cu4O(PO4)2的制备,可通过下列反应制备:2Na3PO4+4CuSO4+2NH3·H2O = Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O。
(1)上述反应涉及的元素中不属于元素周期表p区元素的是______ ,写出基态Cu2+的电子排布式_______ 。
(2)P、S元素第一电离能大小关系为P_____ S(填“>”、“<”或“=”),原因是___________ 。
(3)O的原子核外有____ 种不同能量的电子,其氢化物沸点高于同族元素H2S的原因是___________ 。
(4)CuSO4溶液中逐滴加入氨水,先产生蓝色沉淀,后又溶解得到深蓝色溶液[Cu(NH3)4]SO4,加入乙醇后有深蓝色沉淀析出,关于该深蓝色物质的说法错误的是______ (填序号),写出沉淀溶解生成深蓝色溶液的离子方程式______ 。
A.该物质正离子的中心是Cu原子 B.该配合物的配体数等于配位数
C.外界离子的中心原子的杂化方式为sp3 D.乙醇的作用是将配合物转化为Cu(OH)2
(5)晶体铜的晶胞结构如图甲所示,原子之间相对位置关系的平面图如图乙所示,铜原子的配位数为_____ ,已知铜原子半径为127.8 pm,NA=6.02×1023 mol-1,计算晶体铜的密度______ g·cm-3(写出表达式)。

(1)上述反应涉及的元素中不属于元素周期表p区元素的是
(2)P、S元素第一电离能大小关系为P
(3)O的原子核外有
(4)CuSO4溶液中逐滴加入氨水,先产生蓝色沉淀,后又溶解得到深蓝色溶液[Cu(NH3)4]SO4,加入乙醇后有深蓝色沉淀析出,关于该深蓝色物质的说法错误的是
A.该物质正离子的中心是Cu原子 B.该配合物的配体数等于配位数
C.外界离子的中心原子的杂化方式为sp3 D.乙醇的作用是将配合物转化为Cu(OH)2
(5)晶体铜的晶胞结构如图甲所示,原子之间相对位置关系的平面图如图乙所示,铜原子的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】I.无机非金属材料中C、Si是构成它们的重要元素。
(1)Si在周期表中的位置为_______ 。
(2)为比较C、Si的非金属性,某同学设计了如下实验,装置①中盛放的试剂是_______ ,装置②中发生反应的离子方程式是_______ 。

(3)SiC是一种重要的高温耐磨材料。SiC中C元素显_______ (填“正”或“负”)化合价,从原子结构角度解释原因是_______ 。
II.金属材料中铜及其合金是人类最早使用的。
(4)基态铜原子的电子排布式为_______ 。
(5)图1是Cu2O的晶胞,Cu原子配位数为_______ 。

(6)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可表示如图2。
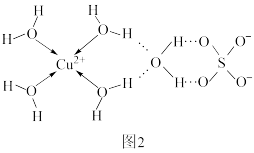
①SO 中S原子的杂化类型为
中S原子的杂化类型为_______ ,写出一个与SO 互为等电子体的分子的化学式
互为等电子体的分子的化学式_______ 。
②胆矾的化学式用配合物的形式可表示为_______ 。1mol胆矾所含σ键的数目为_______ 。
(1)Si在周期表中的位置为
(2)为比较C、Si的非金属性,某同学设计了如下实验,装置①中盛放的试剂是

(3)SiC是一种重要的高温耐磨材料。SiC中C元素显
II.金属材料中铜及其合金是人类最早使用的。
(4)基态铜原子的电子排布式为
(5)图1是Cu2O的晶胞,Cu原子配位数为

(6)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可表示如图2。

①SO
 中S原子的杂化类型为
中S原子的杂化类型为 互为等电子体的分子的化学式
互为等电子体的分子的化学式②胆矾的化学式用配合物的形式可表示为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为_________________________________ 。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)________ I1(Cu)(填“大于”或“小于”)。原因是______________________ 。
(3)ZnF2具有较高的熔点(872 ℃),其化学键类型是________ ;ZnF2不溶于有机溶剂而ZnCl2、ZnBr2、ZnI2能够溶于乙醇、乙醚等有机溶剂,原因是______________________ 。
(4)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为____________________ 。六棱柱底边边长为acm,高为ccm,阿伏加 德罗常数的值为NA,Zn的密度为________ g·cm-3。

(1)Zn原子核外电子排布式为
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)
(3)ZnF2具有较高的熔点(872 ℃),其化学键类型是
(4)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】Fe、Co、Ni是几种重要的金属元素。请回答下列问题:
(1)基态Ni原子的价电子排布式为___________
(2)Ni(CO)4常温下为无色液体,沸点为42.1 ℃,熔点为-19.3 ℃ ,难溶于水,易溶于有机溶剂。推测Ni(CO)4是___________ 分子(填“极性"或“非极性")。
(3)实验室常用KSCN溶液或苯酚检验Fe3+,第一电离能:N___________ O(填“ > ”或“ < ”),苯酚中碳原子杂化类型为___________
(4)配位化合物[Co(NH3)5Cl]C12中心原子Co的配位数为___________ ,配位原子为___________
(5)已知某溶液中,Co2+、Ni2+的浓度分别为0.6mol·L-1和1.2mol·L-1,取一定量的该溶液,向其中滴加NaOH溶液,当Co(OH)2开始沉淀时,溶液中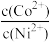 的值等于
的值等于________ (已知Ksp[Co(OH)2]=6.0×10-15,Ksp[Ni(OH)2]=2.0×10-15)
(6)某湿法制备高铁酸钾的基本流程及步骤如下:

①控制反应温度为25 ℃,搅拌1.5h,经氧化等过程溶液变为紫红色,该反应的离子方程式为___________
②在紫红色溶液中加入饱和KOH溶液,析出紫黑色晶体,过滤,得到K2FeO4粗产品。沉淀过程中加入饱和KOH溶液得到晶体的原因是___________ 。
③K2FeO4粗产品含有Fe(OH)3、KCl等杂质,用重结晶方法进行分离提纯,其提纯步骤为________
④若以FeCl3代替Fe(NO3)3作铁源,K2FeO4的产率和纯度都会降低,原因是___________ (写两条)。
(1)基态Ni原子的价电子排布式为
(2)Ni(CO)4常温下为无色液体,沸点为42.1 ℃,熔点为-19.3 ℃ ,难溶于水,易溶于有机溶剂。推测Ni(CO)4是
(3)实验室常用KSCN溶液或苯酚检验Fe3+,第一电离能:N
(4)配位化合物[Co(NH3)5Cl]C12中心原子Co的配位数为
(5)已知某溶液中,Co2+、Ni2+的浓度分别为0.6mol·L-1和1.2mol·L-1,取一定量的该溶液,向其中滴加NaOH溶液,当Co(OH)2开始沉淀时,溶液中
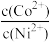 的值等于
的值等于(6)某湿法制备高铁酸钾的基本流程及步骤如下:

①控制反应温度为25 ℃,搅拌1.5h,经氧化等过程溶液变为紫红色,该反应的离子方程式为
②在紫红色溶液中加入饱和KOH溶液,析出紫黑色晶体,过滤,得到K2FeO4粗产品。沉淀过程中加入饱和KOH溶液得到晶体的原因是
③K2FeO4粗产品含有Fe(OH)3、KCl等杂质,用重结晶方法进行分离提纯,其提纯步骤为
④若以FeCl3代替Fe(NO3)3作铁源,K2FeO4的产率和纯度都会降低,原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】(1)二水合草酸镓的结构如图所示,其中镓原子在周期表中的位置为__________ ,草酸根中碳原子的杂化方式为__________ 。
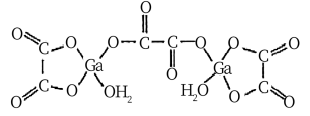
(2)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,其中“亚铁”是关键成分,K3[Fe(CN)6]溶液是检验 Fe2+的试剂,1mol CN-中含π键的数目为______ ,临床建议服用维生素 C 促进“亚铁”的吸收,避免生成 Fe3+,从原子结构角度来看,Fe2+易被氧化成 Fe3+的原因是___________ 。
(3)化合物(CH3)3N 与盐酸反应生成[(CH3) 3NH]+,该过程新生成的化学键为______ (填序号)
a. 离子键 b. 配位键 c. 氢键 d. 非极性共价键
若化合物(CH3)3N 能溶于水,试解析其原因____________________ 。
(4)Cu2+等过渡元素水合离子是否有颜色与原子结构有关,且存在一定的规律。试推断 Ni2+的水合离子为__________ (填“有”或“无”)色离子,依据是_____________ 。
(5)元素铜与镍的第二电离能分别为:ICu=1959kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是_______ 。

(2)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,其中“亚铁”是关键成分,K3[Fe(CN)6]溶液是检验 Fe2+的试剂,1mol CN-中含π键的数目为
(3)化合物(CH3)3N 与盐酸反应生成[(CH3) 3NH]+,该过程新生成的化学键为
a. 离子键 b. 配位键 c. 氢键 d. 非极性共价键
若化合物(CH3)3N 能溶于水,试解析其原因
(4)Cu2+等过渡元素水合离子是否有颜色与原子结构有关,且存在一定的规律。试推断 Ni2+的水合离子为
| 离子 | Sc3+ | Ti3+ | Fe2+ | Cu2+ | Zn2+ |
| 颜色 | 无色 | 紫红色 | 浅绿色 | 蓝色 | 无色 |
(5)元素铜与镍的第二电离能分别为:ICu=1959kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是
您最近一年使用:0次



