下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
(1)请根据对角线规则写出Be与NaOH 溶液反应的化学方程式___________ 。
(2)D的气态氢化物的VSEPR模型为___________ ,其中心原子的杂化类型为___________ 。
(3)G、H和Ⅰ的第一电离能数值由大到小的顺序为:___________ (用元素符号作答)。
(4)C原子在形成化合物时,可采取多种杂化方式。杂化轨道中s轨道成分越多,C元素的电负性越强,连接在该C原子上的H原子越容易电离。下列化合物中,最有可能在碱性体系中形成阴离子的是___________(填编号)。
(5)要证明太阳上是否含有R元素,可采用的方法是___________ 。
(6)与M同周期的所有元素的基态原子中最外层电子数与M原子相同的元素还有___________ (填元素符号)。
(7)C元素是形成有机物的主要元素,下列分子中含有sp和 杂化方式的是
杂化方式的是___________ (填字母)。
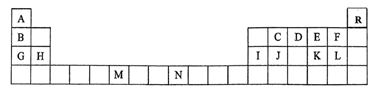
(1)请根据对角线规则写出Be与NaOH 溶液反应的化学方程式
(2)D的气态氢化物的VSEPR模型为
(3)G、H和Ⅰ的第一电离能数值由大到小的顺序为:
(4)C原子在形成化合物时,可采取多种杂化方式。杂化轨道中s轨道成分越多,C元素的电负性越强,连接在该C原子上的H原子越容易电离。下列化合物中,最有可能在碱性体系中形成阴离子的是___________(填编号)。
A. | B. | C. | D.苯 |
(6)与M同周期的所有元素的基态原子中最外层电子数与M原子相同的元素还有
(7)C元素是形成有机物的主要元素,下列分子中含有sp和
 杂化方式的是
杂化方式的是a.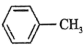 b.
b. c.
c. d.
d.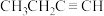
更新时间:2024-04-12 22:29:32
|
相似题推荐
【推荐1】AA705合金(含Al、Zn、Mg和Cu)几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。但这种合金很难被焊接。最近科学家将碳化钛纳米颗粒(大小仅为十亿分之一米)注入AA7075的焊丝内,让这些纳米颗粒充当连接件之间的填充材料。注入了纳米粒子的填充焊丝也可以更容易地连接其他难以焊接的金属和金属合金。回答下列问题:
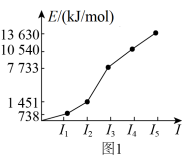
(1)第三周期某元素的前5个电子的电离能如图1所示。该元素是__________ (填元素符号),判断依据是__________ 。
(2)CN-、NH3、H2O和OH—等配体都能与Zn2+形成配离子。1mol[Zn(NH3)4]2+含__________ molσ键,中心离子的配位数为__________ 。
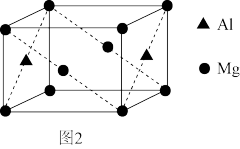
(3)铝镁合金是优质储钠材料,原子位于面心和顶点,其晶胞如图2所示。1个铝原子周围有__________ 个镁原子最近且等距离。
(4)在二氧化钛和光照条件下,苯甲醇可被氧化成苯甲醛:
①苯甲醇中C原子杂化类型是__________ 。
②苯甲醇的沸点高于苯甲醛,其原因是__________ 。
(5)钛晶体有两种晶胞,如图所示。
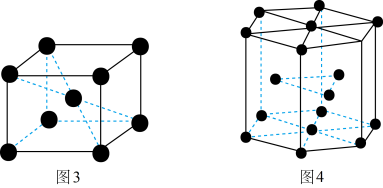
①如图3所示,晶胞的空间利用率为________ (用含π的式子表示)。
②已知图4中六棱柱边长为xcm,高为ycm。该钛晶胞密度为Dg·cm-3,NA为__________ mol-1(用含xy和D的式子表示)。
(1)第三周期某元素的前5个电子的电离能如图1所示。该元素是


(2)CN-、NH3、H2O和OH—等配体都能与Zn2+形成配离子。1mol[Zn(NH3)4]2+含
(3)铝镁合金是优质储钠材料,原子位于面心和顶点,其晶胞如图2所示。1个铝原子周围有
(4)在二氧化钛和光照条件下,苯甲醇可被氧化成苯甲醛:

①苯甲醇中C原子杂化类型是
②苯甲醇的沸点高于苯甲醛,其原因是
(5)钛晶体有两种晶胞,如图所示。

①如图3所示,晶胞的空间利用率为
②已知图4中六棱柱边长为xcm,高为ycm。该钛晶胞密度为Dg·cm-3,NA为
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐2】以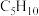 为起始物,通过一系列反应实现某些官能团的相互转化。回答下列问题:
为起始物,通过一系列反应实现某些官能团的相互转化。回答下列问题:
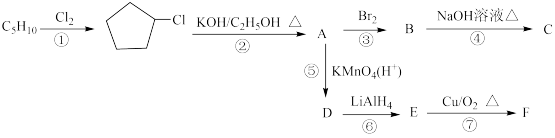
(1)反应①的反应条件是_______ 。
(2)A中碳原子的杂化类型是_______ 。
(3)步骤②⑤⑥⑦中属于氧化反应的是_______ 。
(4)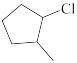 与
与 互为同系物,用*标出
互为同系物,用*标出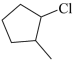 中的手性碳原子
中的手性碳原子______ (标1个即可)。
(5)步骤④反应的方程式为_______ 。
(6)F的核磁共振氢谱峰面积比为_______ 。
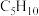 为起始物,通过一系列反应实现某些官能团的相互转化。回答下列问题:
为起始物,通过一系列反应实现某些官能团的相互转化。回答下列问题:
(1)反应①的反应条件是
(2)A中碳原子的杂化类型是
(3)步骤②⑤⑥⑦中属于氧化反应的是
(4)
 与
与 互为同系物,用*标出
互为同系物,用*标出 中的手性碳原子
中的手性碳原子(5)步骤④反应的方程式为
(6)F的核磁共振氢谱峰面积比为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】(1)C 元素是形成有机物的主要元素,下列分子中含有 sp 和 sp3 杂化方式的是 ___________ (填字母)。
a.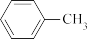 b.CH4 c.CH2=CHCH3 d.CH3CH2C≡CH
b.CH4 c.CH2=CHCH3 d.CH3CH2C≡CH
(2)BF3 能与 NH3 反应生成 BF3·NH3.BF3·NH3中 B 原子的杂化轨道类型为___________ ,B 与 N 之间形成___________ 键。硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质。[B(OH)4]-中 B 的原子杂化类型为 ___________ ,不考虑空间构型,[B(OH)4]-的结构可用示意图表示为___________ 。
(3)麻醉剂的发现和使用是人类医学史上一项了不起的成就。“笑气”(N2O)是人类最早应用于医疗的麻醉剂之一、已知 N2O 分子中氧原子只与一个氮原子相连,则 N2O 的结构式可表示为___________ ,其分子立体构型是 ___________ 形。另一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气(COCl2):2CHCl3+O2→2HCl+2COCl2,光气分子的立体构型是___________ 形。
(4)丁二酮肟常用于检验 Ni2+:在稀氨水介质中,丁二酮肟与 Ni2+反应可生成鲜红色沉淀,其结构如图所示。
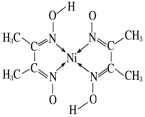
该结构中,碳碳之间的共价键类型是 σ 键,碳氮之间的共价键类型是___________ ,氮镍之间形成的化学键是___________ 。碳原子的杂化轨道类型有 ___________ 。
a.
 b.CH4 c.CH2=CHCH3 d.CH3CH2C≡CH
b.CH4 c.CH2=CHCH3 d.CH3CH2C≡CH(2)BF3 能与 NH3 反应生成 BF3·NH3.BF3·NH3中 B 原子的杂化轨道类型为
(3)麻醉剂的发现和使用是人类医学史上一项了不起的成就。“笑气”(N2O)是人类最早应用于医疗的麻醉剂之一、已知 N2O 分子中氧原子只与一个氮原子相连,则 N2O 的结构式可表示为
(4)丁二酮肟常用于检验 Ni2+:在稀氨水介质中,丁二酮肟与 Ni2+反应可生成鲜红色沉淀,其结构如图所示。

该结构中,碳碳之间的共价键类型是 σ 键,碳氮之间的共价键类型是
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐1】芳香化合物A是一种基本化工原料,可以从煤和石油中得到。A、B、C、D、E的转化关系如图所示。回答下列问题:
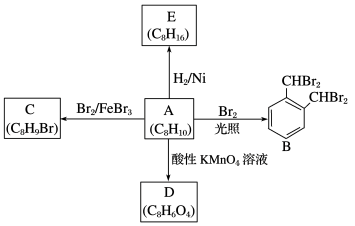
(1)A的化学名称是_________ 。
(2)A→B的反应类型是_________ 。A→E的反应类型是_________ 。
(3)A的一种同分异构体发生在苯环上的一元取代物只有一种其结构简式为:_________ 。
(4)A→C的化学方程式为______ 。(任写一种)
(5)D的官能团名称为:_________ 。

(1)A的化学名称是
(2)A→B的反应类型是
(3)A的一种同分异构体发生在苯环上的一元取代物只有一种其结构简式为:
(4)A→C的化学方程式为
(5)D的官能团名称为:
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】元素周期表是学习化学的重要工具。下表为8种元素在周期表中的位置。

(1)如图所示的模型表示的分子中,可由A、D形成的是____ 。

c与氯气反应生成的二元取代物有____ 种,d分子的结构简式____ 。
(2)Na在F单质中燃烧产物的电子式为____ 。该燃烧产物中化学键的类型为:____ 。上述元素的最高价氧化物的水化物中,碱性最强的是____ (写化学式)。
(3)A与D组成的化合物中,质量相同,在氧气中完全燃烧消耗氧气最多的是:____
(4)关于(1)中d分子有下列问题:
①d分子中同一平面的原子最多有____ 个。
②若用-C4H9取代d上的一个H原子,得到的有机物的同分异构体共有____ 种。

(1)如图所示的模型表示的分子中,可由A、D形成的是

c与氯气反应生成的二元取代物有
(2)Na在F单质中燃烧产物的电子式为
(3)A与D组成的化合物中,质量相同,在氧气中完全燃烧消耗氧气最多的是:
(4)关于(1)中d分子有下列问题:
①d分子中同一平面的原子最多有
②若用-C4H9取代d上的一个H原子,得到的有机物的同分异构体共有
您最近半年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐3】下表是A、B、C、D、E五种有机物的有关信息:
回答下列问题:
(1)A与溴的四氯化碳溶液反应所得产物的名称是__________ 。
(2)B具有的性质是__________ (填序号)。
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大
⑤与酸性KMnO4溶液和溴水反应而使其褪色 ⑥任何条件下都不与氢气反应
(3)C与E反应能生成相对分子质量为100的酯,所发生的反应的反应类型为_______________ ,对应的化学方程式为_______________ 。
(4)写出C氧化生成D的化学反应方程式:_______________ 。
| A | ①能使溴的四氯化碳溶液褪色;②比例模型为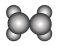 |
| B | ①由C、H两种元素组成;②球棍模型为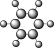 |
| C | ①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与E反应生成相对分子质量为100的酯 |
| D | ①相对分子质量比C少2;②能由C氧化而成 |
| E | ①由C、H、O三种元素组成;②球棍模型为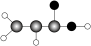 |
回答下列问题:
(1)A与溴的四氯化碳溶液反应所得产物的名称是
(2)B具有的性质是
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大
⑤与酸性KMnO4溶液和溴水反应而使其褪色 ⑥任何条件下都不与氢气反应
(3)C与E反应能生成相对分子质量为100的酯,所发生的反应的反应类型为
(4)写出C氧化生成D的化学反应方程式:
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】磷酸亚铁锂(LiFePO4)和锰酸锂(LiMn2O4)均可用作锂离子电池正极材料。回答下列问题:
(1)在周期表中,与Li化学性质最相似的邻族元素是___________ ,基态P原子电子占据最高能级的电子云轮廓图为___________ 形。
(2)原子核外电子有两种相反的自旋状态,分别用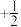 和
和 表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为___________ 。
(3) 的空间结构为
的空间结构为___________ 形,其中心原子的杂化轨道类型为___________ 。
(4)已知; ,
,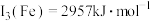 。Mn的第三电离能大于Fe的第三电离能,其主要原因是
。Mn的第三电离能大于Fe的第三电离能,其主要原因是___________ 。
(1)在周期表中,与Li化学性质最相似的邻族元素是
(2)原子核外电子有两种相反的自旋状态,分别用
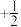 和
和 表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为(3)
 的空间结构为
的空间结构为(4)已知;
 ,
,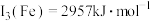 。Mn的第三电离能大于Fe的第三电离能,其主要原因是
。Mn的第三电离能大于Fe的第三电离能,其主要原因是
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】铁被誉为“第一金属”,铁及其化合物在生活中有广泛应用。
(1)基态Fe2+的简化电子排布式为___________ 。
(2)实验室可用KSCN、苯酚(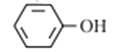 )来检验Fe3+ 。N、O、S三种元素的第一电离能由大到小的顺序为
)来检验Fe3+ 。N、O、S三种元素的第一电离能由大到小的顺序为 ___________ (用元素符号表示),苯酚中碳原子的杂化轨道类型为___________ 。
(3)FeCl3的熔点为306 ℃,沸点为315 ℃。FeCl3的晶体类型是___________ 。FeSO4常作净水剂和补铁剂,SO 的立体构型是
的立体构型是___________ 。
(4)羰基铁[Fe(CO)5]可用作催化剂、汽油抗爆剂等。1 mol Fe(CO)5分子中含___________ molσ键,与CO互为等电子体的离子是 ___________ (填化学式,写一种)。
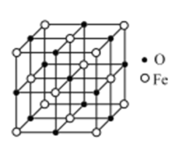
(5)氧化亚铁晶体的晶胞如图所示。已知:氧化亚铁晶体的密度为ρg/cm3 ,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为___________ ;Fe2+与O2-最短核间为 ___________ pm(列出表达式即可)。
(1)基态Fe2+的简化电子排布式为
(2)实验室可用KSCN、苯酚(
 )来检验Fe3+ 。N、O、S三种元素的第一电离能由大到小的顺序为
)来检验Fe3+ 。N、O、S三种元素的第一电离能由大到小的顺序为 (3)FeCl3的熔点为306 ℃,沸点为315 ℃。FeCl3的晶体类型是
 的立体构型是
的立体构型是(4)羰基铁[Fe(CO)5]可用作催化剂、汽油抗爆剂等。1 mol Fe(CO)5分子中含
(5)氧化亚铁晶体的晶胞如图所示。已知:氧化亚铁晶体的密度为ρg/cm3 ,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力。
(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,写出基态镍原子的价电子排布式为_______ ,它位于周期表_______ 区。
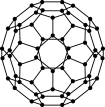
(2)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途。富勒烯(C60)的结构如图,分子中碳原子轨道的杂化类型为_______ ;1 mol C60分子中σ键的数目为_______ 个。
(3)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓(GaAs)、硫化镉(CdS)薄膜电池等。
①第一电离能:As_______ Ga(填“>”“<”或“=”)。
②SeO2分子的空间结构为_______ 。
(4)三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在太阳能电池制造中得到广泛应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应中NH3的沸点_______ (填“>”“<”或“=”)PH3的沸点,NH4F固体属于_______ 晶体(填写晶体类型),写出NH3与F2反应的方程式_______ 。
(1)太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层,写出基态镍原子的价电子排布式为
(2)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途。富勒烯(C60)的结构如图,分子中碳原子轨道的杂化类型为

(3)多元化合物薄膜太阳能电池材料为无机盐,其主要包括砷化镓(GaAs)、硫化镉(CdS)薄膜电池等。
①第一电离能:As
②SeO2分子的空间结构为
(4)三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在太阳能电池制造中得到广泛应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应中NH3的沸点
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】据 科技日报
科技日报 报道,我国科学家研制成功一系列石墨烯限域的3d过渡金属中心(Mn、Fe、Co、Ni、Cu)催化剂,在室温条件下以H2O2为氧化剂直接将CH4氧化成含氧化合物。
报道,我国科学家研制成功一系列石墨烯限域的3d过渡金属中心(Mn、Fe、Co、Ni、Cu)催化剂,在室温条件下以H2O2为氧化剂直接将CH4氧化成含氧化合物。
请回答下列问题:
⑴在Mn、Fe、Co、Ni、Cu中,某基态原子核外电子排布遵循“洪特规则特例”,该原子的外围电子排布式为____________ 。
⑵在第四周期过渡金属中,基态原子第一电离能最大的元素是___________ (填元素符号)。
⑶铜的焰色反应呈绿色,在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为________________ 。
⑷常温下,H2O2氧化CH4生成CH3OH、HCHO、 HCOOH等。
①CH3OH、HCHO、 HCOOH的沸点分别为64.7℃、-195℃、100.8℃,其主要原因是____________________ ;
②CH4和HCHO比较,键角较大的是_________ ,该分子的空间构型为____________ 。
⑸配离子中受配体的影响,中心离子同能级d轨道的能量不同,人们把1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量称为d的分裂能,用符号 表示。分裂能大小一般与配体种类和中心离子所带电荷数有关。据此判断分裂能Δ[Co(H2O)6]2+
表示。分裂能大小一般与配体种类和中心离子所带电荷数有关。据此判断分裂能Δ[Co(H2O)6]2+________ Δ[Co(H2O)6]3+(填“>”“<”或“=” ,理由是
,理由是____________ 。
⑹钴晶胞和白铜(铜镍合金)晶胞如图所示。

①钴晶胞堆积方式的名称为____________ ;
②已知白铜晶胞的密度为dg∙cm-3,NA代表阿伏加 德罗常数的值。图2晶胞中两个面心上铜原子最短核间距为____________ pm(列出计算式)。
 科技日报
科技日报 报道,我国科学家研制成功一系列石墨烯限域的3d过渡金属中心(Mn、Fe、Co、Ni、Cu)催化剂,在室温条件下以H2O2为氧化剂直接将CH4氧化成含氧化合物。
报道,我国科学家研制成功一系列石墨烯限域的3d过渡金属中心(Mn、Fe、Co、Ni、Cu)催化剂,在室温条件下以H2O2为氧化剂直接将CH4氧化成含氧化合物。请回答下列问题:
⑴在Mn、Fe、Co、Ni、Cu中,某基态原子核外电子排布遵循“洪特规则特例”,该原子的外围电子排布式为
⑵在第四周期过渡金属中,基态原子第一电离能最大的元素是
⑶铜的焰色反应呈绿色,在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为
⑷常温下,H2O2氧化CH4生成CH3OH、HCHO、 HCOOH等。
①CH3OH、HCHO、 HCOOH的沸点分别为64.7℃、-195℃、100.8℃,其主要原因是
②CH4和HCHO比较,键角较大的是
⑸配离子中受配体的影响,中心离子同能级d轨道的能量不同,人们把1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量称为d的分裂能,用符号
 表示。分裂能大小一般与配体种类和中心离子所带电荷数有关。据此判断分裂能Δ[Co(H2O)6]2+
表示。分裂能大小一般与配体种类和中心离子所带电荷数有关。据此判断分裂能Δ[Co(H2O)6]2+ ,理由是
,理由是⑹钴晶胞和白铜(铜镍合金)晶胞如图所示。

①钴晶胞堆积方式的名称为
②已知白铜晶胞的密度为dg∙cm-3,NA代表阿伏加 德罗常数的值。图2晶胞中两个面心上铜原子最短核间距为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】Al及其化合物在生产生活中有广泛应用。
回答下列问题:
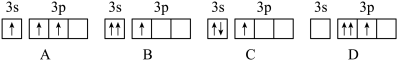
(1)运-20的外壳使用了铝合金:Mg-Al-Mn,下列选项中能表示基态Al原子价层电子排布图的是______ 。(填选项字母);第一电离能:铝______ (填“大于”“等于”或“小于”)镁。
(2)三乙基铝是一种金属有机物,可做火箭燃料,其结构简式为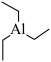 。
。
①三乙基铝熔点为-52.5℃,其晶体类型为______ 。
②三乙基铝中Al的VSEPR模型为______ ,C原子的杂化方式为______ 。
③三乙基铝中所含元素的电负性从大到小的顺序为______ (用元素符号表示)。
(3)工业上冶炼铝时需加入助熔剂冰晶石(Na3AlF6),[AlF6]3-中的中心原子的配位数为______ 。
(4)AlP晶胞结构与Si的类似,如图所示:
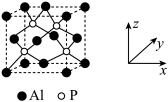
①磷化铝晶胞沿着x轴的投影图为______ (填选项字母)。
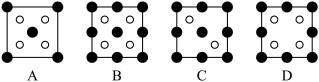
②若磷化铝的晶胞边长为a pm,NA表示阿伏加德罗常数的值,则AlP晶体密度为______ g/cm3(用含NA、a的最简代数式表示)。
回答下列问题:
(1)运-20的外壳使用了铝合金:Mg-Al-Mn,下列选项中能表示基态Al原子价层电子排布图的是

(2)三乙基铝是一种金属有机物,可做火箭燃料,其结构简式为
 。
。①三乙基铝熔点为-52.5℃,其晶体类型为
②三乙基铝中Al的VSEPR模型为
③三乙基铝中所含元素的电负性从大到小的顺序为
(3)工业上冶炼铝时需加入助熔剂冰晶石(Na3AlF6),[AlF6]3-中的中心原子的配位数为
(4)AlP晶胞结构与Si的类似,如图所示:

①磷化铝晶胞沿着x轴的投影图为

②若磷化铝的晶胞边长为a pm,NA表示阿伏加德罗常数的值,则AlP晶体密度为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】周期表是学习物质结构和性质的重要工具,下图是元素周期表的一部分,A、B、D、E、F、G、W、Q各代表一种化学元素。请用元素符号及其物质回答下列问题.
(1)W位于周期表_______ 区;基态Q原子核外简化电子排布式为_______ ;
(2)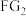 中心原子杂化轨道类型:
中心原子杂化轨道类型:_______ ;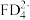 的
的 模型名称:
模型名称:_______ ;
(3)E、F、G三元素第一电离能从大到小的顺序是_______ ;
(4)化合物AD与 溶液反应的离子方程式为
溶液反应的离子方程式为_______ ;
(5)有机物甲由B、氢、D三种元素的原子按个数比为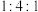 组成,可通过电解法由
组成,可通过电解法由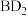 制取,用稀硫酸作电解质溶液,写出生成有机物甲的电极反应式:
制取,用稀硫酸作电解质溶液,写出生成有机物甲的电极反应式:_______ ,有机物甲也可作为燃料电池的原料,写出该燃料电池在碱性条件下的负极反应式:_______ 。
| A | B | D | |||||||||||||||
| E | F | G | |||||||||||||||
| W | Q |
(2)
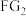 中心原子杂化轨道类型:
中心原子杂化轨道类型: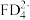 的
的 模型名称:
模型名称:(3)E、F、G三元素第一电离能从大到小的顺序是
(4)化合物AD与
 溶液反应的离子方程式为
溶液反应的离子方程式为(5)有机物甲由B、氢、D三种元素的原子按个数比为
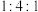 组成,可通过电解法由
组成,可通过电解法由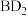 制取,用稀硫酸作电解质溶液,写出生成有机物甲的电极反应式:
制取,用稀硫酸作电解质溶液,写出生成有机物甲的电极反应式:
您最近半年使用:0次



