分别填空(1)已知下列热化学方程式:
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH1=-25 kJ·mol-1
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH2=-47 kJ·mol-1
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH3=+19 kJ·mol-1
写出FeO(s)被CO还原成Fe和CO2的热化学方程式___________
(2)书写下列物质的电子式:NH4Cl___________ HClO___________ Ca(OH)2 ___________ Na2O2 ___________
(3)将Mg、Cu组成的2.64g混合物投入适量稀硝酸中恰好完全反应,并收集还原产物NO气体(还原产物只有一种)。然后向反应后的溶液中加入一定量NaOH溶液,金属离子恰好沉淀完全,沉淀质量为4.68g,则反应过程中收集到NO气体(标况下)体积为___________
(4)在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出 650kJ的热量,反应的热化学方程式为___________
(5)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为___________
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH1=-25 kJ·mol-1
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH2=-47 kJ·mol-1
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH3=+19 kJ·mol-1
写出FeO(s)被CO还原成Fe和CO2的热化学方程式
(2)书写下列物质的电子式:NH4Cl
(3)将Mg、Cu组成的2.64g混合物投入适量稀硝酸中恰好完全反应,并收集还原产物NO气体(还原产物只有一种)。然后向反应后的溶液中加入一定量NaOH溶液,金属离子恰好沉淀完全,沉淀质量为4.68g,则反应过程中收集到NO气体(标况下)体积为
(4)在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出 650kJ的热量,反应的热化学方程式为
(5)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为
更新时间:2021-06-08 21:52:10
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】面对新冠肺炎病毒可以采用的消毒剂常见的有“84”消毒液,医用酒精它们的有效成分分别是NaClO、 ,都可以使病毒中的蛋白质变性,从而杀死病毒。请回答以下问题:
,都可以使病毒中的蛋白质变性,从而杀死病毒。请回答以下问题:
(1)以上涉及元素包含
(2) 是
是 分子中的氢原子的类型有
分子中的氢原子的类型有
(3)NaClO的电子式
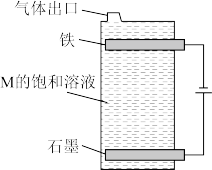
(4)①M的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期元素在周期表中的位置如图所示。请按要求回答下列问题。
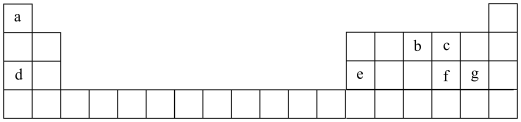
(1)由a、c、d形成的化合物的电子式为___________ ,该物质属于___________ 化合物(填“离子”或“共价”)。可能含有的化学键类型有___________ 。
(2)a与b形成的二元化合物中,所含电子数为10的分子的电子式为___________ ,a与c形成的二元化合物中,所含电子数为18的物质的结构式为___________ 。
(3)在全国抗击“新冠肺炎”的“战疫”中用了大量的“84”来消毒杀菌,84消毒液和洁厕灵混合使用时产生了一种有毒气体,写出两者混合时的化学反应方程式:___________ 。
(4)写出d与e两种元素的最高价氧化物对应的水化物相互反应的离子方程式:___________ 。

(1)由a、c、d形成的化合物的电子式为
(2)a与b形成的二元化合物中,所含电子数为10的分子的电子式为
(3)在全国抗击“新冠肺炎”的“战疫”中用了大量的“84”来消毒杀菌,84消毒液和洁厕灵混合使用时产生了一种有毒气体,写出两者混合时的化学反应方程式:
(4)写出d与e两种元素的最高价氧化物对应的水化物相互反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求回答下列问题:
(1)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是__ 。
(2)下列关于化学键的说法正确的是____ 。
① 含有金属元素的化合物一定是离子化合物
② 第IA族和第ⅦA族元素原子化合时,一定生成离子键
③ 由非金属元素形成的化合物一定不是离子化合物
④ 活泼金属与非金属化合时,能形成离子键
⑤ 离子键就是阴、阳离子间的相互引力
⑥离子化合物中可能含有非极性共价键
(3)写出下列物质的电子式:Mg(OH)2:____ , N2:_______ ,NH4I:_______ 。
(4)用电子式表示下列化合物的形成过程:Na2S:_______ ;H2O:_______ 。
(1)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是
(2)下列关于化学键的说法正确的是
① 含有金属元素的化合物一定是离子化合物
② 第IA族和第ⅦA族元素原子化合时,一定生成离子键
③ 由非金属元素形成的化合物一定不是离子化合物
④ 活泼金属与非金属化合时,能形成离子键
⑤ 离子键就是阴、阳离子间的相互引力
⑥离子化合物中可能含有非极性共价键
(3)写出下列物质的电子式:Mg(OH)2:
(4)用电子式表示下列化合物的形成过程:Na2S:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有14.4gCO和CO2的混合气体,在标准状况下其体积为8.96L。
(1)求CO和CO2的物质的量分别是_____________ 。
(2)求混合气体中碳原子的个数_____________ (用NA表示阿伏加德罗常数的值)。
(1)求CO和CO2的物质的量分别是
(2)求混合气体中碳原子的个数
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知:5SO2+2MnO +2H2O=5SO
+2H2O=5SO +2Mn2++4H+ 。现将3.16mgKMnO4固体溶于水配成20mL溶液,吸收空气管道中的SO2,若管道中空气流量为40L/min,经过5min溶液恰好褪色。请计算:
+2Mn2++4H+ 。现将3.16mgKMnO4固体溶于水配成20mL溶液,吸收空气管道中的SO2,若管道中空气流量为40L/min,经过5min溶液恰好褪色。请计算:
(1)所用KMnO4溶液的物质的量浓度_______ mol/L。
(2)空气样品中SO2的含量_______ mg/L。
(3)若空气中SO2的浓度不超过0.02mg/L为合格,则上述空气质量_______ (填“合格”或“不合格”)。
 +2H2O=5SO
+2H2O=5SO +2Mn2++4H+ 。现将3.16mgKMnO4固体溶于水配成20mL溶液,吸收空气管道中的SO2,若管道中空气流量为40L/min,经过5min溶液恰好褪色。请计算:
+2Mn2++4H+ 。现将3.16mgKMnO4固体溶于水配成20mL溶液,吸收空气管道中的SO2,若管道中空气流量为40L/min,经过5min溶液恰好褪色。请计算:(1)所用KMnO4溶液的物质的量浓度
(2)空气样品中SO2的含量
(3)若空气中SO2的浓度不超过0.02mg/L为合格,则上述空气质量
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】化学小组同学通过实验探究某补铁药品中含亚铁盐,实验过程如下:
(1)甲同学取少量溶液,先加入2滴 溶液,溶液无明显变化;再加入几滴新制氯水,溶液变红。氯水与亚铁盐反应的离子方程式为
溶液,溶液无明显变化;再加入几滴新制氯水,溶液变红。氯水与亚铁盐反应的离子方程式为__________ 。
(2)乙同学也取少量溶液,滴加 溶液,有沉淀生成;将其露置于空气中可观察到的现象是
溶液,有沉淀生成;将其露置于空气中可观察到的现象是__________ ;产生该现象原因是__________ (用化学方程式解释)。
(3)丙同学取少量甲同学实验后的溶液,加入过量铁粉,溶液红色又消失。此实验能证明的是__________ 。
(1)甲同学取少量溶液,先加入2滴
 溶液,溶液无明显变化;再加入几滴新制氯水,溶液变红。氯水与亚铁盐反应的离子方程式为
溶液,溶液无明显变化;再加入几滴新制氯水,溶液变红。氯水与亚铁盐反应的离子方程式为(2)乙同学也取少量溶液,滴加
 溶液,有沉淀生成;将其露置于空气中可观察到的现象是
溶液,有沉淀生成;将其露置于空气中可观察到的现象是(3)丙同学取少量甲同学实验后的溶液,加入过量铁粉,溶液红色又消失。此实验能证明的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求写出下列化学用语
(1)自来水中氯离子检验的离子方程式______
(2)盐酸除铁锈的离子方程式______
(3)二氧化碳通入澄清石灰水的离子方程式______ .
(1)自来水中氯离子检验的离子方程式
(2)盐酸除铁锈的离子方程式
(3)二氧化碳通入澄清石灰水的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】有以下10种物质,请回答下列问题:
①干冰;②氯化钠固体;③氯气;④稀硫酸;⑤NaHSO4溶液;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧液态纯醋酸;⑨氯化氢;⑩NH3
(1)其中能导电的是_______ (填写符号,下同);属于电解质的是_______ ;属于非电解质的是_______ 。
(2)分别写出物质⑤和⑥在水中的电离方程式:_______ 、_______ ;
(3)写出物质④和⑥在水中发生反应的离子方程式:_______ ;
(4)写出物质④和⑦反应的离子方程式:_______ ;
(5)写出少量物质①和过量的物质⑦发生反应的离子方程式:_______ 。
①干冰;②氯化钠固体;③氯气;④稀硫酸;⑤NaHSO4溶液;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧液态纯醋酸;⑨氯化氢;⑩NH3
(1)其中能导电的是
(2)分别写出物质⑤和⑥在水中的电离方程式:
(3)写出物质④和⑥在水中发生反应的离子方程式:
(4)写出物质④和⑦反应的离子方程式:
(5)写出少量物质①和过量的物质⑦发生反应的离子方程式:
您最近一年使用:0次
【推荐1】甲醇(CH3OH)是一种重要的化工原料。已知
CH3OH(1) + O2(g) = CO(g) + 2H2O(g) ; △H = -443.64 kJ·mol-1
2CO (g) + O2(g) = 2CO2(g) ; △H = -566.00 kJ·mol-1
H2O(1) = H2O (g) ; △H = +44.00 kJ·mol-1
(1)试写出能表示CH3OH(l)燃烧热的热化学方程式:_______ 。
(2)800℃时A、B、C三种气体在恒容密闭容器中反应时的浓度变化如图所示,分析图像,回答下列问题:
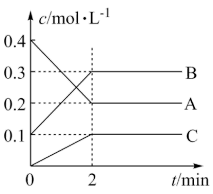
①该反应的方程式为_______ 。
②2min内,用B表示的反应速率为_______ 。
③下列能说明该反应达到平衡状态的是_______ 。
A.体系压强保持不变 B.容器中气体密度保持不变 C.混合气体平均摩尔质量保持不变 D.每消耗2mol A的同时生成1mol C E.A、B、C浓度之比为2:2:1 F.混合气体中A的质量分数保持不变
④为加快该反应的反应速率,可采取的措施是_______ 。
A.恒容通入He B.分离出B C.选择高效的催化剂 D.适当升高体系温度
CH3OH(1) + O2(g) = CO(g) + 2H2O(g) ; △H = -443.64 kJ·mol-1
2CO (g) + O2(g) = 2CO2(g) ; △H = -566.00 kJ·mol-1
H2O(1) = H2O (g) ; △H = +44.00 kJ·mol-1
(1)试写出能表示CH3OH(l)燃烧热的热化学方程式:
(2)800℃时A、B、C三种气体在恒容密闭容器中反应时的浓度变化如图所示,分析图像,回答下列问题:

①该反应的方程式为
②2min内,用B表示的反应速率为
③下列能说明该反应达到平衡状态的是
A.体系压强保持不变 B.容器中气体密度保持不变 C.混合气体平均摩尔质量保持不变 D.每消耗2mol A的同时生成1mol C E.A、B、C浓度之比为2:2:1 F.混合气体中A的质量分数保持不变
④为加快该反应的反应速率,可采取的措施是
A.恒容通入He B.分离出B C.选择高效的催化剂 D.适当升高体系温度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知:
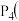 白磷,
白磷,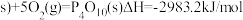
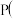 红磷,
红磷,
试写出白磷转化为红磷的热化学方程式_____ ;白磷的稳定性比红磷_____ (填“高”或“低”)
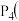 白磷,
白磷,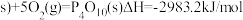
 红磷,
红磷,
试写出白磷转化为红磷的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
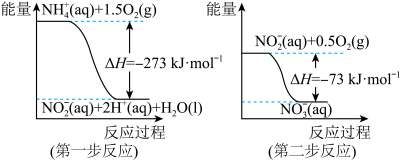
①第一步反应是___________ (填“放热”或“吸热”)反应,判断依据是_______ 。
②1mol NH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是_________________________ 。
(2) 已知红磷比白磷稳定,则反应:
P4(白磷,s)+5O2(g)=2P2O5(s) ΔH1;
4P(红磷,s)+5O2(g)=2P2O5(s) ΔH2;
ΔH1和ΔH2的关系是ΔH1_____ ΔH2(填“>”“<”或“=”)。
(3) 已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ•mol-1①
Na2O2(s)+CO2(g)=Na2CO3(s)+ O2(g) ΔH=-226 kJ•mol-1 ②
O2(g) ΔH=-226 kJ•mol-1 ②
则CO(g)与Na2O2(s)反应放出509kJ热量时,电子转移数目为__________________ 。
(4)已知H2(g)+Br2(l)=2HBr(g) ΔH=-72kJ•mol-1,蒸发1mol Br2(l)需要吸收的能量为30kJ,其他相关数据如下表:
则表中a=__________________ 。
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
①第一步反应是
②1mol NH
 (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是(2) 已知红磷比白磷稳定,则反应:
P4(白磷,s)+5O2(g)=2P2O5(s) ΔH1;
4P(红磷,s)+5O2(g)=2P2O5(s) ΔH2;
ΔH1和ΔH2的关系是ΔH1
(3) 已知:2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ•mol-1①
Na2O2(s)+CO2(g)=Na2CO3(s)+
 O2(g) ΔH=-226 kJ•mol-1 ②
O2(g) ΔH=-226 kJ•mol-1 ②则CO(g)与Na2O2(s)反应放出509kJ热量时,电子转移数目为
(4)已知H2(g)+Br2(l)=2HBr(g) ΔH=-72kJ•mol-1,蒸发1mol Br2(l)需要吸收的能量为30kJ,其他相关数据如下表:
| 物质 | H2(g) | Br2(g) | HBr(g) |
| 1 mol分子中的化学键断裂时需要吸收的能量(kJ) | 436 | 200 | a |
您最近一年使用:0次



