实验室利用反应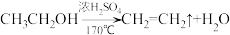 制取乙烯,图1为乙烯的制取及乙烯还原性的验证装置图。
制取乙烯,图1为乙烯的制取及乙烯还原性的验证装置图。
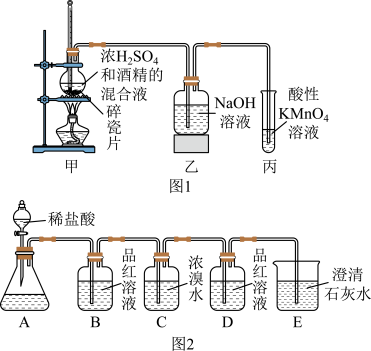
请回答下列问题:
(1)混合浓硫酸和乙醇的方法是_______ 。
(2)碎瓷片的作用是_______ ,若实验中加热一段时间后发现忘记加碎瓷片,则应该采取的措施是_______ 。
(3)能够说明乙烯具有还原性的现象是_______ 。
(4)实验中,因浓硫酸具有_______ 性,故烧瓶内产生的气体中还可能含①_______ 、②_______ ,(填分子式)为检验可能产生的气体,设计如图2所示装置进行检验,将图1装置_______ (填“甲”、“乙”或“丙”)中溶液转移到图2的锥形瓶中,打开分液漏斗活塞,进行实验。则能说明有气体①产生的实验现象是_______ ,能说明有气体②产生的实验现象是_______ 。
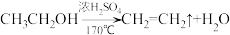 制取乙烯,图1为乙烯的制取及乙烯还原性的验证装置图。
制取乙烯,图1为乙烯的制取及乙烯还原性的验证装置图。
请回答下列问题:
(1)混合浓硫酸和乙醇的方法是
(2)碎瓷片的作用是
(3)能够说明乙烯具有还原性的现象是
(4)实验中,因浓硫酸具有
20-21高二下·河北·阶段练习 查看更多[4]
广东省揭阳第一中学2020-2021学年高二下学期期中考试化学试题专题3 综合检测-苏教版2020选择性必修3(已下线)微专题22 二氧化硫性质四重性探究-备战2022年高考化学考点微专题河北省大联考2020-2021学年高二下学期4月月考化学试题
更新时间:2021-06-19 09:08:04
|
相似题推荐
【推荐1】为探究工业尾气处理副产品X(黑色固体,仅含两种元素)的组成和性质,设计并完成如下实验:

请回答:
(1)X含有的两种元素是__________ ,其化学式是____________ 。
(2)无色气体D与氯化铁溶液反应的离子方程式是____________________ 。
(3)已知化合物X能与稀盐酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518 g·L-1),写出该反应的化学方程式________________________________________ 。

请回答:
(1)X含有的两种元素是
(2)无色气体D与氯化铁溶液反应的离子方程式是
(3)已知化合物X能与稀盐酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518 g·L-1),写出该反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】如图所示装置可进行二氧化硫的制备和某些性质的实验,请回答下列问题:
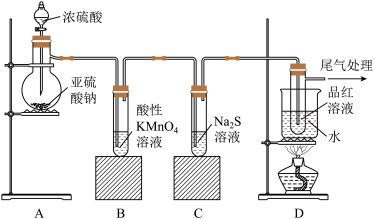
(1)A中盛放浓硫的仪器名称是______________ 。
(2)实验过程中,装置B试管内的___________ 现象证明SO2具有______ 性。
(3)实验过程中,装置C试管内的__________ 现象证明SO2具有______ 性,反应化学方程式为_____________ 。
(4)D的作用是_______ 。
(5)尾气可采用_____________ 溶液吸收。

(1)A中盛放浓硫的仪器名称是
(2)实验过程中,装置B试管内的
(3)实验过程中,装置C试管内的
(4)D的作用是
(5)尾气可采用
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】过氧化钠(Na2O2)是中学常见物质。已知:CO2与SO2均可与Na2O2反应。有人提出CO2、SO2与Na2O2的反应原理相同;但也有人提出,SO2具有较强还原性,与Na2O2反应可能会生成Na2SO4,而CO2无还原性,故反应原理不相同。
(1)下列溶液中,不能用于鉴别SO2和CO2气体的是___________ (填字母编号)。
A.酸化的Ba(NO3)2溶液 B.澄清石灰水 C.酸性高锰酸钾溶液 D.BaCl2溶液 E.品红溶液
(2)实验一:向一定量的Na2O2固体中通入足量的SO2,取反应后的固体进行实验探究,以证明过氧化物与SO2反应的特点。提出假设:
假设1:反应后固体中只有___________ ,证明SO2未被氧化;
假设2:反应后固体中只有___________ ,证明SO2完全被氧化;
假设3:反应后固体中同时含有上述两种物质,证明SO2部分被氧化。
(3)实验二:通过测量气体的体积判断发生的化学反应,实验装置如下:
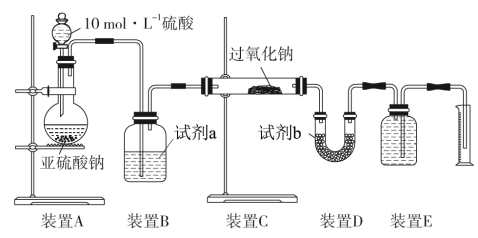
①试剂a可以选用___________ ,试剂b的作用是___________ 。
②若SO2完全被氧化,写出反应的化学方程式:___________ 。
③若SO2未被氧化,实验测得装置C中Na2O2质量增加了m g,装置E中收集气体为V L(标准状况下),用上述有关测量数据判断V与m的关系式:V =___________ (用含m的代数式表示,可不化简)。
(1)下列溶液中,不能用于鉴别SO2和CO2气体的是
A.酸化的Ba(NO3)2溶液 B.澄清石灰水 C.酸性高锰酸钾溶液 D.BaCl2溶液 E.品红溶液
(2)实验一:向一定量的Na2O2固体中通入足量的SO2,取反应后的固体进行实验探究,以证明过氧化物与SO2反应的特点。提出假设:
假设1:反应后固体中只有
假设2:反应后固体中只有
假设3:反应后固体中同时含有上述两种物质,证明SO2部分被氧化。
(3)实验二:通过测量气体的体积判断发生的化学反应,实验装置如下:

①试剂a可以选用
②若SO2完全被氧化,写出反应的化学方程式:
③若SO2未被氧化,实验测得装置C中Na2O2质量增加了m g,装置E中收集气体为V L(标准状况下),用上述有关测量数据判断V与m的关系式:V =
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
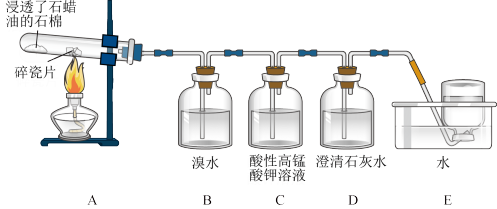
【推荐1】某同学设计实验探究工业制乙烯的原理和乙烯主要的化学性质,实验装置如图所示。
(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热、加压条件下发生反应生成不饱和烃。已知烃类都不与碱反应。
例如:石油分馏产物之一十六烷可发生如下反应,反应式已配平:C16H34 C8H18+甲,甲
C8H18+甲,甲 4乙,乙的电子式为
4乙,乙的电子式为_______ 。
(2)A装置中碎瓷片的作用是_______ ,写出B装置中发生的化学反应方程式_______ ,该反应类型是_______ 。
(3)C装置中的实验现象是_______ ,观察到D装置中澄清的石灰水变浑浊,请写出C中发生反应的离子方程式_______ 。
(4)通过题述实验探究可知,检验甲烷和乙烯的方法是_______ (填序号,下同);除去甲烷中乙烯的方法是_______ 。
A.气体通入水中
B.气体通过装溴水的洗气瓶
C.气体通过装酸性高锰酸钾溶液的洗气瓶
D.气体通过氢氧化钠溶液

(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热、加压条件下发生反应生成不饱和烃。已知烃类都不与碱反应。
例如:石油分馏产物之一十六烷可发生如下反应,反应式已配平:C16H34
 C8H18+甲,甲
C8H18+甲,甲 4乙,乙的电子式为
4乙,乙的电子式为(2)A装置中碎瓷片的作用是
(3)C装置中的实验现象是
(4)通过题述实验探究可知,检验甲烷和乙烯的方法是
A.气体通入水中
B.气体通过装溴水的洗气瓶
C.气体通过装酸性高锰酸钾溶液的洗气瓶
D.气体通过氢氧化钠溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
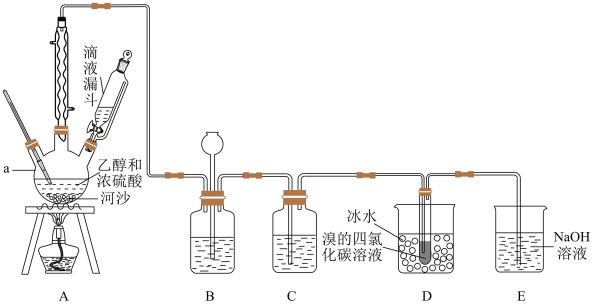
【推荐2】实验室利用下图装置用乙醇和浓硫酸反应制取乙烯,再用乙烯与溴的四氯化碳溶液反应制备1,2-二溴乙烷。
(1)在装置A中,生成的气体除乙烯外还有乙醚、CO2、SO2等,则生成乙烯的化学方程式为______________ ,河沙的作用是________________ 。仪器a的名称为________________________ 。
(2)装置B可起到安全瓶的作用,若气压过大,该装置中出现的现象为___________ 。
(3)装置C可除去CO2、SO2,所盛放的溶液为________________________ 。
(4)装置D中进行的主要反应的化学方程式为____________________________ ;把试管置于盛有冰水的小烧杯中的目的是_______________________________ 。
(1)在装置A中,生成的气体除乙烯外还有乙醚、CO2、SO2等,则生成乙烯的化学方程式为
(2)装置B可起到安全瓶的作用,若气压过大,该装置中出现的现象为
(3)装置C可除去CO2、SO2,所盛放的溶液为
(4)装置D中进行的主要反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
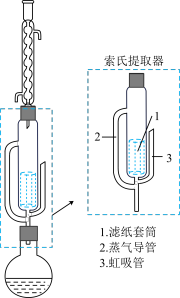
【推荐3】1,2-二溴乙烷常用作杀虫剂,某同学用如图装置制备 1,2-二溴乙烷。

І.1,2-二溴乙烷的制备实验步骤:按图示连接装置,先将C与D连接处断开,再对装置A中粗砂加热,待温度升到150 ℃左右时,连接C与D,并迅速将A内反应温度升温至160~180 ℃,从滴液漏斗中慢慢滴加乙醇和浓硫酸混合液,装置D试管中装有 5.0 mL 10 mol/LBr2的CCl4 溶液,进行1,2-二溴乙烷的纯化。
已知:①浓硫酸具有强氧化性,在加热时可能有一部分与乙醇发生氧化还原反应。②1,2-二溴乙烷的沸点为131℃,熔点为9.3℃。
完成下列填空:
(1)反应前装置A中加入少量粗砂目的是_______ 。装置A中发生的主要反应是_______ 。
(2)装置C的作用_______ 。
(3)装置D的烧杯中需加入冷却剂,下列冷却剂合适的为_______ 。
a.冰水混合物 b.5℃的水 c.10℃的水
Ⅱ.1,2-二溴乙烷的纯化
步骤①:冷却后,把装置D试管中的产物转移至分液漏斗中,用1%的氢氧化钠水溶液洗涤。
步骤②:用水洗至中性。
步骤③:“向所得的有机层中加入适量无水氯化钙,过滤,转移至蒸馏烧瓶中蒸馏,收集130~132℃的馏分,得到产品6.392g。
(4)步骤①中加入1%的氢氧化钠水溶液时,发生反应的离子方程式为_______ 。
(5)该实验所得产品的产率为_______ 。(保留小数点后两位)
(6)有机物纯化过程会进行多次萃取,为了克服多次萃取实验操作繁琐,萃取剂消耗量过大的缺点,FranzvonSoxhlet发明了索氏提取法其装置如图所示。我们可以利用该装置从青蒿中提取青蒿素,实验时需将青蒿切成小段,放入滤纸套筒1中,烧瓶中溶剂受热蒸发,蒸气沿蒸气导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现连续萃取。萃取完全后,青蒿素位于_______ (填“圆底烧瓶”或“索氏提取器”)中。

І.1,2-二溴乙烷的制备实验步骤:按图示连接装置,先将C与D连接处断开,再对装置A中粗砂加热,待温度升到150 ℃左右时,连接C与D,并迅速将A内反应温度升温至160~180 ℃,从滴液漏斗中慢慢滴加乙醇和浓硫酸混合液,装置D试管中装有 5.0 mL 10 mol/LBr2的CCl4 溶液,进行1,2-二溴乙烷的纯化。
已知:①浓硫酸具有强氧化性,在加热时可能有一部分与乙醇发生氧化还原反应。②1,2-二溴乙烷的沸点为131℃,熔点为9.3℃。
完成下列填空:
(1)反应前装置A中加入少量粗砂目的是
(2)装置C的作用
(3)装置D的烧杯中需加入冷却剂,下列冷却剂合适的为
a.冰水混合物 b.5℃的水 c.10℃的水
Ⅱ.1,2-二溴乙烷的纯化
步骤①:冷却后,把装置D试管中的产物转移至分液漏斗中,用1%的氢氧化钠水溶液洗涤。
步骤②:用水洗至中性。
步骤③:“向所得的有机层中加入适量无水氯化钙,过滤,转移至蒸馏烧瓶中蒸馏,收集130~132℃的馏分,得到产品6.392g。
(4)步骤①中加入1%的氢氧化钠水溶液时,发生反应的离子方程式为
(5)该实验所得产品的产率为
(6)有机物纯化过程会进行多次萃取,为了克服多次萃取实验操作繁琐,萃取剂消耗量过大的缺点,FranzvonSoxhlet发明了索氏提取法其装置如图所示。我们可以利用该装置从青蒿中提取青蒿素,实验时需将青蒿切成小段,放入滤纸套筒1中,烧瓶中溶剂受热蒸发,蒸气沿蒸气导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现连续萃取。萃取完全后,青蒿素位于

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,不溶于水,易溶于醇等有机溶剂。实验室制备1,2-二溴乙烷的装置如图所示:

有关数据列表如下:
回答下列问题:
(1)在此制备实验中,A中按最佳体积比3﹕1加入乙醇与浓硫酸后,A中还要加入几粒碎瓷片,其作用是___________ ,然后尽可能迅速地把反应温度提高到170℃左右,写出此时A中发生的主反应的化学方程式___________ 。
(2)装置B的作用是作安全瓶,瓶中盛水,除了可以防止倒吸以外,还可判断装置是否堵塞,若堵塞,B中现象是___________ 。
(3)在装置C中应加入NaOH溶液,其目的是___________ 。
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在___________ 层(填“上”或“下”)。若产物中有少量副产物乙醚,可用___________ (填操作方法名称)的方法除去。
(5)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是___________ 。

有关数据列表如下:
| 类别 | 乙醇 | 1,2-二溴乙烷 | 乙醚 |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)在此制备实验中,A中按最佳体积比3﹕1加入乙醇与浓硫酸后,A中还要加入几粒碎瓷片,其作用是
(2)装置B的作用是作安全瓶,瓶中盛水,除了可以防止倒吸以外,还可判断装置是否堵塞,若堵塞,B中现象是
(3)在装置C中应加入NaOH溶液,其目的是
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在
(5)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】乙烯是一种重要的化工原料,某同学设计实验探究工业制备乙烯的原理(如下图A可以制得)和乙烯的主要化学性质,实验装置如图所示。
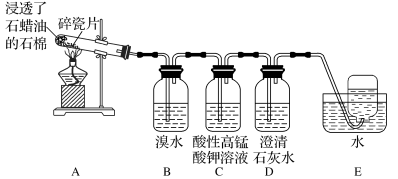
(1)B装置中的实验现象:_______ ,其反应的类型是_______ 。
(2)通过上述实验探究可知,检验甲烷和乙烯的方法是_______
(3)乙烯可以生产日常生活使用高分子材料塑料,写出其反应的化学方程式_______ 。

(1)B装置中的实验现象:
(2)通过上述实验探究可知,检验甲烷和乙烯的方法是_______
| A.将气体通入水中 |
| B.将气体通过装溴水的洗气瓶 |
| C.将气体通过装酸性高锰酸钾溶液的洗气瓶 |
| D.将气体通入氢氧化钠溶液中 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】下图是实验室用来验证乙烯与氢气反应产物的装置,请回答下列问题:
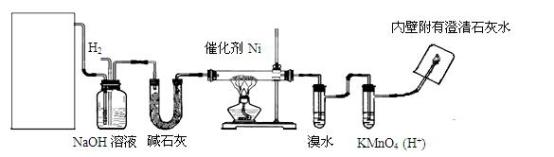
(1)方框内装置用来制取乙烯,其中包括的仪器是:①碎瓷片②石棉网和铁架台③圆底烧瓶④温度计(量程100℃)⑤温度计(量程200℃)⑥酒精灯⑦单孔塞⑧双孔塞⑨导管。不选用的仪器有_______ (填编号)。
(2)写出制乙烯化学方程式:_______ 。
(3)碱石灰的作用是:_______ 。
(4)实验过程中,发现溴水会褪色,可能的原因是:_______ 。
(5)出现什么现象可说明生成了乙烷?_______ 。

(1)方框内装置用来制取乙烯,其中包括的仪器是:①碎瓷片②石棉网和铁架台③圆底烧瓶④温度计(量程100℃)⑤温度计(量程200℃)⑥酒精灯⑦单孔塞⑧双孔塞⑨导管。不选用的仪器有
(2)写出制乙烯化学方程式:
(3)碱石灰的作用是:
(4)实验过程中,发现溴水会褪色,可能的原因是:
(5)出现什么现象可说明生成了乙烷?
您最近一年使用:0次



