用滴管把新制的氯水逐滴加到含有酚酞的氢氧化钠溶液中,当加到最后一滴时,溶液的红色突然消失.对产生实验现象的原因有两种推测:①是氯水中的次氯酸的漂白性使它由红色变成无色;②是氯水的酸性(H+)使它由红色变成无色.假设其中一种是正确的。
请你设计一个实验,由实验现象对以上的推测作出判断.
(1)要使用的实验用品:____________________ ;
(2)要进行的实验操作:_____________________ ;
(3)实验现象和结论:_______________________ 。
请你设计一个实验,由实验现象对以上的推测作出判断.
(1)要使用的实验用品:
(2)要进行的实验操作:
(3)实验现象和结论:
11-12高一·全国·课时练习 查看更多[4]
人教版高中化学必修1第四章《非金属及其化合物》测试卷3人教版高中化学必修1第四章《非金属及其化合物》测试卷4(已下线)【走进新高考】(人教版必修一)4.2.1富集在海水中的元素——氯 (氯气) 同步练习01(已下线)2012年人教版高中化学必修一4.2 富集在海水中的元素-氯练习卷
更新时间:2016-12-09 03:43:17
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】下表是元素周期表的一部分,针对表中的①~⑨9种元素,填写下列空白:
(1)写出元素符号和名称:
①_____ ,②_____ ,⑧_____ ,⑨_____ 。
(2)写出下列反应的化学方程式:
⑦的单质跟④的氢氧化物溶液反应_____ 。
⑤的氧化物跟④的氢氧化物溶液反应:_____ 。
④的单质在③的单质中燃烧:_____ 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 四 | ⑨ |
①
(2)写出下列反应的化学方程式:
⑦的单质跟④的氢氧化物溶液反应
⑤的氧化物跟④的氢氧化物溶液反应:
④的单质在③的单质中燃烧:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】某学习小组用MnO2和浓盐酸共热制取氯气,再用氯气与潮湿的消石灰反应制取漂白粉(这是一个放热反应)。
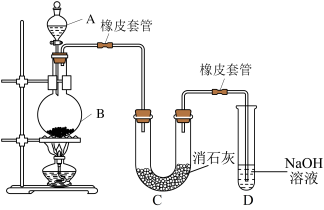
此实验Ca(ClO)2产率太低。经分析发现,主要原因是在U形管中存在两个副反应:
(1)温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是_______ 。
(2)试判断另一个副反应:_______ (用化学方程式表示)。为避免此副反应的发生,可采取的措施是_______ 。

此实验Ca(ClO)2产率太低。经分析发现,主要原因是在U形管中存在两个副反应:
(1)温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是
(2)试判断另一个副反应:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】下表列出了①~⑨九种元素在元素周期表中的位置:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为__________ 。
(2)在①~④四种元素的最高价氧化物对应的水化物中碱性最强的是__________ (填碱的化学式)。
(3)在⑤~⑦三种元素的最简单氢化物中,沸点最高的是__________ (用化学式填空)。
(4)写出⑧的单质与氢氧化钠溶液反应的化学方程式__________ 。
(5)写出①与⑦形成原子个数比为1:1的化合物的电子式__________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑤ | ⑥ | ⑦ | |||||
| 三 | ① | ③ | ④ | ⑧ | ⑨ | |||
| 四 | ② |
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为
(2)在①~④四种元素的最高价氧化物对应的水化物中碱性最强的是
(3)在⑤~⑦三种元素的最简单氢化物中,沸点最高的是
(4)写出⑧的单质与氢氧化钠溶液反应的化学方程式
(5)写出①与⑦形成原子个数比为1:1的化合物的电子式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】氯气(Cl2)是黄绿色气体,其水溶液叫氯水。把品红试纸(染有品红的纸)伸入氯水中,品红褪色。
发现问题:氯水中的哪些成分能使品红褪色呢?
查阅资料:氯气溶于水,部分与水反应,化学方程式为Cl2+H2O=HCl+HClO。其中,HClO名为次氯酸,是一种弱酸,具有强氧化。
猜想:
猜想1:是氯水中的水使品红褪色的;
猜想2:是氯水中的______ (填化学式)使品红褪色的;
猜想3:是氯水中的盐酸使品红褪色的;
猜想4:是氯水中的次氯酸使品红褪色的。
实验探究:
结论:氯水中的______ (填化学式)使品红褪色,具有漂白作用(能使品红等有色物质褪色)。
反思:
(1)氯水中加入AgNO3溶液有白色沉淀生成,化学方程式为______ 。
(2)向氯水中滴加紫色石蕊溶液,观察到的现象是______ 。
发现问题:氯水中的哪些成分能使品红褪色呢?
查阅资料:氯气溶于水,部分与水反应,化学方程式为Cl2+H2O=HCl+HClO。其中,HClO名为次氯酸,是一种弱酸,具有强氧化。
猜想:
猜想1:是氯水中的水使品红褪色的;
猜想2:是氯水中的
猜想3:是氯水中的盐酸使品红褪色的;
猜想4:是氯水中的次氯酸使品红褪色的。
实验探究:
| 实验操作 | 实验现象 | 过程分析 |
| ①把品红试纸伸入水中 | 没有褪色 | 猜想1不成立 |
| ②把品红试纸伸入干燥的氯气中 | 没有褪色 | 猜想2不成立 |
| ③ | 没有褪色 | 猜想3不成立 |
反思:
(1)氯水中加入AgNO3溶液有白色沉淀生成,化学方程式为
(2)向氯水中滴加紫色石蕊溶液,观察到的现象是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】某学生发现氯水能使有色布条褪色,氯水的成分比较复杂,那么氯水中究竟什么成分具有漂白性呢?带着疑问,他做了如下探究:
(1)查找资料后得知氯水的成分有____ 、___ 、____ 、____ 、____ 、____ 、____ 。
(2)根据资料查阅和实验结果分析, 新制的氯水呈____ 色,氯水中含有多种微粒.将紫色石蕊试液滴入其中,溶液显红色.起作用的微粒是___ ;过一会儿,溶液的颜色逐渐褪去,起作用的微粒是___ 。该物质之所以具有漂白性,与它的_______ (填性质)有关。往氯水中滴入硝酸银溶液,产生白色沉淀,起作用的微粒是____ 。氯水能使淀粉碘化钾试纸变蓝,起作用的是____ .(本小题中除第一个外,其余每个空格处都请填写微粒的符号)
(3)从以上过程可看出,该学生的探究活动体现了最基本的科学研究方法,即:
提出问题→________ →________ →分析归纳→得出结论
(1)查找资料后得知氯水的成分有
(2)根据资料查阅和实验结果分析, 新制的氯水呈
(3)从以上过程可看出,该学生的探究活动体现了最基本的科学研究方法,即:
提出问题→
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】某化学兴趣小组用如图装置制取并探究氯气的性质。[A装置中发生反应的化学方程式: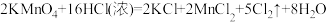 ]
]

(1)A装置中a仪器的名称是_____________________ 。
(2)实验室制氯气也可用 MnO2与浓盐酸反应,化学方程式为_____________________ 。
(3)实验进行一段时间后,可观察到_____________________ (填“B”或“C”)装置中有色布条褪色,请用化学方程式表示其褪色原因_____________________ 。
(4)当氯气进入D装置后,可观察到溶液颜色变为_____________________ (填“红色”或“蓝色”)。
(5)E装置的作用是_____________________ 。
(6)用 31.6g KMnO4固体与足量的浓盐酸反应,最多可生成标准状况下_____________________ L氯气。
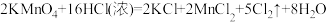 ]
]
(1)A装置中a仪器的名称是
(2)实验室制氯气也可用 MnO2与浓盐酸反应,化学方程式为
(3)实验进行一段时间后,可观察到
(4)当氯气进入D装置后,可观察到溶液颜色变为
(5)E装置的作用是
(6)用 31.6g KMnO4固体与足量的浓盐酸反应,最多可生成标准状况下
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】某实验小组欲探究Na2CO3和NaHCO3的性质,发现实验室里盛放这两种固体的试剂瓶丢失了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊。
①A是___________ (写名称);写出种A的一用途:__________________ 。
②A受热分解的化学方程式为__________________ 。
③加热结束后,该实验小组还测定了A受热分解后制得的纯碱样品的纯度:称取m g样品,置于小烧杯中,加水溶解,滴加足量CaCl2溶液。将反应混合物过滤、洗涤、干燥、称量得到的固体的质量为n g。则制得的该纯碱样品的纯度为____________ (用含m、n的代数式表示)。
(2)称取A、B两种固体各2 g,分别加入两个小烧杯中,再各加10 mL 蒸馏水,振荡,恢复至室温,发现Na2CO3固体完全溶解,而NaHCO3固体有剩余,由此得出结论:_________ 。
(3)如图所示,在气密性良好的装置Ⅰ和Ⅱ中分别放入药品,将气球内的固体同时倒入试管中。
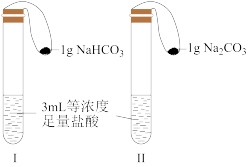
①两试管中均产生气体,_______ (填“Ⅰ”或“Ⅱ”)的反应程度更为剧烈。
②反应结束后,气球均有膨胀,恢复至室温,下列说法正确的是_______ 。
a.装置Ⅰ的气球体积较大 b.装置Ⅱ的气球体积较大
c.装置Ⅰ的气球体积等于装置Ⅱ的气球体积 d.无法判断
(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊。
①A是
②A受热分解的化学方程式为
③加热结束后,该实验小组还测定了A受热分解后制得的纯碱样品的纯度:称取m g样品,置于小烧杯中,加水溶解,滴加足量CaCl2溶液。将反应混合物过滤、洗涤、干燥、称量得到的固体的质量为n g。则制得的该纯碱样品的纯度为
(2)称取A、B两种固体各2 g,分别加入两个小烧杯中,再各加10 mL 蒸馏水,振荡,恢复至室温,发现Na2CO3固体完全溶解,而NaHCO3固体有剩余,由此得出结论:
(3)如图所示,在气密性良好的装置Ⅰ和Ⅱ中分别放入药品,将气球内的固体同时倒入试管中。

①两试管中均产生气体,
②反应结束后,气球均有膨胀,恢复至室温,下列说法正确的是
a.装置Ⅰ的气球体积较大 b.装置Ⅱ的气球体积较大
c.装置Ⅰ的气球体积等于装置Ⅱ的气球体积 d.无法判断
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
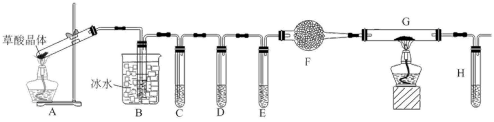
【推荐2】草酸晶体(H2C2O4·xH2O)无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解,草酸钙难溶于水。某研究性小组按照如图装置,检验草酸晶体的分解产物中含有CO、CO2.已知C、E、H中盛装澄清石灰水,D中盛装浓NaOH溶液,G中盛有CuO。
(1)装置B的主要作用是_______ 。
(2)装置C中反应的离子方程式为_______ 。
(3)能证明草酸晶体分解产物中有CO的现象是_______ 。
(4)为测定草酸晶体分子式(H2C2O4·xH2O)中x的值,现做如下实验。
①称取6.3g草酸晶体,将其配置成100.0mL水溶液为待测溶液;
②取25.0mL待测溶液放入锥形瓶中,再加入适量的稀硫酸;
③用浓度为0.4mol/L的KMnO4标准溶液进行滴定,达到滴定终点时,用去12.50mLKMnO4溶液。
写出H2C2O4和酸性KMnO4溶液反应的化学方程式_______ ;经计算x=_______ 。
(5)依据以上实验,写出草酸晶体(H2C2O4·xH2O)受热分解的化学方程式_______ 。

(1)装置B的主要作用是
(2)装置C中反应的离子方程式为
(3)能证明草酸晶体分解产物中有CO的现象是
(4)为测定草酸晶体分子式(H2C2O4·xH2O)中x的值,现做如下实验。
①称取6.3g草酸晶体,将其配置成100.0mL水溶液为待测溶液;
②取25.0mL待测溶液放入锥形瓶中,再加入适量的稀硫酸;
③用浓度为0.4mol/L的KMnO4标准溶液进行滴定,达到滴定终点时,用去12.50mLKMnO4溶液。
写出H2C2O4和酸性KMnO4溶液反应的化学方程式
(5)依据以上实验,写出草酸晶体(H2C2O4·xH2O)受热分解的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某实验小组设计实验探究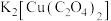 (二草酸合铜酸钾)的热分解产物,装置如下图所示:
(二草酸合铜酸钾)的热分解产物,装置如下图所示:
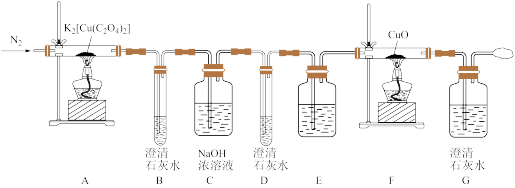
(1)E的广口瓶中盛放的药品是_______________ 。
(2)通过实验证明分解产物中有 、
、 生成,能说明分解产物中有
生成,能说明分解产物中有 的现象是
的现象是________ 。
(3)停止实验时先熄灭两个酒精灯,继续通入 至室温的目的是
至室温的目的是________ 。
(4)取A中的残留固体(已完全分解)溶于水过滤、洗涤,得砖红色滤渣和无色溶液,通过实验证明无色溶液中含 和
和 ,其中验证
,其中验证 的操作是
的操作是_______ ;取少量砖红色滤渣加入稀硫酸,产生蓝色溶液且有红色固体生成,则砖红色滤渣是____________ (一种氧化物)。
(5)依据上述实验,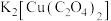 分解的化学方程式为
分解的化学方程式为_______ 。
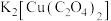 (二草酸合铜酸钾)的热分解产物,装置如下图所示:
(二草酸合铜酸钾)的热分解产物,装置如下图所示:
(1)E的广口瓶中盛放的药品是
(2)通过实验证明分解产物中有
 、
、 生成,能说明分解产物中有
生成,能说明分解产物中有 的现象是
的现象是(3)停止实验时先熄灭两个酒精灯,继续通入
 至室温的目的是
至室温的目的是(4)取A中的残留固体(已完全分解)溶于水过滤、洗涤,得砖红色滤渣和无色溶液,通过实验证明无色溶液中含
 和
和 ,其中验证
,其中验证 的操作是
的操作是(5)依据上述实验,
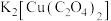 分解的化学方程式为
分解的化学方程式为
您最近一年使用:0次



