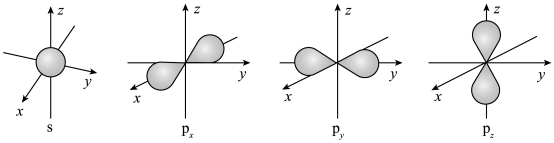
主族元素碳、氧、氮、氟、磷、氯、硒及副族元素镍、铜元素在化学中有很重要的地位,回答下列问题:
(1)在基态14C原子中,核外存在___________ 对自旋相反的电子
(2)X元素的原子最外层电子排布式为(n+1)sn(n+1)pn+1,则X的氢化物的化学式是___________
(3)第三周期第一电离能处于Al和P之间的元素有___________ 种。
(4)某种原子的结构示意图为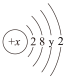 。则该原子的核电荷数x取值范围为
。则该原子的核电荷数x取值范围为___________ 。
(1)在基态14C原子中,核外存在
(2)X元素的原子最外层电子排布式为(n+1)sn(n+1)pn+1,则X的氢化物的化学式是
(3)第三周期第一电离能处于Al和P之间的元素有
(4)某种原子的结构示意图为
 。则该原子的核电荷数x取值范围为
。则该原子的核电荷数x取值范围为
更新时间:2021-07-09 07:41:00
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】钾和碘的相关化合物在化工、医药、材料等领域有广泛的应用。回答下列问题:
(1)钾元素的焰色为紫色,该过程中其原子光谱属于______ 光谱(选填“吸收”或“发射”)。
(2)碘原子中,占据最高能级的电子的电子云轮廓图形状为______ 。
(3)请写出基态钾原子的核外电子排布式______ 。
(4)请比较KI与KCl晶体的熔点高低______ ,并说明理由:______ 。
(5)KIO3常用作食盐添加剂,其晶胞如图所示。

① 离子的立体构型为
离子的立体构型为______ 。
②已知KIO3晶胞的边长为apm,晶胞中K、I、O原子分别处于顶角、体心、面心位置。则每个K原子周围距离最短的O原子有______ 个。该晶胞的密度为______ g/cm3。
(1)钾元素的焰色为紫色,该过程中其原子光谱属于
(2)碘原子中,占据最高能级的电子的电子云轮廓图形状为
(3)请写出基态钾原子的核外电子排布式
(4)请比较KI与KCl晶体的熔点高低
(5)KIO3常用作食盐添加剂,其晶胞如图所示。

①
 离子的立体构型为
离子的立体构型为②已知KIO3晶胞的边长为apm,晶胞中K、I、O原子分别处于顶角、体心、面心位置。则每个K原子周围距离最短的O原子有
您最近一年使用:0次
【推荐2】请填空:
(1)基态F原子核外电子的运动状态有_______ 种。
(2)对于基态Cr原子,下列叙述正确的是_______ (填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为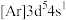
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用—
表示,与之相反的用— 表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和为_______ 。
(1)基态F原子核外电子的运动状态有
(2)对于基态Cr原子,下列叙述正确的是
A.轨道处于半充满时体系总能量低,核外电子排布应为
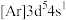
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
 表示,与之相反的用—
表示,与之相反的用— 表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】乙炔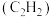 和丙烯腈
和丙烯腈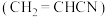 是有机合成工业的重要原料。工业上曾用
是有机合成工业的重要原料。工业上曾用 和
和 反应制取乙炔,用乙炔和氢氰酸(
反应制取乙炔,用乙炔和氢氰酸( )在氯化亚铜等催化作用下生产丙烯腈。
)在氯化亚铜等催化作用下生产丙烯腈。
(1) 的基态核外电子排布式为
的基态核外电子排布式为_______ 。 元素在周期表中的位置为
元素在周期表中的位置为_______ 。
(2)基态N原子第一电离能比基态O原子_______ (填“高”,“低”或“相等”)
(3) 的分子构型为
的分子构型为_______ 。
(4)每个丙烯腈分子中碳原子的杂化轨道类型有_______ 。
(5) 丙烯腈分子中含
丙烯腈分子中含 键的物质的量为
键的物质的量为_______  。
。
(6)丙烯腈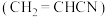 分子中共面的原子数目最多为
分子中共面的原子数目最多为_______ 。
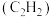 和丙烯腈
和丙烯腈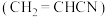 是有机合成工业的重要原料。工业上曾用
是有机合成工业的重要原料。工业上曾用 和
和 反应制取乙炔,用乙炔和氢氰酸(
反应制取乙炔,用乙炔和氢氰酸( )在氯化亚铜等催化作用下生产丙烯腈。
)在氯化亚铜等催化作用下生产丙烯腈。(1)
 的基态核外电子排布式为
的基态核外电子排布式为 元素在周期表中的位置为
元素在周期表中的位置为(2)基态N原子第一电离能比基态O原子
(3)
 的分子构型为
的分子构型为(4)每个丙烯腈分子中碳原子的杂化轨道类型有
(5)
 丙烯腈分子中含
丙烯腈分子中含 键的物质的量为
键的物质的量为 。
。(6)丙烯腈
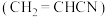 分子中共面的原子数目最多为
分子中共面的原子数目最多为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按照下列元素基态原子的电子排布特征判断元素,并回答问题:A原子中只有一个电子层且只含有一个电子;B原子的3p轨道上得到一个电子后没有未配对电子;C原子的2p轨道上没有空轨道上且电子的自旋方向相同;D原子的第三电子层上有8个电子,第四层上只有1个电子;E原子的价电子排布式为3s23p6。
(1)下列元素的名称是:B:________ ;E:________ ;
(2)D原子在元素周期表的___________ 区。
(3)C原子的电子排布图____________________ 。
(4)B原子的核外价电子排布式________________ 。
(1)下列元素的名称是:B:
(2)D原子在元素周期表的
(3)C原子的电子排布图
(4)B原子的核外价电子排布式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其基态原子的电子排布图为___________ 。
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B-的结构示意图为___________ ,C元素在元素周期表的___________ 区,写出常温下B的单质与C的最高价氧化物对应水化物反应的化学方程式:___________ 。
(3)D元素的正三价离子的3d能级为半充满状态,其基态原子的电子排布式为___________ 。
试根据原子核外电子排布所遵循的原理解释D的二价阳离子具有较强的还原性,易被氧化为正三价离子的原因:___________ 。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的价电子排布式为___________ 。
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其基态原子的电子排布图为
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B-的结构示意图为
(3)D元素的正三价离子的3d能级为半充满状态,其基态原子的电子排布式为
试根据原子核外电子排布所遵循的原理解释D的二价阳离子具有较强的还原性,易被氧化为正三价离子的原因:
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的价电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(CH2=CH2)与四氟乙烯(CF2=CF2)的共聚物(ETFE)制成。回答下列问题:
(1)基态F原子的价电子排布图(轨道表示式)为_______ 。
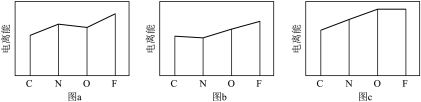
(2)图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第一电离能的变化图是_______ (填标号),判断的根据是_______ ;第三电离能的变化图是_______ (填标号)。
(1)基态F原子的价电子排布图(轨道表示式)为
(2)图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第一电离能的变化图是

您最近一年使用:0次
【推荐2】(1)可正确表示原子轨道的是___________ 。
A.2s B.2d C.3px D.3f
(2)写出基态镓(Ga)原子的价电子排布式:___________ 。
(3)下列物质中,只含有极性键的分子是_____ ,既含离子键又含共价键的化合物是_______ ;只存在σ键的分子是_______ ,同时存在σ键和π键的分子是_____ 。
A.N2 B.CO2 C.CH2Cl2 D.C2H4 E.C2H6 F.CaCl2 G.NH4Cl
(4)用“>”“<”或“=”填空:第一电离能的大小:Mg____ Al;
A.2s B.2d C.3px D.3f
(2)写出基态镓(Ga)原子的价电子排布式:
(3)下列物质中,只含有极性键的分子是
A.N2 B.CO2 C.CH2Cl2 D.C2H4 E.C2H6 F.CaCl2 G.NH4Cl
(4)用“>”“<”或“=”填空:第一电离能的大小:Mg
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】第四周期的过渡元素在工业、农业、科学技术以及人类生活等方面有重要作用。回答下列问题:
(1)钒(V)及其化合物广泛应用于工业催化、新材料等领域。
①周期表中铬位于钒旁边,基态铬原子的价层电子排布图为_______ 。
② 是一种常见的催化剂,在合成硫酸中起到重要作用,其结构式如图所示:
是一种常见的催化剂,在合成硫酸中起到重要作用,其结构式如图所示:

则 分子中σ键和π键数目之比为
分子中σ键和π键数目之比为_______ 。 溶解在NaOH溶液中,可得到钒酸钠(Na3VO4)。
溶解在NaOH溶液中,可得到钒酸钠(Na3VO4)。 与
与 的空间构型相同,其中V原子的杂化方式为
的空间构型相同,其中V原子的杂化方式为_______ 。
(2)①科学研究表明用 作光催化剂可处理废水中的
作光催化剂可处理废水中的 ,则
,则 的电子式为
的电子式为_______ 。
② 是一种储氢材料。基态B原子核外电子的运动状态有
是一种储氢材料。基态B原子核外电子的运动状态有_______ 种。
(3)甘氨酸亚铁络合物[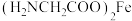 ]广泛用于缺铁性贫血的预防和治疗。
]广泛用于缺铁性贫血的预防和治疗。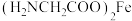 中含有的第二周期元素的第一电离能由大到小的顺序为
中含有的第二周期元素的第一电离能由大到小的顺序为_______ (用元素符号表示)。
(4)Ni(CO)4常温下为无色液体,沸点42.1℃,熔点-19.3℃,难溶于水,易溶于有机溶剂。推测Ni(CO)4是_______ 分子(填“极性”或“非极性”)。
(1)钒(V)及其化合物广泛应用于工业催化、新材料等领域。
①周期表中铬位于钒旁边,基态铬原子的价层电子排布图为
②
 是一种常见的催化剂,在合成硫酸中起到重要作用,其结构式如图所示:
是一种常见的催化剂,在合成硫酸中起到重要作用,其结构式如图所示:
则
 分子中σ键和π键数目之比为
分子中σ键和π键数目之比为 溶解在NaOH溶液中,可得到钒酸钠(Na3VO4)。
溶解在NaOH溶液中,可得到钒酸钠(Na3VO4)。 与
与 的空间构型相同,其中V原子的杂化方式为
的空间构型相同,其中V原子的杂化方式为(2)①科学研究表明用
 作光催化剂可处理废水中的
作光催化剂可处理废水中的 ,则
,则 的电子式为
的电子式为②
 是一种储氢材料。基态B原子核外电子的运动状态有
是一种储氢材料。基态B原子核外电子的运动状态有(3)甘氨酸亚铁络合物[
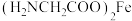 ]广泛用于缺铁性贫血的预防和治疗。
]广泛用于缺铁性贫血的预防和治疗。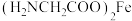 中含有的第二周期元素的第一电离能由大到小的顺序为
中含有的第二周期元素的第一电离能由大到小的顺序为(4)Ni(CO)4常温下为无色液体,沸点42.1℃,熔点-19.3℃,难溶于水,易溶于有机溶剂。推测Ni(CO)4是
您最近一年使用:0次