X、Y、Z、Q四种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳中含量(质量分数)最多的元素,Q的核电荷数是X与Z的核电荷数之和。请回答下列问题。
(1)X、Y的元素符号依次为___________ 、___________ 。
(2)XZ2与YZ2分别属于___________ (填“极性分子”或“非极性分子”,下同)和___________ 。
(3)Q的元素符号是___________ ,它位于第___________ 周期,它的基态原子的核外电子排布式为___________ ,在形成化合物时它的最高化合价为___________ 。
(1)X、Y的元素符号依次为
(2)XZ2与YZ2分别属于
(3)Q的元素符号是
更新时间:2021-07-09 18:57:17
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】铁、钴、镍都属于第Ⅷ族元素,它们的单质、合金及其化合物在催化剂和能源领域用途非常广泛。
⑴基态Fe2+的核外电子排布式为____ 。结合电子排布式分析Fe3+比Co3+氧化性弱的原因:_____ 。
⑵BNCP可用于激光起爆器等,BNCP可由N2H4、HClO4、CTCN、NaNT共反应制备。
①ClO4-的空间构型为________ 。
②CTCN的化学式为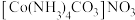 ,与Co3+形成配位键的原子是
,与Co3+形成配位键的原子是________ 。(已知CO32−的结构式为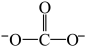 )
)
③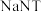 可以
可以 (双聚氰胺为原料制备。双聚氰胺中碳原子杂化轨道类型为
(双聚氰胺为原料制备。双聚氰胺中碳原子杂化轨道类型为________ ,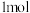
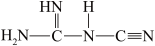 中含有σ键的物质的量为
中含有σ键的物质的量为________ 。
④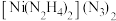 是一种富氮含能材料。配体N2H4能与水混溶,除因为它们都是极性分子外,还因为
是一种富氮含能材料。配体N2H4能与水混溶,除因为它们都是极性分子外,还因为_____ 。
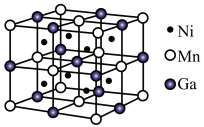
⑶一种新型的功能材料的晶胞结构如图所示,Mn在面心和顶点,它的化学式可表示为________ 。
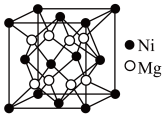
⑷镍镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。若该晶体储氢时,H2分子在晶胞的体心和棱的中心位置,距离最近的两个H2分子之间的距离为anm。则镍镁晶体未储氢时的密度为________ (列出计算表达式,NA表示阿伏加 德罗常数的数值) g∙cm-3。
⑴基态Fe2+的核外电子排布式为
⑵BNCP可用于激光起爆器等,BNCP可由N2H4、HClO4、CTCN、NaNT共反应制备。
①ClO4-的空间构型为
②CTCN的化学式为
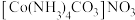 ,与Co3+形成配位键的原子是
,与Co3+形成配位键的原子是 )
)③
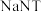 可以
可以 (双聚氰胺为原料制备。双聚氰胺中碳原子杂化轨道类型为
(双聚氰胺为原料制备。双聚氰胺中碳原子杂化轨道类型为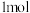
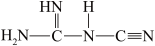 中含有σ键的物质的量为
中含有σ键的物质的量为④
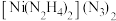 是一种富氮含能材料。配体N2H4能与水混溶,除因为它们都是极性分子外,还因为
是一种富氮含能材料。配体N2H4能与水混溶,除因为它们都是极性分子外,还因为⑶一种新型的功能材料的晶胞结构如图所示,Mn在面心和顶点,它的化学式可表示为

⑷镍镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。若该晶体储氢时,H2分子在晶胞的体心和棱的中心位置,距离最近的两个H2分子之间的距离为anm。则镍镁晶体未储氢时的密度为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】A、B、C、D、E、F的核电荷数依次增大。A的最外层电子数是次外层电子数的一半、是最内层电子数的2倍,D和E的价电子数都是7,F的基态原子中有4个未成对电子。
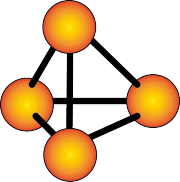
(1)A在元素周期表中的位置是_______ ,基态 的核外电子排布式是
的核外电子排布式是_______ 。
(2)A、B、C、D的第一电离能由小到大的顺序是_______ (用元素符号表示)。
(3) 分子的空间结构为
分子的空间结构为_______ 。
(4)单质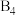 的结构如图所示,
的结构如图所示, 该分子中含有的
该分子中含有的 键的数目为
键的数目为_______ 。

(1)A在元素周期表中的位置是
 的核外电子排布式是
的核外电子排布式是(2)A、B、C、D的第一电离能由小到大的顺序是
(3)
 分子的空间结构为
分子的空间结构为(4)单质
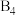 的结构如图所示,
的结构如图所示, 该分子中含有的
该分子中含有的 键的数目为
键的数目为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】钙和铜合金可用作电解制钙的阴极电极材料,回答下列问题:
(1)Cu在元素周期表中的位置是_______ ,基态Cu2+核外电子填充的最高能级符号为_____ 。
(2)CaCO3高温分解可制得CaO。CaO与C在一定条件下可生成CaC2,CaC2与水反应生成Ca(OH)2和一种4原子气体分子。
①该气体分子的电子式______ ,该气体分子中σ键与π键的数目之比为______ 。
②C原子未成对电子的数目为______ 。
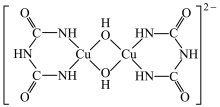
(3)在碱性溶液中,缩二脲HN(CONH2)2与CuSO4反应得到一种特征紫色物质,其结构如下图所示,该反应原理可用于检验蛋白质或其他含肽键的化合物。______ 、_______ 。
(1)Cu在元素周期表中的位置是
(2)CaCO3高温分解可制得CaO。CaO与C在一定条件下可生成CaC2,CaC2与水反应生成Ca(OH)2和一种4原子气体分子。
①该气体分子的电子式
②C原子未成对电子的数目为
(3)在碱性溶液中,缩二脲HN(CONH2)2与CuSO4反应得到一种特征紫色物质,其结构如下图所示,该反应原理可用于检验蛋白质或其他含肽键的化合物。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】铝的化合物在化工、医药、材料等方面应用广泛。回答下列问题:
(1) 分子中心原子的杂化方式为
分子中心原子的杂化方式为_______ ,其空间结构为_______ 。
(2) 属于
属于_______ (填“极性”或“非极性”)分子,其熔点低于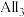 ,原因是
,原因是_______ 。
(3) (共价化合物,高熔、沸点)是良好的耐热冲击材料,其晶胞结构如图所示。
(共价化合物,高熔、沸点)是良好的耐热冲击材料,其晶胞结构如图所示。 晶胞中含有
晶胞中含有_______ 个Al,其配位数为_______ 。
②熔融 晶体,需要破坏的作用力是
晶体,需要破坏的作用力是_______ 。
③若 晶体的密度为
晶体的密度为 ,其晶胞参数为
,其晶胞参数为_______ nm(设 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(1)
 分子中心原子的杂化方式为
分子中心原子的杂化方式为(2)
 属于
属于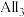 ,原因是
,原因是(3)
 (共价化合物,高熔、沸点)是良好的耐热冲击材料,其晶胞结构如图所示。
(共价化合物,高熔、沸点)是良好的耐热冲击材料,其晶胞结构如图所示。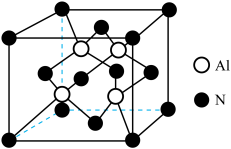
 晶胞中含有
晶胞中含有②熔融
 晶体,需要破坏的作用力是
晶体,需要破坏的作用力是③若
 晶体的密度为
晶体的密度为 ,其晶胞参数为
,其晶胞参数为 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
您最近一年使用:0次
【推荐2】用煤炭制得的焦炭在工业上是重要的还原剂和燃料,用于许多物质的例备,如工业上用焦炭与硫酸钠反应制备硫化钠。反应方程式如下:Na2SO4+2C Na2S+CO2↑
Na2S+CO2↑
完成下列填空:
(1)上述反应的元素中,原子半径最小的元素的原子的核外电子排布式为___________ ,其最外层电子有 ___________ 种不同的能量,有 ___________ 种不同的运动状态。
(2)下列可以证明二氧化碳是非极性分子的事实是___________ (填编号)。
a.二氧化碳密度比空气大
b.二氧化碳能溶于水
c.液态二氧化碳在电场中通过不偏向
d.二氧化碳常温常压下为气态
(3)判断C、S两种元素非金属性的强弱,并写出一个能支持你的结论的实验事实___________ ,
(4)工业上利用焦炭与高温水蒸气反应制备水煤气,下面是水煤气反应的方程式:C(s)+H2O(g) CO(g)+H2(g)-Q(Q<0),写出上述反应的平衡常数表达式
CO(g)+H2(g)-Q(Q<0),写出上述反应的平衡常数表达式 ___________ ,增大该反应平衡常数的措施有 ___________ (填编号)
A.升温 B.增加水蒸气的浓度 C.减压 D.增加焦炭的量
(5)在一个2L的容器中进行该反应的实验,若混合气体的密度不变,(填“能”或“不能”)___________ 判断该反应已经达到平衡状态。若初始加入的C为16.8g,10min后为7.2g,则v(H2)=___________ 。
 Na2S+CO2↑
Na2S+CO2↑完成下列填空:
(1)上述反应的元素中,原子半径最小的元素的原子的核外电子排布式为
(2)下列可以证明二氧化碳是非极性分子的事实是
a.二氧化碳密度比空气大
b.二氧化碳能溶于水
c.液态二氧化碳在电场中通过不偏向
d.二氧化碳常温常压下为气态
(3)判断C、S两种元素非金属性的强弱,并写出一个能支持你的结论的实验事实
(4)工业上利用焦炭与高温水蒸气反应制备水煤气,下面是水煤气反应的方程式:C(s)+H2O(g)
 CO(g)+H2(g)-Q(Q<0),写出上述反应的平衡常数表达式
CO(g)+H2(g)-Q(Q<0),写出上述反应的平衡常数表达式 A.升温 B.增加水蒸气的浓度 C.减压 D.增加焦炭的量
(5)在一个2L的容器中进行该反应的实验,若混合气体的密度不变,(填“能”或“不能”)
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】氮、磷、砷、锑为元素周期表中原子序数依次增大的同族元素。
(1)锑在元素周期表中的位置_______ 。
(2)除 外,科学家还先后研究出了
外,科学家还先后研究出了 、
、 、
、 、高聚氮等氮的单质。
、高聚氮等氮的单质。 为正四面体结构,高聚氮具有空间网状结构,如图所示。
为正四面体结构,高聚氮具有空间网状结构,如图所示。
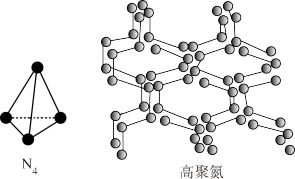
① 分子是一种
分子是一种_______ (填“极性”或“非极性”)分子。
② 的沸点
的沸点_______ (填“>”、“<”或“=”)高聚氮的沸点,原因是_______ 。
(3)热稳定性:
_______  (填“>”“<”),判断依据是
(填“>”“<”),判断依据是_______ 。
(4) 链状分子中所有原子都满足8电子稳定结构,则其分子中
链状分子中所有原子都满足8电子稳定结构,则其分子中 键与
键与 键之比为
键之比为_______ ,C原子的杂化类型为_______ 。
(1)锑在元素周期表中的位置
(2)除
 外,科学家还先后研究出了
外,科学家还先后研究出了 、
、 、
、 、高聚氮等氮的单质。
、高聚氮等氮的单质。 为正四面体结构,高聚氮具有空间网状结构,如图所示。
为正四面体结构,高聚氮具有空间网状结构,如图所示。
①
 分子是一种
分子是一种②
 的沸点
的沸点(3)热稳定性:

 (填“>”“<”),判断依据是
(填“>”“<”),判断依据是(4)
 链状分子中所有原子都满足8电子稳定结构,则其分子中
链状分子中所有原子都满足8电子稳定结构,则其分子中 键与
键与 键之比为
键之比为
您最近一年使用:0次



