用煤炭制得的焦炭在工业上是重要的还原剂和燃料,用于许多物质的例备,如工业上用焦炭与硫酸钠反应制备硫化钠。反应方程式如下:Na2SO4+2C Na2S+CO2↑
Na2S+CO2↑
完成下列填空:
(1)上述反应的元素中,原子半径最小的元素的原子的核外电子排布式为___________ ,其最外层电子有 ___________ 种不同的能量,有 ___________ 种不同的运动状态。
(2)下列可以证明二氧化碳是非极性分子的事实是___________ (填编号)。
a.二氧化碳密度比空气大
b.二氧化碳能溶于水
c.液态二氧化碳在电场中通过不偏向
d.二氧化碳常温常压下为气态
(3)判断C、S两种元素非金属性的强弱,并写出一个能支持你的结论的实验事实___________ ,
(4)工业上利用焦炭与高温水蒸气反应制备水煤气,下面是水煤气反应的方程式:C(s)+H2O(g) CO(g)+H2(g)-Q(Q<0),写出上述反应的平衡常数表达式
CO(g)+H2(g)-Q(Q<0),写出上述反应的平衡常数表达式 ___________ ,增大该反应平衡常数的措施有 ___________ (填编号)
A.升温 B.增加水蒸气的浓度 C.减压 D.增加焦炭的量
(5)在一个2L的容器中进行该反应的实验,若混合气体的密度不变,(填“能”或“不能”)___________ 判断该反应已经达到平衡状态。若初始加入的C为16.8g,10min后为7.2g,则v(H2)=___________ 。
 Na2S+CO2↑
Na2S+CO2↑完成下列填空:
(1)上述反应的元素中,原子半径最小的元素的原子的核外电子排布式为
(2)下列可以证明二氧化碳是非极性分子的事实是
a.二氧化碳密度比空气大
b.二氧化碳能溶于水
c.液态二氧化碳在电场中通过不偏向
d.二氧化碳常温常压下为气态
(3)判断C、S两种元素非金属性的强弱,并写出一个能支持你的结论的实验事实
(4)工业上利用焦炭与高温水蒸气反应制备水煤气,下面是水煤气反应的方程式:C(s)+H2O(g)
 CO(g)+H2(g)-Q(Q<0),写出上述反应的平衡常数表达式
CO(g)+H2(g)-Q(Q<0),写出上述反应的平衡常数表达式 A.升温 B.增加水蒸气的浓度 C.减压 D.增加焦炭的量
(5)在一个2L的容器中进行该反应的实验,若混合气体的密度不变,(填“能”或“不能”)
更新时间:2024-01-22 20:38:34
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
【推荐1】2022年12月4日神舟十四号载人飞船成功返回地面,圆满完成飞行任务。载人航天工程对科学研究及太空资源开发具有重要意义。
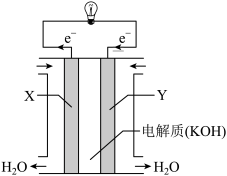
(1)氢氧燃料电池(如图所示)反应生成的水可作为航天员的饮用水,由图示的电子转移方向判断Y气体是___________ ,OH-向___________ (填“正”或“负”)极作定向移动,负极的电极反应式为___________ 。
①镉镍蓄电池的工作原理为:Cd+2NiOOH+2H2O Cd(OH)2+2Ni(OH)2.当飞船运行到地影区时,镉镍蓄电池为飞船供电,此时在正极反应的物质是
Cd(OH)2+2Ni(OH)2.当飞船运行到地影区时,镉镍蓄电池为飞船供电,此时在正极反应的物质是___________ ,负极附近溶液的碱性___________ (填“增强”“减弱”或“不变”)。
②应急电池在紧急状况下会自动启动,工作原理为Zn+A2O+H2O 2Ag+Zn(OH)2,工作时,当消耗32.5gZn时,理论上外电路转移的电子数目为
2Ag+Zn(OH)2,工作时,当消耗32.5gZn时,理论上外电路转移的电子数目为___________ 。
(3)在体积为2L的绝热刚性密闭容器中发生反应: ,
,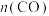 随时间的变化如下表所示:
随时间的变化如下表所示:
①用 表示0~2s内该反应的平均速率v=
表示0~2s内该反应的平均速率v=___________ mol/(L•s)。
②从表格数据可知,该反应速率先加快,再减慢,请说明反应速率加快的原因是___________ 。
③对于该反应,下列说法正确的是___________ 。
A.当混合气体平均摩尔质量不变,说明反应达到平衡
B.当消耗1molCO,同时生成1mol ,说明反应达到平衡
,说明反应达到平衡
C.当温度不变,说明反应达到平衡
D.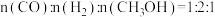 ,说明反应已达平衡
,说明反应已达平衡
(1)氢氧燃料电池(如图所示)反应生成的水可作为航天员的饮用水,由图示的电子转移方向判断Y气体是
①镉镍蓄电池的工作原理为:Cd+2NiOOH+2H2O
 Cd(OH)2+2Ni(OH)2.当飞船运行到地影区时,镉镍蓄电池为飞船供电,此时在正极反应的物质是
Cd(OH)2+2Ni(OH)2.当飞船运行到地影区时,镉镍蓄电池为飞船供电,此时在正极反应的物质是②应急电池在紧急状况下会自动启动,工作原理为Zn+A2O+H2O
 2Ag+Zn(OH)2,工作时,当消耗32.5gZn时,理论上外电路转移的电子数目为
2Ag+Zn(OH)2,工作时,当消耗32.5gZn时,理论上外电路转移的电子数目为(3)在体积为2L的绝热刚性密闭容器中发生反应:
 ,
,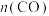 随时间的变化如下表所示:
随时间的变化如下表所示:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
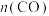 /mol /mol | 0.40 | 0.32 | 0.20 | 0.10 | 0.06 | 0.06 | 0.06 |
 表示0~2s内该反应的平均速率v=
表示0~2s内该反应的平均速率v=②从表格数据可知,该反应速率先加快,再减慢,请说明反应速率加快的原因是
③对于该反应,下列说法正确的是
A.当混合气体平均摩尔质量不变,说明反应达到平衡
B.当消耗1molCO,同时生成1mol
 ,说明反应达到平衡
,说明反应达到平衡C.当温度不变,说明反应达到平衡
D.
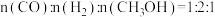 ,说明反应已达平衡
,说明反应已达平衡
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】I.如图所示,800℃时A、B、C三种气体在密闭容器中反应时的浓度变化,分析图像回答问题:
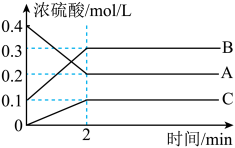
(1)2min内,用C表示的反应速率为______________ 。
(2)该反应的方程式为______________ 。
(3)在其他条件下,测得A的反应速率为0.05 mol/(L·s),此时的反应与800℃时相比,________ 。
A.比800℃ 时快 B.比800℃ 时慢 C.和800℃ 时速率一样
Ⅱ.学习小组甲利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如表实验:
(4)通过实验A、B,可探究出___________ (填外部因素)的改变对化学反应速率的影响,其中V1=_____ 、T1=_____ ;通过实验________ (填实验序号)可探究出温度变化对化学反应速率的影响,其中V2=_______ ,t2_______ 8 (填写“=”、“>”或“<”)。
(5)若t1<8,则由此实验可以得出的结论是_______ 。

(1)2min内,用C表示的反应速率为
(2)该反应的方程式为
(3)在其他条件下,测得A的反应速率为0.05 mol/(L·s),此时的反应与800℃时相比,
A.比800℃ 时快 B.比800℃ 时慢 C.和800℃ 时速率一样
Ⅱ.学习小组甲利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如表实验:
实验序号 | 实验温度/K | 有关物质 | 溶液颜色褪至无色所需时间/s | ||||
酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
| V/mL | c/mol•L-1 | V/mL | c/mol•L-1 | V/mL | |||
A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
(5)若t1<8,则由此实验可以得出的结论是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】Ⅰ.用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
(1)该实验探究的是____ 因素对化学反应速率的影响。如图一,相同时间内针筒中所得的CO2体积大小关系是___ (填实验序号)。
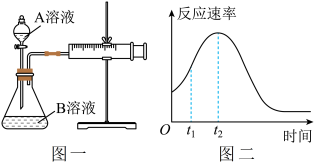
(2)若实验①在2min末收集了2.24mLCO2(标准状况下),则在2min末,c(MnO4-)___ mol·L-1(假设混合液体积为50mL)。
(3)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定___ 来比较化学反应速率。
(4)小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是①产物MnSO4是该反应的催化剂、②_____ 。
Ⅱ.一定温度下,将一定量的N2和H2充入固定体积的密闭容器中进行反应:
N2(g)+3H2(g)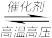 2NH3(g)。
2NH3(g)。
(1)下列描述能说明该可逆反应达到化学平衡状态的有___ 。
A.容器内的压强不变
B.容器内气体的密度不变
C.相同时间内有3mol H-H键断裂,有6mol N-H键形成
D.c(N2):c(H2):c(NH3)=1:3:2
E.NH3的质量分数不再改变
(2)若起始时向容器中充入10mol ·L-1的N2和15mol ·L-1的H2,10min时测得容器内NH3的浓度为1.5mol ·L-1。10min内用N2表示的反应速率为___ ;此时H2的转化率为___ 。
| 实验序号 | A溶液 | B溶液 |
| ① | 20mL 0.1mol·L-1H2C2O4溶液 | 30mL 0.1 mol·L-1KMnO4溶液 |
| ② | 20mL 0.2mol·L-1H2C2O4溶液 | 30mL 0.1mol·L-1KMnO4溶液 |

(2)若实验①在2min末收集了2.24mLCO2(标准状况下),则在2min末,c(MnO4-)
(3)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定
(4)小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是①产物MnSO4是该反应的催化剂、②
Ⅱ.一定温度下,将一定量的N2和H2充入固定体积的密闭容器中进行反应:
N2(g)+3H2(g)
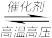 2NH3(g)。
2NH3(g)。(1)下列描述能说明该可逆反应达到化学平衡状态的有
A.容器内的压强不变
B.容器内气体的密度不变
C.相同时间内有3mol H-H键断裂,有6mol N-H键形成
D.c(N2):c(H2):c(NH3)=1:3:2
E.NH3的质量分数不再改变
(2)若起始时向容器中充入10mol ·L-1的N2和15mol ·L-1的H2,10min时测得容器内NH3的浓度为1.5mol ·L-1。10min内用N2表示的反应速率为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视。目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,进行如下实验:在容积为1L的密闭容器中,充入1molCO2和3molH2。在500℃下发生发应,CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。实验测得CO2和CH3OH(g)的物质的量(n)随时间变化如图1所示:

(1)500℃该反应的平衡常数为_____ (结果保留一位小数),
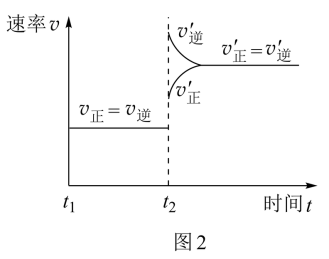
(2)图2是改变温度时化学反应速率随时间变化的示意图,若提高温度到800℃进行,达平衡时,K值_____ (填“增大”“减小”或“不变”)。
(3)下列措施中不能使CO2的转化率增大的是_______ 。
A.在原容器中再充入1molH2 B.在原容器中再充入1molCO2
C.缩小容器的容积 D.使用更有效的催化剂 E将水蒸气从体系中分离出
(4)500℃条件下,测得某时刻,CO2(g)、H2(g)、CH3OH(g)和H2O(g)的浓度均为0.5mol/L,则此时v(正)____ v(逆)(填“>”“<”或“=”)。

(1)500℃该反应的平衡常数为
(2)图2是改变温度时化学反应速率随时间变化的示意图,若提高温度到800℃进行,达平衡时,K值

(3)下列措施中不能使CO2的转化率增大的是
A.在原容器中再充入1molH2 B.在原容器中再充入1molCO2
C.缩小容器的容积 D.使用更有效的催化剂 E将水蒸气从体系中分离出
(4)500℃条件下,测得某时刻,CO2(g)、H2(g)、CH3OH(g)和H2O(g)的浓度均为0.5mol/L,则此时v(正)
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】亚硝酰氯(NOCl)是有机合成试剂,实验室中可用反应(I)进行合成:
 。
。
(1)在常温下,常用高锰酸钾和浓盐酸反应制备氯气,反应的离子方程式为___________ 。
(2)已知几种物质的相对能量如下:
根据表格中数据估算上述反应(I)的反应热
___________  。
。
(3) ,可逆反应
,可逆反应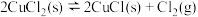 用气体物质的分压表示的平衡常数
用气体物质的分压表示的平衡常数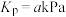 。(提示:分压=总压
。(提示:分压=总压 该物质的物质的量分数)
该物质的物质的量分数) 下,在某真空容器中加入足量的
下,在某真空容器中加入足量的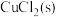 并充入
并充入 ,测得起始压强为
,测得起始压强为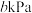 ,发生上述反应(I)达到平衡时测得
,发生上述反应(I)达到平衡时测得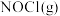 的压强为
的压强为 。平衡时
。平衡时 的转化率为
的转化率为___________ ;该温度下,反应(I)的平衡常数
___________  。
。
(4) 的速率方程可表示为:
的速率方程可表示为: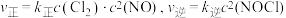 ,其中
,其中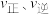 表示正、逆反应速率,k正、k逆表示正、逆反应的速率常数,只与温度、催化剂、接触面有关,与浓度无关。
表示正、逆反应速率,k正、k逆表示正、逆反应的速率常数,只与温度、催化剂、接触面有关,与浓度无关。
①上述反应(I)的平衡常数
___________ (用k正、k逆表示)。
②加入催化剂,k正增大的倍数___________ (填“大于”“小于”或“等于”)k逆增大的倍数。
③已知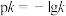 ,当温度降低时,如图所示中的2条直线代表
,当温度降低时,如图所示中的2条直线代表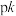 与
与 关系,其中代表pk正与
关系,其中代表pk正与 关系的是直线
关系的是直线___________ (填字母)。判断理由是___________ 。

 。
。(1)在常温下,常用高锰酸钾和浓盐酸反应制备氯气,反应的离子方程式为
(2)已知几种物质的相对能量如下:
| 物质 | Cl2 | NO(g) | NOCl(g) |
| 相对能量/kJ·mol—1 | 0 | 90.25 | 51.71 |

 。
。(3)
 ,可逆反应
,可逆反应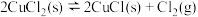 用气体物质的分压表示的平衡常数
用气体物质的分压表示的平衡常数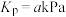 。(提示:分压=总压
。(提示:分压=总压 该物质的物质的量分数)
该物质的物质的量分数) 下,在某真空容器中加入足量的
下,在某真空容器中加入足量的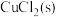 并充入
并充入 ,测得起始压强为
,测得起始压强为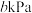 ,发生上述反应(I)达到平衡时测得
,发生上述反应(I)达到平衡时测得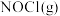 的压强为
的压强为 。平衡时
。平衡时 的转化率为
的转化率为
 。
。(4)
 的速率方程可表示为:
的速率方程可表示为: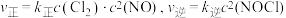 ,其中
,其中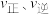 表示正、逆反应速率,k正、k逆表示正、逆反应的速率常数,只与温度、催化剂、接触面有关,与浓度无关。
表示正、逆反应速率,k正、k逆表示正、逆反应的速率常数,只与温度、催化剂、接触面有关,与浓度无关。①上述反应(I)的平衡常数

②加入催化剂,k正增大的倍数
③已知
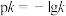 ,当温度降低时,如图所示中的2条直线代表
,当温度降低时,如图所示中的2条直线代表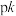 与
与 关系,其中代表pk正与
关系,其中代表pk正与 关系的是直线
关系的是直线
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】火山爆发时会喷出SO2,SO2是大气主要污染物之一,在工业中可用于制备硫酸。回答下列问题:
(1)SO2是_____ (填“电解质”或“非电解质”)。
(2)Cu2S与O2反应可生成SO2,已知:
Cu(s)+ O2(g)=CuO(s) △H=x kJ∙mol-1
O2(g)=CuO(s) △H=x kJ∙mol-1
Cu(s)+ S(s)=
S(s)= Cu2S(s) △H=y kJ∙mol-1
Cu2S(s) △H=y kJ∙mol-1
S(s)+O2(g)=SO2(g) △H=z kJ∙mol-1
写出Cu2S与O2反应生成CuO和SO2的热化学方程式__________________________ 。
(3)硫酸工业中涉及反应:2SO2(g)+O2(g)⇌2SO3(g)△H=Q kJ·mol-1。一定条件下,在2L恒容密闭容器中,通入2molSO2和1molO2发生上述反应,SO2的平衡转化率与压强、温度的关系如图所示。a点时此反应的平衡常数的数值为_____ 。
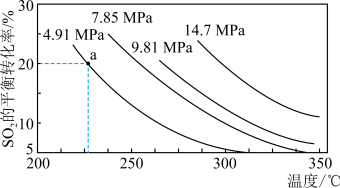
关于该反应,下列说法正确的是____ 。
A.容器内混合气体的密度不再变化时,反应达到平衡
B.相同时间内生成2molSO2同时消耗1molO2,反应达到平衡
C.Q大于0
D.相同温度下,压强越大,SO2的平衡转化率就越大,该反应的平衡常数就越大
E.反应达到平衡后保持温度不变,再充入2molSO2和1molO2,SO2的平衡转化率增大
F.反应达到平衡后保持温度不变,再充入He(g),SO2的平衡转化率增大
(4)将SO2通入酸化的硝酸钡溶液可生成硫酸钡沉淀,25℃时,KSP(BaSO4)=1×10-10。KSP(BaCO3)=2.6×10-9。该温度下,BaSO4和BaCO3沉淀共存的悬浊液中, =
=___ 。
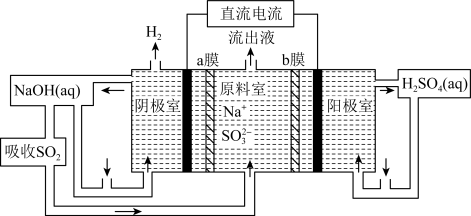
(5)用如图装置回收SO2可制得硫酸,电极为惰性电极,a、b膜分别为阳离子交换膜、阴离子交换膜。阳极的电极反应为____ 。
(1)SO2是
(2)Cu2S与O2反应可生成SO2,已知:
Cu(s)+
 O2(g)=CuO(s) △H=x kJ∙mol-1
O2(g)=CuO(s) △H=x kJ∙mol-1Cu(s)+
 S(s)=
S(s)= Cu2S(s) △H=y kJ∙mol-1
Cu2S(s) △H=y kJ∙mol-1S(s)+O2(g)=SO2(g) △H=z kJ∙mol-1
写出Cu2S与O2反应生成CuO和SO2的热化学方程式
(3)硫酸工业中涉及反应:2SO2(g)+O2(g)⇌2SO3(g)△H=Q kJ·mol-1。一定条件下,在2L恒容密闭容器中,通入2molSO2和1molO2发生上述反应,SO2的平衡转化率与压强、温度的关系如图所示。a点时此反应的平衡常数的数值为

关于该反应,下列说法正确的是
A.容器内混合气体的密度不再变化时,反应达到平衡
B.相同时间内生成2molSO2同时消耗1molO2,反应达到平衡
C.Q大于0
D.相同温度下,压强越大,SO2的平衡转化率就越大,该反应的平衡常数就越大
E.反应达到平衡后保持温度不变,再充入2molSO2和1molO2,SO2的平衡转化率增大
F.反应达到平衡后保持温度不变,再充入He(g),SO2的平衡转化率增大
(4)将SO2通入酸化的硝酸钡溶液可生成硫酸钡沉淀,25℃时,KSP(BaSO4)=1×10-10。KSP(BaCO3)=2.6×10-9。该温度下,BaSO4和BaCO3沉淀共存的悬浊液中,
 =
=(5)用如图装置回收SO2可制得硫酸,电极为惰性电极,a、b膜分别为阳离子交换膜、阴离子交换膜。阳极的电极反应为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】2022年北京冬奥会实现了100%的绿电供应,充分利用了电动汽车和氢燃料汽车等先进技术,基本实现了碳中和,下面是几种储氢材料,回答下面问题:
(1) 是一种白色粉末,与水发生反应:
是一种白色粉末,与水发生反应: ↑。
↑。
①上述反应中含有离子键的化合物是___________ (填化学式)。
②写出基态 原子最高能层符号
原子最高能层符号___________ ,最高能级符号___________ 。基态O原子最高能级含有___________ 个电子。
(2) 和
和 也是很好的储氢材料。
也是很好的储氢材料。
①基态 原子核外电子的空间运动状态(原子轨道)有
原子核外电子的空间运动状态(原子轨道)有___________ 种。
②基态 原子的电子排布式
原子的电子排布式___________ ,基态 原子的价层电子排布式
原子的价层电子排布式___________ , 和
和 都处于元素周期表的
都处于元素周期表的___________ 区。
(3)金属氨络合物储氢材料 和
和 是研究的热点。
是研究的热点。
①基态S原子最高能级上最多有___________ 个电子顺时针旋转。
②氮元素与氧元素的第一电离能较高的是___________ (填元素符号)。
③Cl-和S2-的还原性比较,还原性较强的是___________ (填离子符号)。
(1)
 是一种白色粉末,与水发生反应:
是一种白色粉末,与水发生反应: ↑。
↑。①上述反应中含有离子键的化合物是
②写出基态
 原子最高能层符号
原子最高能层符号(2)
 和
和 也是很好的储氢材料。
也是很好的储氢材料。①基态
 原子核外电子的空间运动状态(原子轨道)有
原子核外电子的空间运动状态(原子轨道)有②基态
 原子的电子排布式
原子的电子排布式 原子的价层电子排布式
原子的价层电子排布式 和
和 都处于元素周期表的
都处于元素周期表的(3)金属氨络合物储氢材料
 和
和 是研究的热点。
是研究的热点。①基态S原子最高能级上最多有
②氮元素与氧元素的第一电离能较高的是
③Cl-和S2-的还原性比较,还原性较强的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】A、B、C、D是四种短周期元素,E是过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图为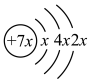 ,B是同周期除稀有气体外半径最大的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期除稀有气体外半径最大的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
(1)A为____ (写出元素符号,下同);
(2)B为____ ,简化电子排布式是____ ;
(3)C为____ ,外围电子排布式是____ ;
(4)D为____ ,轨道表示式是____ ;
(5)E原子结构示意图是____ 。
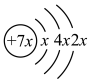 ,B是同周期除稀有气体外半径最大的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期除稀有气体外半径最大的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:(1)A为
(2)B为
(3)C为
(4)D为
(5)E原子结构示意图是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】金属和非金属分界线附近的元素(如Ga、Ge、As),可用于制造半导体材料,是科学研究的热点。试回答下列问题。
(1)锗(Ge)是一种重要的半导体材料,写出基态Ge原子的价层电子排布式:___________ 。
(2)利用离子液体[EMIM][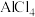 ]可电沉积还原金属Ge.
]可电沉积还原金属Ge. 结构如图所示。
结构如图所示。
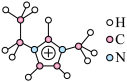
① 中各元素的电负性从小到大的顺序是:
中各元素的电负性从小到大的顺序是:___________ (用元素符号表示)。
② 的空间结构为
的空间结构为___________ 。
(3)镓(Ga)位于元素周期表中第4周期第ⅢA族,其卤化物的熔点如下表:
 的熔点比
的熔点比 的高很多的原因是
的高很多的原因是___________ 。
(4)GaAs是一种人工合成的新型半导体材料,其晶体结构与金刚石相似,如图所示,若该立方晶胞参数为a nm。
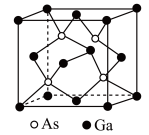
①晶体中与As原子距离最近且相等的Ga原子个数为___________ 。
②已知阿伏加德罗常数的值为 ,GaAs的式量为
,GaAs的式量为 ,则GaAs晶体的密度为
,则GaAs晶体的密度为___________ g·cm (列计算式)。
(列计算式)。
(1)锗(Ge)是一种重要的半导体材料,写出基态Ge原子的价层电子排布式:
(2)利用离子液体[EMIM][
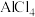 ]可电沉积还原金属Ge.
]可电沉积还原金属Ge. 结构如图所示。
结构如图所示。
①
 中各元素的电负性从小到大的顺序是:
中各元素的电负性从小到大的顺序是:②
 的空间结构为
的空间结构为(3)镓(Ga)位于元素周期表中第4周期第ⅢA族,其卤化物的熔点如下表:
 |  | 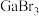 | |
| 熔点/℃ | 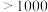 | 77.75 | 122.3 |
 的熔点比
的熔点比 的高很多的原因是
的高很多的原因是(4)GaAs是一种人工合成的新型半导体材料,其晶体结构与金刚石相似,如图所示,若该立方晶胞参数为a nm。

①晶体中与As原子距离最近且相等的Ga原子个数为
②已知阿伏加德罗常数的值为
 ,GaAs的式量为
,GaAs的式量为 ,则GaAs晶体的密度为
,则GaAs晶体的密度为 (列计算式)。
(列计算式)。
您最近一年使用:0次
【推荐1】四种元素A、B、C、D,其中A元素原子的原子核内只有一个质子;B的基态原子s能级的总电子数比p能级的总电子数多1;C元素的原子最外层电子数是次外层的3倍;D是形成化合物种类最多的元素。
(1)A、D形成的某种化合物甲是一种重要的化工产品,可用作水果和蔬菜的催熟剂,甲分子中σ键和π键数目之比为____ ;写出由甲制高聚物的反应方程式____ 。
(2)A、C形成的某种化合物乙分子中含非极性共价键,乙分子属于____ (“极性分子”或“非极性分子”);其电子式____ ;将乙加入浅绿色酸性溶液中,溶液变为棕黄色,写出该反应的离子方程式____ 。
(3)写出B的基态原子电子排布图为____ ;与PH3相比,BA3易液化的主要原因是_____ 。
(4)笑气(B2C)是一种麻醉剂,有关理论认为B2C与DC2分子具有相似的结构;故B2C的空间构型是____ ;DC2分子为____ (填“极性”或“非极性”)分子。
(1)A、D形成的某种化合物甲是一种重要的化工产品,可用作水果和蔬菜的催熟剂,甲分子中σ键和π键数目之比为
(2)A、C形成的某种化合物乙分子中含非极性共价键,乙分子属于
(3)写出B的基态原子电子排布图为
(4)笑气(B2C)是一种麻醉剂,有关理论认为B2C与DC2分子具有相似的结构;故B2C的空间构型是
您最近一年使用:0次
【推荐2】某电镀铜厂有两种废水,分别含有CN-和Cr2O72-等有毒离子,拟用NaClO和Na2S2O3按照下列流程进行处理。

请完成下列填空:
(1)HCN有剧毒,电子式是__ ,其分子属于__ (填“极性”、“非极性”)分子。
(2)表示原子结构的化学用语有:原子结构示意图、核外电子排布式、轨道表示式。从中选择最详尽描述核外电子运动状态的方式,来表示氧原子的最外层电子的运动状态:__ ,其中最外层有__ 种不同能量的电子。
(3)下列事实能说明氯与硫两元素非金属性相对强弱的是___ 。
a.相同条件下水溶液的pH:NaClO>Na2S2O3
b.还原性:H2S>HCl
c.相同条件下水溶液的酸性:HClO3>H2SO3
d.稳定性:HCl>H2S
(4)写出流程③的离子方程式为:___ 。
(5)反应③中,每消耗0.5molCr2O72-转移的电子数为___ ;
(6)取少量待测水样于试管中,加入NaOH溶液观察到有蓝色沉淀生成,继续加至不再产生蓝色沉淀为止,再向溶液中加入足量Na2S溶液,蓝色沉淀转化成黑色沉淀,解释产生该现象的原因___ 。

请完成下列填空:
(1)HCN有剧毒,电子式是
(2)表示原子结构的化学用语有:原子结构示意图、核外电子排布式、轨道表示式。从中选择最详尽描述核外电子运动状态的方式,来表示氧原子的最外层电子的运动状态:
(3)下列事实能说明氯与硫两元素非金属性相对强弱的是
a.相同条件下水溶液的pH:NaClO>Na2S2O3
b.还原性:H2S>HCl
c.相同条件下水溶液的酸性:HClO3>H2SO3
d.稳定性:HCl>H2S
(4)写出流程③的离子方程式为:
(5)反应③中,每消耗0.5molCr2O72-转移的电子数为
(6)取少量待测水样于试管中,加入NaOH溶液观察到有蓝色沉淀生成,继续加至不再产生蓝色沉淀为止,再向溶液中加入足量Na2S溶液,蓝色沉淀转化成黑色沉淀,解释产生该现象的原因
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】A、B、C、D、E、F均为前四周期的元素,原子序数依次增大,A的核外电子数等于其电子层数,B的最外层电子数是次外层电子数的3倍,A和C、B和E同主族,B、C、D的离子具有相同的电子层结构,D的离子是同周期中离子半径最小的,F原子中共有6个未成对电子。
请回答下列问题:
(1)写出下列元素的元素符号:A____ 、C_____ 、E_____ 、F_____ 。
(2)元素A和元素B可以形成A2B物质甲,写出甲的分子式____ ,甲为_____ (填“极性”或“非极性”)分子。
(3)元素A和元素E形成化合物乙,用电子式表示化合物乙_______________ ;常温下甲为液态,乙为气态,试解释原因__________________________ 。
(4)元素A与元素C形成化合物丙,丙的水溶液显碱性,试用化学方程式解释其原因:_________________ 。
(5)元素C、元素D的最高价氧化物的水化物相互反应的离子方程式是__________ 。
(6)写出元素F的外围电子排布式_______________________ 。
请回答下列问题:
(1)写出下列元素的元素符号:A
(2)元素A和元素B可以形成A2B物质甲,写出甲的分子式
(3)元素A和元素E形成化合物乙,用电子式表示化合物乙
(4)元素A与元素C形成化合物丙,丙的水溶液显碱性,试用化学方程式解释其原因:
(5)元素C、元素D的最高价氧化物的水化物相互反应的离子方程式是
(6)写出元素F的外围电子排布式
您最近一年使用:0次



