我国力争2060年前实现碳中和,将 转化为甲醇是实现碳中和的途径之一、原理为:
转化为甲醇是实现碳中和的途径之一、原理为: 。在一定温度下,体积为1L的密闭容器中,充入
。在一定温度下,体积为1L的密闭容器中,充入 和
和 ,测得
,测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
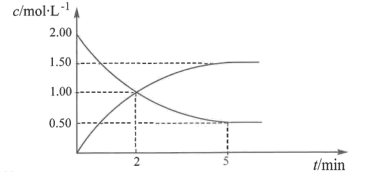
回答下列问题:
(1)2min~5min的平均反应速率
_______ 。
(2)平衡时 的转化率为
的转化率为_______ %。
(3)2min时,
_______  (填“>”“<”“=”或“无法比较”)。
(填“>”“<”“=”或“无法比较”)。
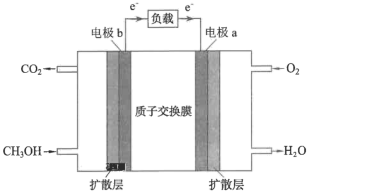
(4)下图为甲醇酸性燃料电池的构造示意图,根据原电池的工作原理,电极a是____ (填“正极”或“负极”),此电池工作时,负极的电极反应为___ 。
 转化为甲醇是实现碳中和的途径之一、原理为:
转化为甲醇是实现碳中和的途径之一、原理为: 。在一定温度下,体积为1L的密闭容器中,充入
。在一定温度下,体积为1L的密闭容器中,充入 和
和 ,测得
,测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
回答下列问题:
(1)2min~5min的平均反应速率

(2)平衡时
 的转化率为
的转化率为(3)2min时,

 (填“>”“<”“=”或“无法比较”)。
(填“>”“<”“=”或“无法比较”)。(4)下图为甲醇酸性燃料电池的构造示意图,根据原电池的工作原理,电极a是

更新时间:2021-07-15 21:34:27
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】化学研究的物质多种多样,按要求回答下列问题:
(1)过二硫酸钠( )可以看成过氧化氢的衍生物,
)可以看成过氧化氢的衍生物, 分子中的两个H原子被磺酸基(
分子中的两个H原子被磺酸基(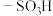 )取代后即为过二硫酸。
)取代后即为过二硫酸。
① 中硫元素的化合价为
中硫元素的化合价为_______ 。
②用 溶液可以检测废水中的
溶液可以检测废水中的 ,含有
,含有 的废水加入
的废水加入 溶液后会变为紫红色,
溶液后会变为紫红色, 被还原为稳定的
被还原为稳定的 。发生上述反应的氧化剂与还原剂的物质的量之比为
。发生上述反应的氧化剂与还原剂的物质的量之比为_______ 。
(2)硫代硫酸钠( )又名大苏打,造纸工业用作纸浆漂白后的除氯剂。
)又名大苏打,造纸工业用作纸浆漂白后的除氯剂。
① 在中性与碱性溶液中很稳定,遇酸则迅速反应。
在中性与碱性溶液中很稳定,遇酸则迅速反应。 溶液中加入稀硫酸时反应的离子方程式为
溶液中加入稀硫酸时反应的离子方程式为_______ 。
② 常用于防毒面具中吸收
常用于防毒面具中吸收 。若1 mol
。若1 mol  完全反应,失去8 mol电子,则其水溶液吸收
完全反应,失去8 mol电子,则其水溶液吸收 的离子方程式为
的离子方程式为_______ 。
(3)在室温下,化学反应 的反应物初始浓度、溶液中的
的反应物初始浓度、溶液中的 初始浓度及初始速率间的关系如下表所示。
初始浓度及初始速率间的关系如下表所示。
已知表中初始反应速率与有关离子浓度关系可以表示为: (温度一定时,k为常数)
(温度一定时,k为常数)
(1)计算b、c的值:b=_______ ,c=_______ 。
(2)若实验编号4的其他浓度不变,仅将溶液的酸碱值变更为 ,反应的初始速率v=
,反应的初始速率v=_______ mol⋅L ⋅s
⋅s 。
。
(1)过二硫酸钠(
 )可以看成过氧化氢的衍生物,
)可以看成过氧化氢的衍生物, 分子中的两个H原子被磺酸基(
分子中的两个H原子被磺酸基(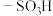 )取代后即为过二硫酸。
)取代后即为过二硫酸。①
 中硫元素的化合价为
中硫元素的化合价为②用
 溶液可以检测废水中的
溶液可以检测废水中的 ,含有
,含有 的废水加入
的废水加入 溶液后会变为紫红色,
溶液后会变为紫红色, 被还原为稳定的
被还原为稳定的 。发生上述反应的氧化剂与还原剂的物质的量之比为
。发生上述反应的氧化剂与还原剂的物质的量之比为(2)硫代硫酸钠(
 )又名大苏打,造纸工业用作纸浆漂白后的除氯剂。
)又名大苏打,造纸工业用作纸浆漂白后的除氯剂。①
 在中性与碱性溶液中很稳定,遇酸则迅速反应。
在中性与碱性溶液中很稳定,遇酸则迅速反应。 溶液中加入稀硫酸时反应的离子方程式为
溶液中加入稀硫酸时反应的离子方程式为②
 常用于防毒面具中吸收
常用于防毒面具中吸收 。若1 mol
。若1 mol  完全反应,失去8 mol电子,则其水溶液吸收
完全反应,失去8 mol电子,则其水溶液吸收 的离子方程式为
的离子方程式为(3)在室温下,化学反应
 的反应物初始浓度、溶液中的
的反应物初始浓度、溶液中的 初始浓度及初始速率间的关系如下表所示。
初始浓度及初始速率间的关系如下表所示。| 实验编号 |  的初始浓度(mol⋅L 的初始浓度(mol⋅L ) ) |  的初始浓度(mol⋅L 的初始浓度(mol⋅L ) ) |  的初始浓度(mol⋅L 的初始浓度(mol⋅L ) ) | 初始速率ν(mol⋅L ⋅s ⋅s ) ) |
| 1 |  |  | 1.00 |  |
| 2 | a |  | 1.00 |  |
| 3 |  | 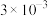 | 2.00 |  |
| 4 | 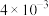 | 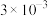 | 1.00 | 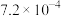 |
已知表中初始反应速率与有关离子浓度关系可以表示为:
 (温度一定时,k为常数)
(温度一定时,k为常数)(1)计算b、c的值:b=
(2)若实验编号4的其他浓度不变,仅将溶液的酸碱值变更为
 ,反应的初始速率v=
,反应的初始速率v= ⋅s
⋅s 。
。
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】I.一定条件下,将2molA气体和2molB气体加入2L的恒容密闭容器中进行反应: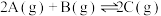 。2min后达化学平衡,测得C的浓度为
。2min后达化学平衡,测得C的浓度为 ,填写下列空白:
,填写下列空白:
(1)2min内用A表示的平均反应速率为_______ 。
(2)平衡时B的物质的量浓度为_______ 。
(3)平衡时A的转化率是B的转化率的_______ 倍。
(4)能说明该反应达到化学平衡状态的是:_______ 。
(5)要使该反应的化学反应速率加快,可采取的措施是:_______ (任写两种)。
II.理论上,任何自发的氧化还原反应都可以设计成原电池。利用反应 设计一种化学电池,回答下列问题:
设计一种化学电池,回答下列问题:
(6)正极上发生的电极反应式为_______ 。
(7)若导线上转移的电子为1mol,则消耗金属铜的质量为_______ 。
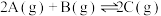 。2min后达化学平衡,测得C的浓度为
。2min后达化学平衡,测得C的浓度为 ,填写下列空白:
,填写下列空白:(1)2min内用A表示的平均反应速率为
(2)平衡时B的物质的量浓度为
(3)平衡时A的转化率是B的转化率的
(4)能说明该反应达到化学平衡状态的是:
| A.A表示的平均反应速率等于C表示的平均反应速率 |
| B.消耗1molA的同时生成0.5molB |
| C.分别用A、B、C表示的反应速率之比为2∶1∶2 |
| D.C的物质的量不再变化 |
II.理论上,任何自发的氧化还原反应都可以设计成原电池。利用反应
 设计一种化学电池,回答下列问题:
设计一种化学电池,回答下列问题:(6)正极上发生的电极反应式为
(7)若导线上转移的电子为1mol,则消耗金属铜的质量为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某酸性工业废水中含有K2Cr2O7。光照下,草酸(H2C2O4)能将其中的Cr2O 转化为Cr3+,草酸被氧化成CO2,某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
转化为Cr3+,草酸被氧化成CO2,某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
在25℃下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,做对比实验,实验设计表如下:
测得实验①和②溶液中的Cr2O 浓度随时间变化关系如图所示。
浓度随时间变化关系如图所示。

(1)在K2Cr2O7稀溶液中存在平衡:___ (用离子方程式表示),其平衡常数表达式K=___ 。
(2)实验设计表中a=__ 。
(3)上述实验中参加反应的Cr2O 与草酸的物质的量之比为
与草酸的物质的量之比为__ ,该反应的离子方程式为:____ 。
(4)实验①和②的结果表明___ ;实验①中0~t1时间段反应速率v(Cr3+)=___ mol/(L·min)(用代数式表示)。
 转化为Cr3+,草酸被氧化成CO2,某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
转化为Cr3+,草酸被氧化成CO2,某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:在25℃下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,做对比实验,实验设计表如下:
| 实验编号 | 初始pH | 废水样品体积/mL | 草酸溶液体积/mL | 蒸馏水体积/mL |
| ① | 4 | 60 | 10 | 30 |
| ② | 5 | 60 | 10 | 30 |
| ③ | 5 | 60 | a | 20 |
 浓度随时间变化关系如图所示。
浓度随时间变化关系如图所示。
(1)在K2Cr2O7稀溶液中存在平衡:
(2)实验设计表中a=
(3)上述实验中参加反应的Cr2O
 与草酸的物质的量之比为
与草酸的物质的量之比为(4)实验①和②的结果表明
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某课外兴趣小组对H2O2的分解速率做了如下实验探究.
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据。表中数据为在不同条件下用10mL H2O2制取15OmLO2所需的时间(秒)。
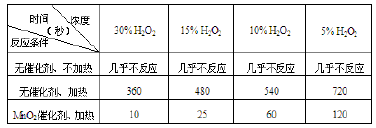
① 上述实验结果体现了______ 、_____ 、_____ 等因素对过氧化氢分解速率的影响;
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对化学反应速率的影响___________________________ 。
(2)某温度时,在一个2L的密闭容器中,M、N、W三种气体的物质的量随时间的变化曲线如图所示。根据图中数据.试填写下列空白:
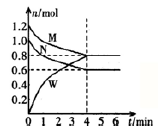
① 该反应的化学方程式为______________ 。
② 从开始至4min,N的平均反应速率为___________ ;4min 末M的转化率为___________
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据。表中数据为在不同条件下用10mL H2O2制取15OmLO2所需的时间(秒)。

① 上述实验结果体现了
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对化学反应速率的影响
(2)某温度时,在一个2L的密闭容器中,M、N、W三种气体的物质的量随时间的变化曲线如图所示。根据图中数据.试填写下列空白:

① 该反应的化学方程式为
② 从开始至4min,N的平均反应速率为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】已知A(g)+B(g)  C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
回答下列问题:
(1)该反应的平衡常数表达式K=____________ ,ΔH__ 0(填“<”“ >”或“ =”)。
(2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1,则6s时C的物质的量为_____ ;则反应达到平衡时,A的转化率为____ ,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为_____ (填“增大”“减少”或“不变”)。
(3)1200℃时反应C(g)+D(g) A(g)+B(g)的平衡常数的值为
A(g)+B(g)的平衡常数的值为_______ 。
 C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下: | 温度/ ℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)该反应的平衡常数表达式K=
(2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1,则6s时C的物质的量为
(3)1200℃时反应C(g)+D(g)
 A(g)+B(g)的平衡常数的值为
A(g)+B(g)的平衡常数的值为
您最近一年使用:0次
【推荐3】天然气的主要成分甲烷,有着广泛的用途,试回答下列问题:
(1) CH4与CO2在高温下发生反应:CH4(g)+CO2(g) ⇌2CO(g)+2H2(g)
①在600K时,将0.10 mol CH4与0.40 mol CO2充入2.5 L的空钢瓶中,反应平衡后氢气的体积分数为20%,则CH4的平衡转化率α1=___________ ,反应的平衡常数K=___________ (保留小数点后3位)。
②在700K重复实验,反应平衡后氢气的体积分数为25%,CH4的转化率α2___________ α1 (填“>”、“<”或“=” ,下同) ,该反应的∆H___________ 0。
(2) 分析“甲烷-空气”燃料电池在碱性电解液中的工作原理,负极反应式为___________ 。

(1) CH4与CO2在高温下发生反应:CH4(g)+CO2(g) ⇌2CO(g)+2H2(g)
①在600K时,将0.10 mol CH4与0.40 mol CO2充入2.5 L的空钢瓶中,反应平衡后氢气的体积分数为20%,则CH4的平衡转化率α1=
②在700K重复实验,反应平衡后氢气的体积分数为25%,CH4的转化率α2
(2) 分析“甲烷-空气”燃料电池在碱性电解液中的工作原理,负极反应式为

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐1】甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)已知在常温常压下反应的热化学方程式:
①CO(g)+2H2(g) CH3OH(g) ΔH1=-90 kJ·mol-1
CH3OH(g) ΔH1=-90 kJ·mol-1
②CO(g)+H2O(g)== CO2(g) +H2(g) ΔH2=-41 kJ·mol-1
写出由二氧化碳、氢气制备甲醇的热化学方程式______________ ;
(2)在一定条件下,某密闭容器中进行上述二氧化碳与氢气制备甲醇的反应,反应过程中部分数据如下表:
①0〜l0min内,用H2O(g)表示的化学反应速率v(H2O)=__ mol/(L·s)
②达到平衡时,该反应的平衡常数K=____ (用分数表示),平衡时H2的转化率是____ 。
③在其它条件不变的情况下,若30min时改变温度为T2℃,此时H2的物质的量为3.2mol,则T1___ T2(填“>”、“<”或“=”),理由是_____ 。在其他条件不变的情况下,若30min时向容器中再充入lmolCO2(g)和lmolH2O (g),则平衡____ 移动(填“正向”、“逆向”或“不”)。
(3)以甲醇为燃料的新型燃料电池,正极通入O2,负极通入甲醇,在酸性溶液中甲醇与氧作用生成水和二氧化碳。
①负极的电极反应式是________________ ;
②若以该燃料电池作为电源,用石墨作电极电解500mL饱和食盐水,当两极共收集到标准状况下的气体1.12L (不考虑气体的溶解)时,所得溶液的pH=____ (假设反应前后溶液体积不变)。
(1)已知在常温常压下反应的热化学方程式:
①CO(g)+2H2(g)
 CH3OH(g) ΔH1=-90 kJ·mol-1
CH3OH(g) ΔH1=-90 kJ·mol-1②CO(g)+H2O(g)== CO2(g) +H2(g) ΔH2=-41 kJ·mol-1
写出由二氧化碳、氢气制备甲醇的热化学方程式
(2)在一定条件下,某密闭容器中进行上述二氧化碳与氢气制备甲醇的反应,反应过程中部分数据如下表:
| 反应条件 | 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) |
| 恒温恒容 (T1℃、2L) | Omin | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 |
①0〜l0min内,用H2O(g)表示的化学反应速率v(H2O)=
②达到平衡时,该反应的平衡常数K=
③在其它条件不变的情况下,若30min时改变温度为T2℃,此时H2的物质的量为3.2mol,则T1
(3)以甲醇为燃料的新型燃料电池,正极通入O2,负极通入甲醇,在酸性溶液中甲醇与氧作用生成水和二氧化碳。
①负极的电极反应式是
②若以该燃料电池作为电源,用石墨作电极电解500mL饱和食盐水,当两极共收集到标准状况下的气体1.12L (不考虑气体的溶解)时,所得溶液的pH=
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】科学家预言,燃料电池将是21世纪获得电能的重要途径。美国已计划将甲醇燃料电池使用于军事项目。某一种甲醇燃料电池是采用铂作为电极催化剂,在氢氧化钾溶液中加入甲醇,同时向另一个电极通入空气。回答下列问题:
(1)电池放电时发生反应的化学方程式为_______ 。
(2)电池的负极反应式为_______ 。
(3)电解液中的OH-向_______ 极运动(填写“正“或“负”),向外电路释放电子的电极为_______ (填写“正极”或“负极”)。
(1)电池放电时发生反应的化学方程式为
(2)电池的负极反应式为
(3)电解液中的OH-向
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】(1)工业上一般以CO和H2为原料在密闭容器中合成甲醇:CO(g)+2H2(g) ===CH3OH(g) ΔH=-90.8 kJ·mol-1。在容积为1 L的恒容容器中,分别研究在230 ℃、250 ℃和270 ℃三种温度下合成甲醇的规律。
如图是上述三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1 mol)与CO平衡转化率的关系,则曲线Z对应的温度是__________ 。



(2)如图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。
Ⅰ.甲中负极的电极反应式为__________________________ 。
Ⅱ.乙中反应的化学方程式为_________________________________ ;A极析出的气体在标准状况下的体积为________ 。
Ⅲ.丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图,则图中②线表示的是________ 的变化;反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要______ mL 5.0 mol·L-1 NaOH溶液。
如图是上述三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1 mol)与CO平衡转化率的关系,则曲线Z对应的温度是



(2)如图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。
Ⅰ.甲中负极的电极反应式为
Ⅱ.乙中反应的化学方程式为
Ⅲ.丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图,则图中②线表示的是
您最近一年使用:0次



