根据下列实验操作和现象所得出的结论正确的是

| 选项 | 实验操作和现象 | 结论 |
| A | 向某黄色溶液中加入淀粉KI溶液,溶液呈蓝色 | 溶液中含Br2 |
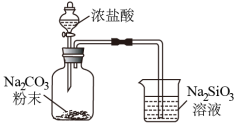
| B | 如图所示,烧杯中看见白色沉淀 | 证明酸性强弱:H2CO3>H2SiO3 |
| C | 向Fe(NO3)2溶液中滴入硫酸酸化的H2O2溶液,溶液变黄 | 氧化性:H2O2>Fe3+ |
| D | 取5mL0.1mol·L-1KI溶液,加入1mL0.1mol·L-1FeCl3溶液,萃取分液后,向水层滴入KSCN溶液,溶液变成血红色 | Fe3+与I-所发生的反应为可逆反应 |
| A.A | B.B | C.C | D.D |
更新时间:2021-08-07 18:01:16
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列有关化学反应的叙述正确的是( )
| A.SO2与Ba(NO3)2反应生成BaSO3 |
| B.NH3在纯O2中燃烧生成NO2 |
| C.过量CO2与氨水反应生成NH4HCO3 |
| D.高温条件下Fe与水蒸气反应生成Fe(OH)3和H2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】K2Cr2O7溶液中存在平衡:Cr2O72-(橙色)+H2O 2CrO42-(黄色)+2H+,用K2Cr2O7溶液进行下列实验:
2CrO42-(黄色)+2H+,用K2Cr2O7溶液进行下列实验:

结合实验,下列说法错误的是( )
 2CrO42-(黄色)+2H+,用K2Cr2O7溶液进行下列实验:
2CrO42-(黄色)+2H+,用K2Cr2O7溶液进行下列实验:
结合实验,下列说法错误的是( )
| A.①中溶液橙色加深,③中溶液变黄 | B.对比②和④可知K2Cr2O7酸性溶液氧化性强 |
| C.②中C2H5OH使Cr2O72-被氧化 | D.若向④中加入70%H2SO4溶液至过量,溶液可变为绿色 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列反应中,不能产生氢气的是
| A.红热的铁与水蒸气 | B.钠与水 |
C.铝和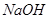 溶液反应 溶液反应 | D.铁与稀硝酸反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法错误的是
A.氯气使KBr溶液变黄, 被还原 被还原 |
B.将铁屑放入稀 中证明Fe比 中证明Fe比 活泼 活泼 |
| C.O、Cl的某些单质或两元素之间形成的某些化合物可作水的消毒剂 |
D. 使溴水褪色与乙烯使 使溴水褪色与乙烯使 溶液褪色的原理相同 溶液褪色的原理相同 |
您最近一年使用:0次
【推荐1】用FeCl3溶液腐蚀覆铜板产生的腐蚀废液可回收利用,实验流程如下。下列有关说法错误的是
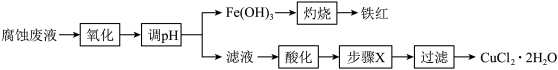

| A.“氧化”步骤中可用的试剂为氯气 |
| B.“调pH”后,检验Fe3+是否沉淀完全的操作为:取少量上层清液于试管中,滴加几滴酸性KMnO4溶液,观察溶液紫色是否褪去 |
| C.进行“灼烧”操作时需用到的仪器有坩埚和酒精灯 |
| D.“步骤X”包含的操作有蒸发浓缩、冷却结晶 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】室温下进行下列实验,根据实验操作、现象和所得到的实验结论均正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 常温下,用pH计测定等物质的量浓度的NaHCO3、NaClO4两种盐溶液的pH,测得NaHCO3的pH大于NaClO4 | 非金属性: Cl>C |
| B | 向含有K+、Na+、 、 、 的溶液中逐滴滴加盐酸,立即产生气泡 的溶液中逐滴滴加盐酸,立即产生气泡 |  和H+反应生成SO2气体 和H+反应生成SO2气体 |
| C | 向某溶液中滴加氯水后再加入KSCN溶液,溶液呈红色 | 溶液中一定含有Fe2+ |
| D | 向2 mL 0.1 mol·L-1 Na2S溶液中滴入2 mL0.1 mol·L-1 ZnSO4溶液,再加入几滴0.1 mol·L-1 CuSO4溶液。开始有白色沉淀生成,后有黑色沉淀生成 | Ksp(CuS)>Ksp(ZnS) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】利用如下实验研究Fe3+与I—的反应。
步骤1:向烧杯中加入10mL0.1mol·L-1的KI溶液,再滴加2mL0.1mol·L-1的Fe2(SO4)3溶液,振荡,把溶液分为四等份于编号为①②③④的四支试管中。
步骤2:向试管①中加入淀粉溶液,观察到溶液变蓝。
步骤3:向试管②中滴加15%KSCN溶液5~6滴,观察到溶液变红。
步骤4:向试管③、试管④中分别加入1mL2.0mol·L-1的FeSO4溶液和1mL的蒸馏水,振荡,观察到试管③中溶液颜色比试管④中溶液颜色浅。
下列说法不正确的是
步骤1:向烧杯中加入10mL0.1mol·L-1的KI溶液,再滴加2mL0.1mol·L-1的Fe2(SO4)3溶液,振荡,把溶液分为四等份于编号为①②③④的四支试管中。
步骤2:向试管①中加入淀粉溶液,观察到溶液变蓝。
步骤3:向试管②中滴加15%KSCN溶液5~6滴,观察到溶液变红。
步骤4:向试管③、试管④中分别加入1mL2.0mol·L-1的FeSO4溶液和1mL的蒸馏水,振荡,观察到试管③中溶液颜色比试管④中溶液颜色浅。
下列说法不正确的是
| A.试管①中的现象说明此条件下Fe3+的氧化性大于I2 |
| B.试管②中的现象说明Fe3+与I—的反应为可逆反应 |
| C.步骤4的现象能说明此条件下I2能将Fe2+氧化成Fe3+ |
| D.试管②中红色物质的组成为[Fe(SCN)n(H2O)6—n]3—n,此微粒中心离子的配位数为n |
您最近一年使用:0次

 中混有的
中混有的 :用澄清石灰水洗气
:用澄清石灰水洗气 固体中混有的
固体中混有的 :加过量盐酸后,过滤、洗涤
:加过量盐酸后,过滤、洗涤 中混有的
中混有的 :加入过量氢氧化钠溶液,过滤、洗涤
:加入过量氢氧化钠溶液,过滤、洗涤 粉中混有的
粉中混有的 :加适量稀硝酸后,过滤、洗涤
:加适量稀硝酸后,过滤、洗涤

