利用硫酸渣(主要含Fe2O3、FeO,杂质为Al2O3和SiO2等)生产铁基颜料铁黄(FeOOH)的制备流程如图:
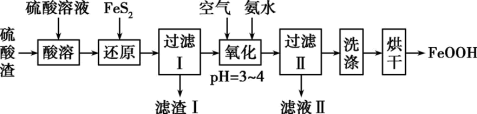
(1)滤渣Ⅰ的主要成分是FeS2、S和_______ (填化学式);Fe3+被FeS2还原的离子方程式为_______ 。
(2)“氧化”中,生成FeOOH的离子方程式为_______ 。

(1)滤渣Ⅰ的主要成分是FeS2、S和
(2)“氧化”中,生成FeOOH的离子方程式为
更新时间:2021-09-23 21:40:57
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】氧化剂和还原剂在生产生活中广泛使用。
(1)KMnO4和HBr溶液可以发生如下反应:2KMnO4+16HBr=2KBr+2MnBr2+8H2O+5Br2
①其中还原剂和氧化剂的物质的量之比为_________
②若消耗0.1mol氧化剂,则被氧化的还原剂的物质的量为_________ ,转移电子数目_______ 。
(2)人体内所含铁元素以Fe2+和Fe3+的形式存在。市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐,此反应的离子方程式为______________ ,但Fe2+在酸性条件下很容易被空气中的O2氧化,写出该反应的离子方程式_________________
(3)次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,可与足量的NaOH完全中和生成NaH2PO2,NaH2PO2溶液可使酚酞试液变红,回答下列问题:
①H3PO2中,磷元素的化合价为______ ②写出H3PO2电离方程式__________________________
③H3PO2及NaH2PO2均可将溶液中的Ag+还原为金属银,从而用于化学镀银。利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4︰1,写出该反应的离子方程式_________
(1)KMnO4和HBr溶液可以发生如下反应:2KMnO4+16HBr=2KBr+2MnBr2+8H2O+5Br2
①其中还原剂和氧化剂的物质的量之比为
②若消耗0.1mol氧化剂,则被氧化的还原剂的物质的量为
(2)人体内所含铁元素以Fe2+和Fe3+的形式存在。市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐,此反应的离子方程式为
(3)次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,可与足量的NaOH完全中和生成NaH2PO2,NaH2PO2溶液可使酚酞试液变红,回答下列问题:
①H3PO2中,磷元素的化合价为
③H3PO2及NaH2PO2均可将溶液中的Ag+还原为金属银,从而用于化学镀银。利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4︰1,写出该反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】Cu2O是一种用途广泛的无机化工原料,一种以氧化铜矿(CuO,含有Fe2O3、Al2O3、SiO2杂质)为原料制备Cu2O的流程如图所示:

已知氨浸过程中仅发生的反应为:CuO+4NH3·H2O= [Cu(NH3)4]2++2OH-+3H2O
回答下列问题:
(1)氨浸之前需将矿物粉碎、过筛,目的是_______________________________ 。
(2)氨浸时的温度一般不超过30℃,主要原因是__________________ 。按此工艺,能否用NaOH溶液代替氨水?__________________ (填“能”或“否”)。
(3)蒸馏过程中会生成一种黑色固体,则此过程中发生反应的化学方程式为____________ 。
(4)电解过程中阳极的电极反应式为_________________ 。
(5)Cu(OH)2也可与NH3·H2O反应,已知常温下:
Cu(OH)2(s)+4NH3·H2O(aq) [Cu(NH3)4]2+(aq)+2OH-(aq)+4H2O(l) K1=4.4×10-7
[Cu(NH3)4]2+(aq)+2OH-(aq)+4H2O(l) K1=4.4×10-7
Cu2+(aq)+4NH3·H2O(aq) [Cu(NH3)4]2+(aq)+4H2O(l) K2=2.0×1013
[Cu(NH3)4]2+(aq)+4H2O(l) K2=2.0×1013
则常温下Ksp[Cu(OH)2]=________________ 。
(6)为了尽量减少流程中所用原料的种类,还原过程可用气体A代替气体B,在加热条件下生成两种单质,该反应的化学方程式为________________________ 。

已知氨浸过程中仅发生的反应为:CuO+4NH3·H2O= [Cu(NH3)4]2++2OH-+3H2O
回答下列问题:
(1)氨浸之前需将矿物粉碎、过筛,目的是
(2)氨浸时的温度一般不超过30℃,主要原因是
(3)蒸馏过程中会生成一种黑色固体,则此过程中发生反应的化学方程式为
(4)电解过程中阳极的电极反应式为
(5)Cu(OH)2也可与NH3·H2O反应,已知常温下:
Cu(OH)2(s)+4NH3·H2O(aq)
 [Cu(NH3)4]2+(aq)+2OH-(aq)+4H2O(l) K1=4.4×10-7
[Cu(NH3)4]2+(aq)+2OH-(aq)+4H2O(l) K1=4.4×10-7Cu2+(aq)+4NH3·H2O(aq)
 [Cu(NH3)4]2+(aq)+4H2O(l) K2=2.0×1013
[Cu(NH3)4]2+(aq)+4H2O(l) K2=2.0×1013则常温下Ksp[Cu(OH)2]=
(6)为了尽量减少流程中所用原料的种类,还原过程可用气体A代替气体B,在加热条件下生成两种单质,该反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】金属A常用于铁的防护。A与氯气反应,生成易挥发的液态物质B,B和过量A反应生成具有还原性的物质C ,C可以还原Fe3+;B和格氏试剂( C6H5MgBr)反应生成D(含元素A碳和氢)。D和B反应得到E,E水解、聚合成链状的F并放出HCl。向B的盐酸溶液中通入H,S,得到金黄色沉淀G(俗名“金粉”), G溶于硫化铵溶液得到 H。向C的盐酸溶液中通入 H2S,得到黑色沉淀I,I可溶于多硫化铵溶液但不溶于硫化铵溶液。写出A~ I的化学式A_____ B______ C______ D______ E______ F_____ G____ H______ I _____ 。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】金属钢主要用于制造低熔合金、轴承合金、半导体、光电源等。铟在自然界以微量伴生于其他金属矿石中,一种以锌精矿焙砂中回收钢的工艺流程如图所示:
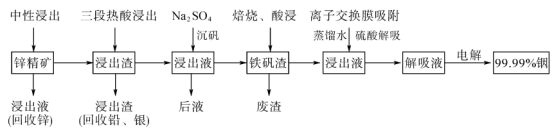
回答下列问题:
(1)提高“中性浸出”步骤浸出速率的措施有___________ (任写两条)。
(2)“三段热酸浸出”时使用的是硫酸,“浸出渣”中含铅物质的化学式为___________ 。
(3)已知:在一定温度、酸度及Na+存在条件下,溶液中的Fe3+可形成黄钠铁矾类矿物NaFe3(SO4)2(OH)6而沉降下来,In3+与Fe3+性质相似,在黄钠铁矾形成过程中,In3+可取代部分Fe3+而形成一种新的难溶于水的化合物M。取0.544g所得干燥纯净的M配,成悬浊液,滴入几滴指示剂,用0.15 H2SO4溶液进行滴定,达到滴定终点时,消耗H2SO4溶液20mL。
H2SO4溶液进行滴定,达到滴定终点时,消耗H2SO4溶液20mL。
①M的化学式为 ,则x=
,则x=___________ 。
②“沉矾”步骤发生反应生成化合物M的离子方程式为___________ 。
(4)离子交换膜吸附过程选用阳离子交换膜,pH<5时,对In3+的吸附率较低,原因是___________ ,pH>5时,会有沉淀出现,原因是___________ 。
(5)电解制铟时,阴极的电极反应式为___________ 。

回答下列问题:
(1)提高“中性浸出”步骤浸出速率的措施有
(2)“三段热酸浸出”时使用的是硫酸,“浸出渣”中含铅物质的化学式为
(3)已知:在一定温度、酸度及Na+存在条件下,溶液中的Fe3+可形成黄钠铁矾类矿物NaFe3(SO4)2(OH)6而沉降下来,In3+与Fe3+性质相似,在黄钠铁矾形成过程中,In3+可取代部分Fe3+而形成一种新的难溶于水的化合物M。取0.544g所得干燥纯净的M配,成悬浊液,滴入几滴指示剂,用0.15
 H2SO4溶液进行滴定,达到滴定终点时,消耗H2SO4溶液20mL。
H2SO4溶液进行滴定,达到滴定终点时,消耗H2SO4溶液20mL。①M的化学式为
 ,则x=
,则x=②“沉矾”步骤发生反应生成化合物M的离子方程式为
(4)离子交换膜吸附过程选用阳离子交换膜,pH<5时,对In3+的吸附率较低,原因是
(5)电解制铟时,阴极的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】某工厂的废金属屑中主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。
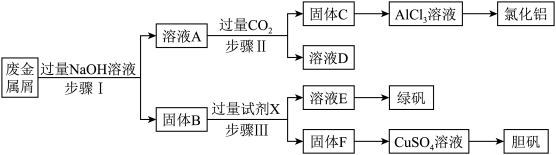
请回答:
(1)步骤Ⅰ、步骤Ⅱ和步骤Ⅲ中需要过滤操作的有___________ 步(填数字)。
(2)写出步骤Ⅰ中Al与NaOH溶液反应的离子方程式___________ 。
(3)步骤Ⅱ试剂X是___________ (填化学式), 固体C是___________ (填化学式)。
(4)溶液E中含有CuSO4,生成该物质的原因是___________ (用离子方程式表示)。
(5)由固体F转化为CuSO4溶液,下列途径最合理可行的是___________ 。
A.固体F与浓硫酸共热
B.固体F与混酸(浓硫酸和硝酸)常温下反应,
C.固体F溶于稀H2SO4和H2O2的混合液中
D.固体F与硫反应后,灼烧,再加水溶解
(6)由CuSO4溶液获得胆矾晶体的操作是___________ 、___________ 、(填操作名称)过滤、洗涤、干燥。

请回答:
(1)步骤Ⅰ、步骤Ⅱ和步骤Ⅲ中需要过滤操作的有
(2)写出步骤Ⅰ中Al与NaOH溶液反应的离子方程式
(3)步骤Ⅱ试剂X是
(4)溶液E中含有CuSO4,生成该物质的原因是
(5)由固体F转化为CuSO4溶液,下列途径最合理可行的是
A.固体F与浓硫酸共热
B.固体F与混酸(浓硫酸和硝酸)常温下反应,
C.固体F溶于稀H2SO4和H2O2的混合液中
D.固体F与硫反应后,灼烧,再加水溶解
(6)由CuSO4溶液获得胆矾晶体的操作是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】铝是一种重要金属,从铝土矿(主要成分为Al2O3、Fe2O3、SiO2等)中冶炼Al的工业生产流程如图:

已知:SiO2是酸性氧化物,不溶于盐酸
(1)步骤Ⅰ、Ⅱ、Ⅲ都要用到的分离方法是_______ 。在实验室模拟该操作,要用到的玻璃仪器有:烧杯、_______ 、_______ 。
(2)溶液A含有的金属阳离子为_______ 。沉淀D的化学式为_______ 。
(3)步骤Ⅲ生成Al(OH)3沉淀的化学方程式为_______ 。
(4)生产过程中,可循环使用的物质有CaO、_______ 、_______ (填化学式)。

已知:SiO2是酸性氧化物,不溶于盐酸
(1)步骤Ⅰ、Ⅱ、Ⅲ都要用到的分离方法是
(2)溶液A含有的金属阳离子为
(3)步骤Ⅲ生成Al(OH)3沉淀的化学方程式为
(4)生产过程中,可循环使用的物质有CaO、
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】重铬酸钾常用作有机合成的氧化剂和催化剂等。由含铬废液(主要含Cr3+、Fe3+、K+、SO42-等)制备K2Cr2O7的流程如下图所示。
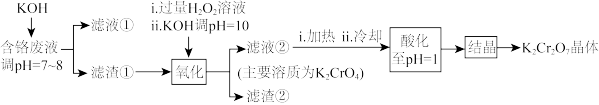
已知:I 在酸性条件下,H2O2能将Cr2O72-还原为Cr3+
II相关金属离子形成氢氧化物沉淀的pH范围如下:
回答下列问题:
(1)滤渣②的主要成分为___________ (填化学式)。
(2)写出“氧化”步骤中反应的化学方程式_______________ 。
(3)“加热”操作的目的是__________________ 。
(4)“酸化”过程中发生反应2CrO42-+2H+ Cr2O72-+H2O (K=4×1014 L3.mol3)已知,“酸化”后溶液中c(Cr2O72-)=1.6×10-3mol/L则溶液中c(CrO42-)=
Cr2O72-+H2O (K=4×1014 L3.mol3)已知,“酸化”后溶液中c(Cr2O72-)=1.6×10-3mol/L则溶液中c(CrO42-)=_________
(5)“结晶”后得到K2Cr2O7(M=294g.mol-1)产品0.5000 g,将其溶解后用稀H2SO4酸化,再用浓度为1.0000 mol.L-1 (NH4)2Fe(SO4)2标准溶液滴定,滴定终点消耗标准溶液的体积为 9.00 mL,则产品的纯度为_____________ 。[滴定反应为:K2Cr2O7+6(NH4)2Fe(SO4)2+7H2SO4 =K2SO4 +Cr2(SO4)3 +6(NH4)2SO4+3Fe2(SO4)3+7H2O]
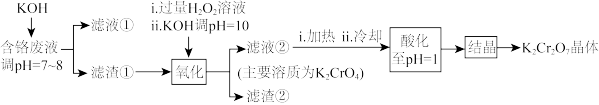
已知:I 在酸性条件下,H2O2能将Cr2O72-还原为Cr3+
II相关金属离子形成氢氧化物沉淀的pH范围如下:
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Cr3+ | 4.9 | 6.8 |
| Fe3+ | 1.5 | 2.8 |
(1)滤渣②的主要成分为
(2)写出“氧化”步骤中反应的化学方程式
(3)“加热”操作的目的是
(4)“酸化”过程中发生反应2CrO42-+2H+
 Cr2O72-+H2O (K=4×1014 L3.mol3)已知,“酸化”后溶液中c(Cr2O72-)=1.6×10-3mol/L则溶液中c(CrO42-)=
Cr2O72-+H2O (K=4×1014 L3.mol3)已知,“酸化”后溶液中c(Cr2O72-)=1.6×10-3mol/L则溶液中c(CrO42-)=(5)“结晶”后得到K2Cr2O7(M=294g.mol-1)产品0.5000 g,将其溶解后用稀H2SO4酸化,再用浓度为1.0000 mol.L-1 (NH4)2Fe(SO4)2标准溶液滴定,滴定终点消耗标准溶液的体积为 9.00 mL,则产品的纯度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
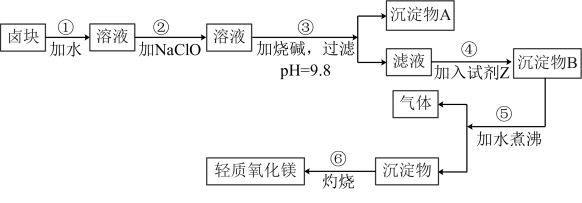
【推荐2】卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子的易溶盐。以卤块为原料可制得轻质氧化镁,工艺流程如图
已知:(1)Fe2+氢氧化物呈絮状,不易从溶液中除去,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。
(2)原料价格表
(3)生成氢氧化物沉淀的PH
回答下列问题:
(1)某课外兴趣小组设计实验证明卤块中含有Fe3+为:取少许样品加水溶解,____ ,则说明卤块中含Fe3+。
(2)工业上冶炼镁常用的方法的化学方程式为____ 。
(3)步骤②加入NaClO而不用H2O2的原因是____ ,步骤②反应后产生少量红褐色沉淀,该反应中氧化剂与还原剂的比例为____ 。
(4)沉淀A的主要成分为____ ;步骤④加入的物质为____ 。
(5)步骤⑤发生的反应的化学方程式为____ 。
(6)步骤⑥如在实验室进行,应选用在____ (填仪器名称)中灼烧。

已知:(1)Fe2+氢氧化物呈絮状,不易从溶液中除去,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。
(2)原料价格表
| 物质 | 价格/(元·吨-1) |
| 漂液(含25.2%NaClO) | 450 |
| 双氧水(含30%H2O2) | 2400 |
| 烧碱(含98%NaOH) | 2100 |
| 纯碱(含99.5%Na2CO3) | 600 |
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
(1)某课外兴趣小组设计实验证明卤块中含有Fe3+为:取少许样品加水溶解,
(2)工业上冶炼镁常用的方法的化学方程式为
(3)步骤②加入NaClO而不用H2O2的原因是
(4)沉淀A的主要成分为
(5)步骤⑤发生的反应的化学方程式为
(6)步骤⑥如在实验室进行,应选用在
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】侯德榜为我国的制碱工业发展做出卓越贡献,其制碱的工艺流程如图所示:
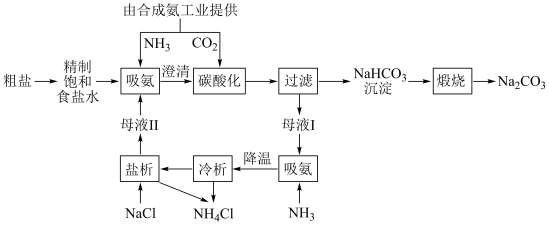
回答下列问题:
(1)粗盐中主要含有 NaCl 和泥沙、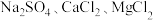 杂质,现对其进行除杂并制备精制饱和食盐水。
杂质,现对其进行除杂并制备精制饱和食盐水。
①通过粗盐制备精制饱和食盐水的第一步操作名称为____________ 。
②除去泥沙后,通过加入化学试剂除可溶性杂质,应选用___________ (填序号)除去 杂质。
杂质。
a. BaCl₂ 溶液 b. 溶液 c. NaOH 溶液
溶液 c. NaOH 溶液
写出除去 杂质时发生反应的离子方程式:
杂质时发生反应的离子方程式:___________ 。
(2)“碳酸化”过程发生反应的化学方程式为___________ 。
(3)“煅烧”时,发生反应的化学方程式为___________ 。
(4)实验室中进行“过滤”操作时,使用的玻璃仪器除烧杯、玻璃棒外,还有___________ 。
(5)“母液 I”中含有大量的Cl-,检验其存在的操作方法为___________ 。
(6)根据流程分析,“降温”和“盐析”的目的均为___________ 。
(7)根据流程分析,该工艺中可循环利用的物质为___________ (写出一种即可)。

回答下列问题:
(1)粗盐中主要含有 NaCl 和泥沙、
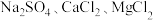 杂质,现对其进行除杂并制备精制饱和食盐水。
杂质,现对其进行除杂并制备精制饱和食盐水。①通过粗盐制备精制饱和食盐水的第一步操作名称为
②除去泥沙后,通过加入化学试剂除可溶性杂质,应选用
 杂质。
杂质。a. BaCl₂ 溶液 b.
 溶液 c. NaOH 溶液
溶液 c. NaOH 溶液写出除去
 杂质时发生反应的离子方程式:
杂质时发生反应的离子方程式:(2)“碳酸化”过程发生反应的化学方程式为
(3)“煅烧”时,发生反应的化学方程式为
(4)实验室中进行“过滤”操作时,使用的玻璃仪器除烧杯、玻璃棒外,还有
(5)“母液 I”中含有大量的Cl-,检验其存在的操作方法为
(6)根据流程分析,“降温”和“盐析”的目的均为
(7)根据流程分析,该工艺中可循环利用的物质为
您最近一年使用:0次



