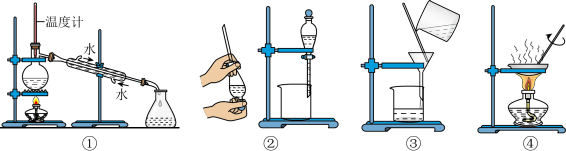
下列实验设计不能 达到实验目的的是
| 实验目的 | 实验设计 | |
| A | 向NaAlO2溶液中加入NaHCO3溶液,观察到有白色沉淀生成 | 证明AlO 得质子的能力强于CO 得质子的能力强于CO |
| B | 工业酒精制备无水乙醇 | 工业酒精中加生石灰,蒸馏 |
| C | 检验NH3 | 用湿润的红色石蕊试纸检验 |
| D | 向NaCl、NaI的混合溶液中滴加少量AgNO3溶液,生成淡黄色沉淀 | 证明Ksp(AgCl) > Ksp(AgI) |
| A.A | B.B | C.C | D.D |
21-22高三上·重庆北碚·开学考试 查看更多[3]
重庆市西南大学附中2022届高三上期开学考试化学试题(已下线)专题3.4.2 沉淀溶解平衡的应用(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)
更新时间:2021-09-05 16:55:07
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】对下列事实的解释或说法错误的是
| A.浓硝酸在光照条件下颜色变黄,说明浓硝酸不稳定 |
| B.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 |
| C.分别蘸有浓氨水和浓盐酸的玻璃棒靠近但不接触,有白烟生成,说明氨气与HCl极易挥发 |
| D.硫化钠溶液中滴入足量酸性高锰酸钾溶液,试管口塞上浸有NaOH溶液的棉花团,目的是吸收反应生成的三氧化硫 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】相比索尔维制碱法,下列不属于侯氏制碱法的优点的是
| A.食盐的利用率高 | B.氨气可循环使用、生产过程简单 |
| C.不生成难以处理的CaCl2 | D.副产物可做氮肥 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列物质不能通过化合反应得到的是
| A.Al(OH)3 | B.Fe (OH)3 | C.Fe3O4 | D.FeS |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
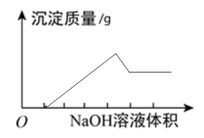
【推荐2】向某无色溶液中逐滴加入 溶液、产生沉淀的质量与加入的
溶液、产生沉淀的质量与加入的 溶液体积的关系如图所示,由此确定,原溶液中含有的阳离子是
溶液体积的关系如图所示,由此确定,原溶液中含有的阳离子是
 溶液、产生沉淀的质量与加入的
溶液、产生沉淀的质量与加入的 溶液体积的关系如图所示,由此确定,原溶液中含有的阳离子是
溶液体积的关系如图所示,由此确定,原溶液中含有的阳离子是
A.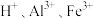 | B.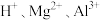 |
C.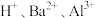 | D.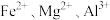 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】已知:室温下,CaCO3的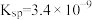 ,H2CO3的电离常数
,H2CO3的电离常数 ,
, ,HClO的电离常数
,HClO的电离常数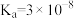 。室温下,向60 mL蒸馏水加入1 g CaCO3,
。室温下,向60 mL蒸馏水加入1 g CaCO3,经过 一段 时间,迅速加入 10 mL蒸馏水 该操作重复多次 ,过程中电导率的变化如图,下列说法不正确 的是

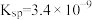 ,H2CO3的电离常数
,H2CO3的电离常数 ,
, ,HClO的电离常数
,HClO的电离常数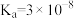 。室温下,向60 mL蒸馏水加入1 g CaCO3,
。室温下,向60 mL蒸馏水加入1 g CaCO3,
| A.a→b:电导率上升是由于CaCO3固体溶解速率大于沉淀速率 |
B.c点溶液中Ca2+浓度接近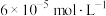 |
| C.g→h:向饱和CaCO3溶液中迅速加入10 mL蒸馏水 |
D.向NaClO浓溶液通入少量CO2气体,溶液含碳微粒主要以 的形式存在 的形式存在 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定温度下,AgCl溶于水达到溶解平衡时,下列说法错误的是
| A.该溶液为此温度下AgCl饱和溶液 |
| B.其他条件不变,再加少量AgCl固体,溶液中c(Ag+)增大 |
| C.沉淀溶解速率等于沉淀生成速率 |
| D.滴加几滴浓的AgNO3溶液,AgCl溶解度降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】湿法提银工艺中,浸出Ag+需加Cl-沉淀。25℃,平衡体系中含Ag微粒的分布系数δ随lgc(Cl-)的变化曲线如图所示。已知:lgKsp(AgCl)=-9.75,下列叙述正确的是
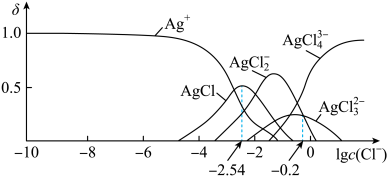
| A.25℃时,AgCl的溶解度随c(Cl-)增大而减小 |
| B.沉淀最彻底时,溶液中c(Ag+)=10-7.21mol•L-1 |
C.25℃时,AgCl +Cl- +Cl- AgCl AgCl 的平衡常数K=10-0.2 的平衡常数K=10-0.2 |
D.当c(Cl-)=10-2.54mol•L-1时,溶液中c(Ag+)>c(Cl-)>c(AgCl ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列叙述错误的是
| A.用金属钠可区分乙醇和乙醚 |
| B.用高锰酸钾酸性溶液可区分乙烷和3-己烯 |
| C.用水可区分苯和溴苯 |
| D.除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤、过滤、干燥、蒸馏 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
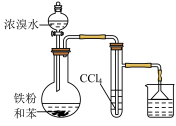
【推荐2】利用下列装置(夹持装置略)或操作进行实验,能达到实验目的的是
|
|
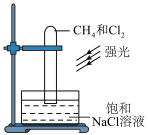
| A. 制备溴苯 | B. 探究CH4与Cl2的取代反应 |
|
|
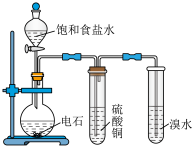
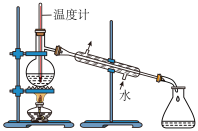
| C. 检验产物乙炔 | D.分离甲苯和乙醇 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次


 ,再通入
,再通入
 增大了
增大了 的溶解度
的溶解度