关于反应4Li+2SOCl2=4LiCl+S+SO2↑的叙述,正确的是
| A.SOCl2既是氧化剂又是还原剂 |
| B.该反应可在水溶液中进行 |
| C.若将该反应设计成原电池,SOCl2在正极上发生反应 |
| D.若生成1molSO2,转移8mol电子 |
2021·全国·模拟预测 查看更多[1]
(已下线)第5周 周测卷-备战2022年高考化学周测与晚练(新高考专用)
更新时间:2021-09-30 12:51:25
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】新型净水剂高铁酸钾(K2FeO4)为暗紫色固体,可溶于水。工业上制备K2FeO4的常用方法之一是次氯酸盐氧化法:
①2FeCl3+10NaOH+3NaClO=2Na2FeO4+9NaCl+5H2O,
②Na2FeO4+2KOH=K2FeO4+2NaOH。下列说法不正确的是
①2FeCl3+10NaOH+3NaClO=2Na2FeO4+9NaCl+5H2O,
②Na2FeO4+2KOH=K2FeO4+2NaOH。下列说法不正确的是
| A.反应①为氧化还原反应,反应②为复分解反应 |
| B.反应①中NaClO是氧化剂 |
| C.反应②的产物K2FeO4中Fe为+6价,具有强氧化性,能杀菌消毒 |
| D.若有2 mol FeCl3发生反应,转移电子的物质的量为2 mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】关于反应 ,下列说法错误的是
,下列说法错误的是
 ,下列说法错误的是
,下列说法错误的是A.生成 ,转移 ,转移 电子 电子 | B. 的价电子排布式为 的价电子排布式为 |
C. 既是氧化剂又是还原剂 既是氧化剂又是还原剂 | D. 中N、O原子均为 中N、O原子均为 杂化 杂化 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(如图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,已知0—t1时,原电池的负极是Al片,反应过程中有红棕色气体产生。下列说法不正确的是
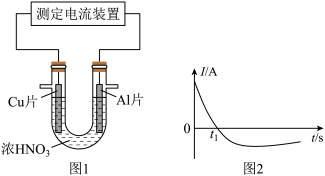

| A.t1时,负极的电极反应式为:Cu-2e- = Cu2+ |
| B.0 — t1时,溶液中的H+向Cu电极移动 |
C.0 — t1时,正极的电极反应式为:2H++ - e- = NO2 + H2O - e- = NO2 + H2O |
| D.t1时,原电池中电子流动方向发生改变是因为Al在浓硝酸中钝化,氧化膜阻碍了Al的进一步反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
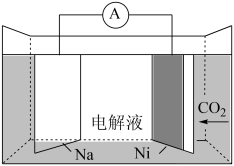
【推荐2】我国科学家研发了一种室温下“可呼吸”的Na—CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na 2Na2CO3+C。下列说法错误的是( )
2Na2CO3+C。下列说法错误的是( )
 2Na2CO3+C。下列说法错误的是( )
2Na2CO3+C。下列说法错误的是( )
A.充电时,ClO 向镍网一极移动 向镍网一极移动 |
B.放电时,正极反应为:3CO2+4e− =2CO +C +C |
| C.放电时,钠失去的电子通过电解液移向正极,构成闭合回路 |
| D.充电时,负极反应为:Na++e−=Na |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】已知:①2K2CrO4+H2SO4=K2Cr2O7+K2SO4+H2O;②K2Cr2O7+6FeSO4+7H2SO4=3Fe2(SO4)3+Cr2(SO4)3+K2SO4+7H2O;③Fe2(SO4)3+2HI=2FeSO4+I2+H2SO4,下列结论正确的是
| A.①②③均是氧化还原反应 |
| B.反应③中生成0.1molI2时转移电子数为0.1NA |
| C.反应②中氧化剂与还原剂的物质的量之比为6:1 |
| D.氧化性强弱顺序是K2Cr2O7>Fe2(SO4)3>I2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】用某复合金属作电极电解催化还原 时,复合金属优先与O原子结合,产物是HCOOH,复合金属优先与C原子结合,产物是
时,复合金属优先与O原子结合,产物是HCOOH,复合金属优先与C原子结合,产物是 和
和 。该反应机理及各产物的物质的量分数如图所示。下列说法正确的是
。该反应机理及各产物的物质的量分数如图所示。下列说法正确的是
 时,复合金属优先与O原子结合,产物是HCOOH,复合金属优先与C原子结合,产物是
时,复合金属优先与O原子结合,产物是HCOOH,复合金属优先与C原子结合,产物是 和
和 。该反应机理及各产物的物质的量分数如图所示。下列说法正确的是
。该反应机理及各产物的物质的量分数如图所示。下列说法正确的是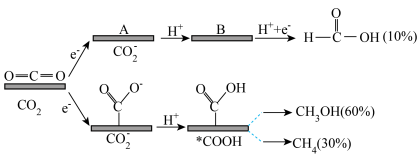
| A.过程中有极性键和非极性的断裂和形成 |
B.中间体B的结构简式为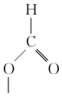 |
C. |
D.若有 完全转化,反应中转移的电子数为3.8mol 完全转化,反应中转移的电子数为3.8mol |
您最近一年使用:0次

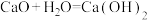 ,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能。
,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能。 6KH(IO3)2+5KCl+3Cl2↑,下列说法不正确的是
6KH(IO3)2+5KCl+3Cl2↑,下列说法不正确的是

