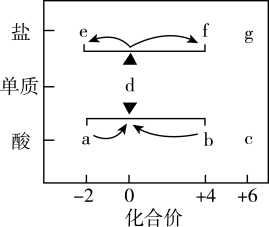
天然海水中所含的离子有Na+、Ca2+、Mg2+、 、Br-、
、Br-、 、
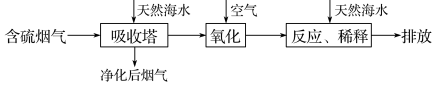
、 等。火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如图所示,下列说法错误的是
等。火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如图所示,下列说法错误的是
 、Br-、
、Br-、 、
、 等。火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如图所示,下列说法错误的是
等。火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如图所示,下列说法错误的是
| A.工艺中天然海水显碱性 |
B.“氧化”是利用氧气将H2SO3、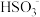 、 、 等氧化生成 等氧化生成 |
C.“反应、稀释”时可能发生反应的离子方程式有:H++ =CO2↑+H2O =CO2↑+H2O |
D.“排放”出来的海水中 的物质的量浓度与进入吸收塔的天然海水相同 的物质的量浓度与进入吸收塔的天然海水相同 |
2021·全国·模拟预测 查看更多[1]
(已下线)第5周 周测卷-备战2022年高考化学周测与晚练(新高考专用)
更新时间:2021-09-30 12:51:25
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验操作、现象及结论错误的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向2 mL0.1 mol/LFeCl3溶液中滴加KSCN溶液,再加入少量KCl固体 | 溶液变红,加入KCl固体后,红色变浅 | 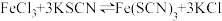 的平衡逆向移动 的平衡逆向移动 |
| B | 用pH计测量相同浓度的NaClO溶液和NaF溶液的pH | NaClO溶液的pH大于NaF溶液的 | Ka(HF)>Ka(HClO) |
| C | 向2支试管中依次加入等体积等浓度的Na2S2O3和H2SO4混合液,分别置于冷水和热水中 | 置于热水中的混合溶液先出现浑浊 | 温度升高,化学反应速率加快 |
| D | 向盛有1 mL0.1 mol/LAgNO3溶液的试管中逐滴滴入0.1 mol/L的Na2CrO4溶液至不再产生沉淀,再向其中滴加0.1 mol/L的Na2S溶液 | 观察到先产生砖红色沉淀(Ag2CrO4),然后砖红色沉淀变为黑色(Ag2S) |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温时,向20mL 0.1mol/L的醋酸溶液中不断滴加0.1mol/L的NaOH溶液,溶液的pH变化曲线如图所示,在滴定过程中,下列关于溶液中离子浓度大小关系的描述不正确的是
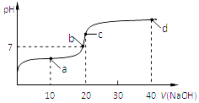

| A.a点时:c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) |
| B.b点时:c(Na+) = c(CH3COO-) |
| C.c点时:c(OH-) =c(CH3COOH) + c(H+) |
| D.d点时:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列说法正确的个数是
①pH=6的溶液一定是酸性溶液
②25℃时,水溶液中水电离出的c(H+)和水电离出的c(OH-)的乘积一定等于10-14
③pH=4的盐酸与pH=4的醋酸溶液等体积混合后pH=4
④25℃,pH=7.0的NaClO和HClO(Ka=4.0×10-8)的混合溶液中,c(HClO)>c(ClO-)=(Na+)
⑤强电解质熔化时都完全电离,弱电解质在水溶液中部分电离
⑥离子化合物都是强电解质,弱电解质都是共价化合物
⑦室温下用干燥、洁净的玻璃棒蘸取氯水,滴在pH试纸上,测出其pH<7
⑧25℃,向pH=m的盐酸中加入pH=n的氢氧化钠溶液,恰好完全反应时,测得盐酸与氢氧化钠溶液的体积比为10:1,则m+n=13
⑨室温时,0.1mol/L某一元酸HA溶液的pH=4,则该酸的电离度为0.1%
⑩酸度的计算公式是 ,常温下0.1mol/L盐酸的AG=12
,常温下0.1mol/L盐酸的AG=12
①pH=6的溶液一定是酸性溶液
②25℃时,水溶液中水电离出的c(H+)和水电离出的c(OH-)的乘积一定等于10-14
③pH=4的盐酸与pH=4的醋酸溶液等体积混合后pH=4
④25℃,pH=7.0的NaClO和HClO(Ka=4.0×10-8)的混合溶液中,c(HClO)>c(ClO-)=(Na+)
⑤强电解质熔化时都完全电离,弱电解质在水溶液中部分电离
⑥离子化合物都是强电解质,弱电解质都是共价化合物
⑦室温下用干燥、洁净的玻璃棒蘸取氯水,滴在pH试纸上,测出其pH<7
⑧25℃,向pH=m的盐酸中加入pH=n的氢氧化钠溶液,恰好完全反应时,测得盐酸与氢氧化钠溶液的体积比为10:1,则m+n=13
⑨室温时,0.1mol/L某一元酸HA溶液的pH=4,则该酸的电离度为0.1%
⑩酸度的计算公式是
 ,常温下0.1mol/L盐酸的AG=12
,常温下0.1mol/L盐酸的AG=12| A.5 | B.3 | C.1 | D.0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】化学与科学、技术、社会、环境密切相关。下列有关说法中错误的是
| A.利用太阳能等清洁能源代替化石燃料,有利于节约能源保护环境 |
| B.日常生活中的废旧电池会污染环境,应填埋处理 |
| C.化学反应过程中,不仅有物质的变化,同时还伴随有能量的变化 |
| D.家用铁锅用水清洗后放置在干燥处,能减缓铁锅生锈 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
A.电解熔融态的 冶炼金属铝 冶炼金属铝 |
B.接触法制硫酸时,煅烧黄铁矿(含 )得到三氧化硫 )得到三氧化硫 |
| C.晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维 |
D.用石灰石-石膏法对燃煤烟气进行脱硫,同时可得到石膏(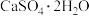 ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】焦亚硫酸钠(Na2S2O5)为白色或黄色结晶,有强烈的刺激性气味,溶于水,水溶液呈酸性,与强酸接触放出SO2并生成相应的盐类;久置空气中,易氧化变质。Na2S2O5可由NaHSO3过饱和溶液经结晶脱水制得。利用SO2生产Na2S2O5的流程如图:
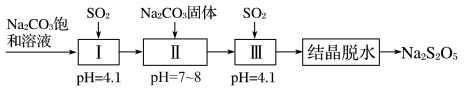
下列相关叙述不正确的是

下列相关叙述不正确的是
| A.1molNa2S2O5晶体中过氧键数目为NA |
| B.Na2S2O5久置空气中可发生反应为:Na2S2O5+O2+H2O=2NaHSO4 |
| C.反应Ⅱ为:Na2CO3+2NaHSO3=2Na2SO3+CO2↑+H2O |
| D.反应Ⅲ中充入SO2是为得到NaHSO3过饱和溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验与结论相匹配的是
| 实验 | 结论 | |
| A. | 用FeCl3溶液刻蚀铜电路板 | 还原性:Fe>Cu |
| B. | 向某溶液中加入淀粉KI溶液,溶液呈蓝色 | 溶液中一定含Fe3+ |
| C. | 将彩色鲜花放入干燥氯气中,发现彩色鲜花褪色 | 氯气具有漂白性 |
| D. | 向久置的Na2SO3溶液中加入足量BaCl2溶液,出现白色沉淀;再加入稀盐酸,沉淀部分溶解 | Na2SO3部分被氧化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次