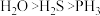根据元素性质递变规律,下列判断不正确的是
| A.酸性:H2SiO3<H3PO4<H2SO4 | B.电负性:I>Br>Cl>F |
| C.第一电离能:N>O>C | D.沸点:NH3>AsH3>PH3 |
更新时间:2021-10-14 23:01:40
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列各组比较中,正确的是
| A.原子半径:S>Na>O | B.热稳定性:NH3>H2O |
| C.碱性:LiOH<NaOH | D.还原性:Br->I- |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列各组元素性质的递变错误的是
| A.Li、Be、B原子最外层电子数依次增多 |
| B.P、S、Cl元素的最高正化合价依次升高 |
| C.B、C、N、O、F原子半径依次增大 |
| D.Be、Mg、Ca、Sr、Ba的失电子能力依次增强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
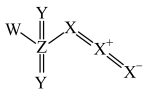
【推荐1】前4周期主族元素X、Y、Z、W的原子序数依次增大,X的单质是空气中含量最多的气体,基态时Y原子的原子轨道上没有未成对电子,Z的最高价与最低负价的绝对值之差为6,W与 Y处于同一主族。下列说法正确的是
| A.原子半径:r(W)>r(Z)>r(Y)>r(X) |
| B.Y的第一电离能比W的大 |
| C.X的简单气态氢化物与Z的单质不能反应 |
| D.Y的最高价氧化物对应水化物的碱性比W的强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W四种短周期元素,原子半径依次增大,X和Y位于同一周期,可组成多种化合物,其中一种是红棕色的大气污染物。Z元素的逐级电离能数据依次为738、1451、7733、10540、13630……下列有关说法正确的是
| A.简单氢化物的沸点:Y>X |
| B.简单离子半径:X>Z>W |
| C.电负性:X>Y>Z |
| D.Z的最高价氧化物对应水化物的碱性大于W |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】卤化钠(NaX)和四卤化钛(TiX4)的熔点如图所示。下判断不正确的是
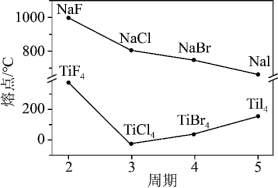
| A.TiF4的熔点反常升高是由于氢键的作用 | B.NaX随X–半径增大,离子键减弱 |
| C.四氯化钛中存在共价键和分子间作用力 | D.由图可看出F的电负性强于Cl、Br、I |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】2021年1月20日中国科学院和中国工程院评选出2020年世界十大科技进展,排在第四位的是一种可借助光将二氧化碳转化为甲烷的新型催化转化方法: CO2+4H2=CH4+2H2O,这是迄今最接近人造光合作用的方法。下列有关CO2、CH4的说法不正确的是
| A.CH4分子为正四面体的空间构型 |
| B.电负性由大到小的顺序是O>C>H |
| C.CO2转化为CH4是将热能转化为化学能 |
| D.CO2转化为CH4利用了CO2的氧化性 |
您最近一年使用:0次
【推荐3】下列说法中正确的是
①原子光谱的特征谱线用于鉴定元素,从 2
2 s2
s2 1跃迁至
1跃迁至 2
2 s2
s2 4时释放能量
4时释放能量
②Cl2分子中,Cl-Cl键是p-pσ键
③铍原子最外层原子轨道的电子云图:
④ ,该电子排布图违背了泡利原理
,该电子排布图违背了泡利原理
⑤键能N-N>P-P、N-H>P-H,因此N2H4的沸点大于P2H4的沸点
⑥碘易溶于浓碘化钾溶液,甲烷难溶于水都可用“相似相溶”原理解释
⑦氟的电负性大于氯的电负性,导致三氟乙酸的酸性大于三氯乙酸的酸性
⑧三氧化硫有单分子气体和三聚分子固体(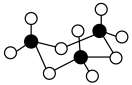 )两种存在形式,两种形式中S原子的杂化轨道类型不同
)两种存在形式,两种形式中S原子的杂化轨道类型不同
①原子光谱的特征谱线用于鉴定元素,从
 2
2 s2
s2 1跃迁至
1跃迁至 2
2 s2
s2 4时释放能量
4时释放能量②Cl2分子中,Cl-Cl键是p-pσ键
③铍原子最外层原子轨道的电子云图:

④
 ,该电子排布图违背了泡利原理
,该电子排布图违背了泡利原理⑤键能N-N>P-P、N-H>P-H,因此N2H4的沸点大于P2H4的沸点
⑥碘易溶于浓碘化钾溶液,甲烷难溶于水都可用“相似相溶”原理解释
⑦氟的电负性大于氯的电负性,导致三氟乙酸的酸性大于三氯乙酸的酸性
⑧三氧化硫有单分子气体和三聚分子固体(
 )两种存在形式,两种形式中S原子的杂化轨道类型不同
)两种存在形式,两种形式中S原子的杂化轨道类型不同| A.①②④⑦ | B.①②⑤⑦ | C.①②⑦⑧ | D.①④⑥⑦ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列有关物质结构与性质说法错误的是
| A.“电子气理论”用于描述金属键的本质,可用于解释金属晶体的延展性、导电性和导热性 |
| B.干冰中CO2的配位数大于冰中水分子的配位数,这与水分子间形成氢键有关 |
| C.邻羟基苯甲酸的沸点低于对羟基苯甲酸的沸点 |
| D.氟的电负性大于氯,所以三氟乙酸的酸性比三氯乙酸的弱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】氮是生命所需的重要元素,是蛋白质的重要组成部分。亚硝酸(HNO2)是一种亮蓝色的弱酸,电离平衡常数为4.6×10-4;亚硝酸既有氧化性,又有还原性。亚硝酸溶液微热即分解。亚硝酸钠(NaNO2)是肉制品生产中最常使用的一种食品添加剂。氨气的燃烧热316.25kJ·mol-1,肼(N2H4)为无色油状液体,有类似于氨的刺鼻气味,是一种强极性化合物。连二亚硝酸(HON=NOH)是一种重要的还原剂,可由亚硝酸和羟胺反应制备,其反应的化学方程式为HONO+H2NOH→HON=NOH+H2O。下列说法错误的是
A.亚硝酸根离子(NO )为V形结构 )为V形结构 | B.羟胺是极性分子 |
| C.1个HON=NOH中有6个σ键 | D.连二亚硝酸可能易溶于水 |
您最近一年使用:0次