回答下列问题
I.已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol。回答有关中和反应的问题。
(1)用0.1molBa(OH)2配成稀溶液与足量稀硝酸反应,能放出_______ kJ热量。
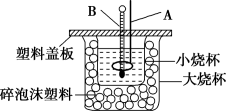
(2)如图装置中仪器A的名称_______ ,作用是_______ ;仪器B的名称_______ ,作用是_______ ;碎泡沫塑料的作用是_______ 。若通过实验测定中和热的ΔH,其结果常常大于-57.3kJ/mol,其原因可能是_______ 。
II.已知某反应A(g)+B(g)⇌C(g)+D(g),反应过程中的能量变化如图所示。
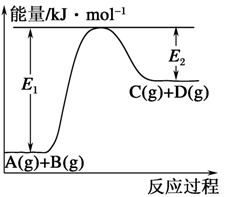
(3)该反应是_______ 反应(填“吸热”或“放热”),该反应的ΔH=_______ kJ·mol-1(用含E1、E2的代数式表示),1mol气体A和1mol气体B具有的总能量比1mol气体C和1mol气体D具有的总能量_______ (填“高”、“低”或“高低不一定”)。
I.已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol。回答有关中和反应的问题。
(1)用0.1molBa(OH)2配成稀溶液与足量稀硝酸反应,能放出
(2)如图装置中仪器A的名称

II.已知某反应A(g)+B(g)⇌C(g)+D(g),反应过程中的能量变化如图所示。

(3)该反应是
更新时间:2021-10-16 19:02:52
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(1)已知:P4(s)+6Cl2(g) 4PCl3(g) ΔH=akJ·mol-1,P4(s)+10Cl2(g)
4PCl3(g) ΔH=akJ·mol-1,P4(s)+10Cl2(g) 4PCl5(g) ΔH=bkJ·mol-1;破坏PCl5中1mol P—Cl键所需能量为ckJ·mol-1,破坏PCl3中1molP—Cl键所需能量为1.2ckJ·mol-1。则破坏Cl2中1molCl—Cl键所需的能量为
4PCl5(g) ΔH=bkJ·mol-1;破坏PCl5中1mol P—Cl键所需能量为ckJ·mol-1,破坏PCl3中1molP—Cl键所需能量为1.2ckJ·mol-1。则破坏Cl2中1molCl—Cl键所需的能量为___________________ 。
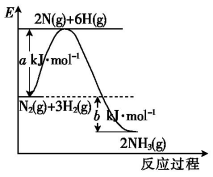
(2)工业合成氨时,合成塔中每生成1molNH3放出46kJ的热量。其反应过程的能量变化如图。b值为________ kJ。加入催化剂,a值____ (填“增大”“减小”或“不变”,下同)。压缩容器体积,b值___ 。
(3)“嫦娥二号”卫星使用液态四氧化二氮和液态偏二甲肼(C2H8N2)作推进剂。N2O4与偏二甲肼燃烧产物只有CO2(g)、H2O(g)、N2(g),并放出大量热,已知10.0 g液态偏二甲肼与液态四氧化二氮完全燃烧可放出425 kJ热量,该反应的热化学方程式为_____________________________ 。
 4PCl3(g) ΔH=akJ·mol-1,P4(s)+10Cl2(g)
4PCl3(g) ΔH=akJ·mol-1,P4(s)+10Cl2(g) 4PCl5(g) ΔH=bkJ·mol-1;破坏PCl5中1mol P—Cl键所需能量为ckJ·mol-1,破坏PCl3中1molP—Cl键所需能量为1.2ckJ·mol-1。则破坏Cl2中1molCl—Cl键所需的能量为
4PCl5(g) ΔH=bkJ·mol-1;破坏PCl5中1mol P—Cl键所需能量为ckJ·mol-1,破坏PCl3中1molP—Cl键所需能量为1.2ckJ·mol-1。则破坏Cl2中1molCl—Cl键所需的能量为(2)工业合成氨时,合成塔中每生成1molNH3放出46kJ的热量。其反应过程的能量变化如图。b值为

(3)“嫦娥二号”卫星使用液态四氧化二氮和液态偏二甲肼(C2H8N2)作推进剂。N2O4与偏二甲肼燃烧产物只有CO2(g)、H2O(g)、N2(g),并放出大量热,已知10.0 g液态偏二甲肼与液态四氧化二氮完全燃烧可放出425 kJ热量,该反应的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】能源是人类赖以生存和发展的重要物质基础,常规能源的合理利用和新能源的合理开发是当今社会面临的严峻课题。
回答下列问题:
(1)乙醇是未来内燃机的首选环保型液体燃料。2.0g乙醇完全燃烧生成液态水放出59.43kJ的热量,则乙醇燃烧的热化学方程式为________ 。
(2)在 的反应中,反应物具有的总能量
的反应中,反应物具有的总能量________ (填“大于”“等于”或“小于”)生成物具有的总能量,那么在发生该反应时,反应物就需要________ (填“放出”或“吸收”)能量才能转化为生成物。
(3)关于用水制取二次能源氢气,以下研究方向不正确的是________ (填序号)。
A.组成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二次能源
B.设法将太阳光聚焦,产生高温,使水分解产生氢气
C.寻找高效催化剂,使水分解产生氢气,同时释放能量
D.寻找特殊催化剂,用于开发廉价能源,以分解水制取氢气
回答下列问题:
(1)乙醇是未来内燃机的首选环保型液体燃料。2.0g乙醇完全燃烧生成液态水放出59.43kJ的热量,则乙醇燃烧的热化学方程式为
(2)在
 的反应中,反应物具有的总能量
的反应中,反应物具有的总能量(3)关于用水制取二次能源氢气,以下研究方向不正确的是
A.组成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二次能源
B.设法将太阳光聚焦,产生高温,使水分解产生氢气
C.寻找高效催化剂,使水分解产生氢气,同时释放能量
D.寻找特殊催化剂,用于开发廉价能源,以分解水制取氢气
您最近一年使用:0次
【推荐1】按要求回答下列问题
(1)以下反应:①木炭与水制备水煤气②氯酸钾分解③炸药爆炸④酸与碱的中和反应⑤生石灰与水作用制熟石灰⑥ 与
与 ⑦浓硫酸溶于水,属于放热反应
⑦浓硫酸溶于水,属于放热反应_______ (填序号)
(2)某温度时,在一个 的恒容容器中,
的恒容容器中, 、
、 、
、 均为气体,三种物质的物质的量随时间的变化曲线如图所示,根据图中数据填空:
均为气体,三种物质的物质的量随时间的变化曲线如图所示,根据图中数据填空:

①该反应的化学方程式为_______
②将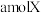 与
与 的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:
的混合气体发生上述反应,反应到某时刻各物质的量恰好满足: ,则原混合气体中
,则原混合气体中
_______ 。
③一定能证明该反应达到平衡状态的是_______ 。
A.单位时间内生成 ,同时消耗
,同时消耗
B.某时刻 、
、 、
、 的浓度相等
的浓度相等
C.混合气体的密度不变
D.混合气体的平均相对分子质量不变
E.各反应物或生成物的反应速率之比等于化学计量数之比
④在其他条件不变时,若改变下列条件,能使生成 的速率变大的是
的速率变大的是_______
A.升高温度 B.增大 的浓度 C.使用催化剂 D.恒容下充入
的浓度 C.使用催化剂 D.恒容下充入 (不参与体系反应)
(不参与体系反应)
(1)以下反应:①木炭与水制备水煤气②氯酸钾分解③炸药爆炸④酸与碱的中和反应⑤生石灰与水作用制熟石灰⑥
 与
与 ⑦浓硫酸溶于水,属于放热反应
⑦浓硫酸溶于水,属于放热反应(2)某温度时,在一个
 的恒容容器中,
的恒容容器中, 、
、 、
、 均为气体,三种物质的物质的量随时间的变化曲线如图所示,根据图中数据填空:
均为气体,三种物质的物质的量随时间的变化曲线如图所示,根据图中数据填空:
①该反应的化学方程式为
②将
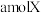 与
与 的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:
的混合气体发生上述反应,反应到某时刻各物质的量恰好满足: ,则原混合气体中
,则原混合气体中
③一定能证明该反应达到平衡状态的是
A.单位时间内生成
 ,同时消耗
,同时消耗
B.某时刻
 、
、 、
、 的浓度相等
的浓度相等C.混合气体的密度不变
D.混合气体的平均相对分子质量不变
E.各反应物或生成物的反应速率之比等于化学计量数之比
④在其他条件不变时,若改变下列条件,能使生成
 的速率变大的是
的速率变大的是A.升高温度 B.增大
 的浓度 C.使用催化剂 D.恒容下充入
的浓度 C.使用催化剂 D.恒容下充入 (不参与体系反应)
(不参与体系反应)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)下列各组化合物中,化学键类型和化合物类型均相同的是_________ (填序号)。
①CaCl2和 Na2S ②Na2O 和 Na2O2③CO2和CaO ④HCl 和 NaOH
(2)下列过程不一定释放能量的是________ 。
①化合反应;②分解反应;③形成化学键;④燃料燃烧;⑤酸碱中和;⑥炸药爆炸
(3)Ba(OH)2 • 8H2O和NH4Cl反应的化学方程式是________________________________ ,反应过程能量变化的图象符合_____________ (填“图1”或“图2”)。

(4)已知1 mol石墨转化为1 mol金刚石要吸收能量,则石墨比金刚石_______ (填“稳定”或“不稳定”)。
(5)一定量的氢气在氧气中充分燃烧并放出热量。若生成气态水放出的热量为Q1,生成液态水放出的热量为Q2,那么Q1______ Q2(填大于、小于或等于)。
(6)已知:4HCl+O2=2Cl2+2H2O。该反应中,4 mol HCl被氧化,放出115.6 kJ的热量,且断开O=O键和Cl-Cl键所需的能量如下图所示。则断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为______ kJ。

①CaCl2和 Na2S ②Na2O 和 Na2O2③CO2和CaO ④HCl 和 NaOH
(2)下列过程不一定释放能量的是
①化合反应;②分解反应;③形成化学键;④燃料燃烧;⑤酸碱中和;⑥炸药爆炸
(3)Ba(OH)2 • 8H2O和NH4Cl反应的化学方程式是

(4)已知1 mol石墨转化为1 mol金刚石要吸收能量,则石墨比金刚石
(5)一定量的氢气在氧气中充分燃烧并放出热量。若生成气态水放出的热量为Q1,生成液态水放出的热量为Q2,那么Q1
(6)已知:4HCl+O2=2Cl2+2H2O。该反应中,4 mol HCl被氧化,放出115.6 kJ的热量,且断开O=O键和Cl-Cl键所需的能量如下图所示。则断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请根据要求回答相关问题:

(1)在装置a的试管里装入固体氢化钾(KH),滴加适量水,观察到烧杯里澄清石灰水变浑浊,在反应后的试管里液几滴酚酞溶液,溶液变红色。该反应是___________ (填“放热”或“吸热”)反应。写出KH与石灰水水反应的化学方程式:___________ 。
(2)在标准状况下,3.36L仅由C、H两种元素组成的某气体质量为2.4g,在25℃和101kPa下完全燃烧生成放出133.5KJ的热量。则该气体的分子式为___________ ;表示该气体燃烧热的热化学方程式为___________ 。

(1)在装置a的试管里装入固体氢化钾(KH),滴加适量水,观察到烧杯里澄清石灰水变浑浊,在反应后的试管里液几滴酚酞溶液,溶液变红色。该反应是
(2)在标准状况下,3.36L仅由C、H两种元素组成的某气体质量为2.4g,在25℃和101kPa下完全燃烧生成放出133.5KJ的热量。则该气体的分子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】生产生活中的化学反应都伴随能量的变化,请根据有关知识回答下列问题:
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用___________ (填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热饭盒”给人们生活带来方便,它可利用下面___________ (填序号)反应释放的热量加热食物。
a.生石灰和水 b.浓硫酸和水 c.硫酸和氢氧化钠溶液
(3) 是优质液体燃料,在25℃、101kPa下,充分燃烧1g
是优质液体燃料,在25℃、101kPa下,充分燃烧1g  并恢复到原状态,会释放22.68kJ的热量。请写出
并恢复到原状态,会释放22.68kJ的热量。请写出 燃烧的热化学反应方程式:
燃烧的热化学反应方程式:___________ 。
已知:

则

___________ 。
(4)已知某些化学键的键能数据如下表所示:
则反应 的焓变
的焓变
___________ 。
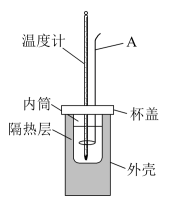
(5)中和反应反应热的测定实验装置如图所示,装置中仪器A的名称是___________ 。
(6)已知:
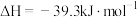 ;
;
 ;
;
由此推知,其中最稳定的磷单质是___________ 。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用
(2)“即热饭盒”给人们生活带来方便,它可利用下面
a.生石灰和水 b.浓硫酸和水 c.硫酸和氢氧化钠溶液
(3)
 是优质液体燃料,在25℃、101kPa下,充分燃烧1g
是优质液体燃料,在25℃、101kPa下,充分燃烧1g  并恢复到原状态,会释放22.68kJ的热量。请写出
并恢复到原状态,会释放22.68kJ的热量。请写出 燃烧的热化学反应方程式:
燃烧的热化学反应方程式:已知:


则


(4)已知某些化学键的键能数据如下表所示:
| 共价键 | H—H | Cl—Cl | H—Cl |
| 键能(kJ/mol) | 436 | 247 | 434 |
则反应
 的焓变
的焓变
(5)中和反应反应热的测定实验装置如图所示,装置中仪器A的名称是

(6)已知:

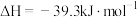 ;
;
 ;
;由此推知,其中最稳定的磷单质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学反应过程中,不仅有物质的变化,同时还伴随有能量的变化。
(1)已知几种化学键的键能如表所示:
则反应Cl2(g)+ 3F2(g) 2ClF3(g) 的△H=
2ClF3(g) 的△H=_____________ kJ·mol—1 。
(2)如图是乙烷、二甲醚燃烧过程中的能量变化图。
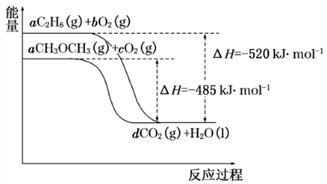
请回答下列问题:
①乙烷的燃烧热ΔH=____ kJ·mol-1。
②等物质的量的液态乙烷比气态乙烷完全燃烧生成稳定的氧化物时放出的热量__ (填“多”或“少”)。
③根据题图写出二甲醚完全燃烧时的热化学方程式_____________ 。
(3)实验室用50mL 0.50mol·L﹣1HCl与50mL 0.55mol·L﹣1NaOH溶液测定中和热。
①若改用60mL HCl进行实验,与原实验相比,所放出的热量____ (填“相等”或“不相等”,忽略实验本身误差,下同),所求中和热_____ (填“相等”或“不相等”,)。
②若用相同浓度和体积的氨水代替NaOH溶液进行上述实验,所求中和热数值会___ (填“偏大”“偏小”或“无影响”)。
(1)已知几种化学键的键能如表所示:
| 化学键 | Cl—Cl | F—F | Cl—F |
| 键能/ kJ·mol—1 | 242 | 159 | 172 |
则反应Cl2(g)+ 3F2(g)
 2ClF3(g) 的△H=
2ClF3(g) 的△H=(2)如图是乙烷、二甲醚燃烧过程中的能量变化图。

请回答下列问题:
①乙烷的燃烧热ΔH=
②等物质的量的液态乙烷比气态乙烷完全燃烧生成稳定的氧化物时放出的热量
③根据题图写出二甲醚完全燃烧时的热化学方程式
(3)实验室用50mL 0.50mol·L﹣1HCl与50mL 0.55mol·L﹣1NaOH溶液测定中和热。
①若改用60mL HCl进行实验,与原实验相比,所放出的热量
②若用相同浓度和体积的氨水代替NaOH溶液进行上述实验,所求中和热数值会
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于放热反应的是_________ (填字母)。
A. 碳与水蒸气反应 B .铝和氧化铁反应 C .CaCO3受热分解 D .锌与盐酸反应
(2)获取能量变化的途径
①通过化学键的键能计算。已知:
计算可得:2H2(g)+O2(g)=2H2O(g) △H=____ 。
②通过物质所含能量计算。已知反应中M+N=P+Q中M、N、P、Q所含能量依次可表示为EM、EN、EP、EQ,该反应△H=______ 。
③通过盖斯定律可计算。已知在25℃、101 kPa时:
I.2Na(s)+ O2(g)=Na2O(s) △H=-412 kJ·mol-1
O2(g)=Na2O(s) △H=-412 kJ·mol-1
II.2Na(s)+O2(g)=Na2O2(s) △H=-511 kJ·mol-1
写出Na2O2与Na反应生成Na2O的热化学方程式_______________ 。
④利用实验装置测量盐酸与NaOH溶液反应的热量变化的过程中,若取50 mL 0.50 mol·L-1的盐酸,则还需加入________ (填序号)。
A .1.0 g NaOH固体 B. 50 mL 0.50 mol·L-1 NaOH溶液 C .50 mL0.55 mol·L-1 NaOH溶液
(1)下列反应中,属于放热反应的是
A. 碳与水蒸气反应 B .铝和氧化铁反应 C .CaCO3受热分解 D .锌与盐酸反应
(2)获取能量变化的途径
①通过化学键的键能计算。已知:
| 化学键种类 | H-H | O=O | O-H |
| 键能(kJ/ mol) | 436 | 496 | 463.4 |
计算可得:2H2(g)+O2(g)=2H2O(g) △H=
②通过物质所含能量计算。已知反应中M+N=P+Q中M、N、P、Q所含能量依次可表示为EM、EN、EP、EQ,该反应△H=
③通过盖斯定律可计算。已知在25℃、101 kPa时:
I.2Na(s)+
 O2(g)=Na2O(s) △H=-412 kJ·mol-1
O2(g)=Na2O(s) △H=-412 kJ·mol-1II.2Na(s)+O2(g)=Na2O2(s) △H=-511 kJ·mol-1
写出Na2O2与Na反应生成Na2O的热化学方程式
④利用实验装置测量盐酸与NaOH溶液反应的热量变化的过程中,若取50 mL 0.50 mol·L-1的盐酸,则还需加入
A .1.0 g NaOH固体 B. 50 mL 0.50 mol·L-1 NaOH溶液 C .50 mL0.55 mol·L-1 NaOH溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氮、磷、砷(As)、锑(Sb)、铋(Bi)、镆(Mc)为元素周期表中原子序数依次增大的同族元素。回答下列问题:
(1)砷在元素周期表中的位置_______ 。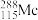 的中子数为
的中子数为_______ 。已知:P(s,白磷)=P(s,黑磷) 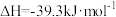 ;P(s,白磷)=P (s,红磷)
;P(s,白磷)=P (s,红磷)  ;由此推知,其中最稳定的磷单质是
;由此推知,其中最稳定的磷单质是_______ 。
(2)氮和磷氢化物性质的比较:热稳定性:NH3_______ PH3(填“>”或“<”)。沸点:N2H4_______ P2H4(填“>”或“<”),判断依据是_______ 。
(3)PH3和NH3与卤化氢的反应相似,产物的结构和性质也相似。下列对PH3与HI反应产物的推断正确的是___ (填序号)。
a.不能与NaOH反应 b.含离子键 c.含共价键
(4)SbCl3能发生较强烈的水解,生成难溶的SbOCl,写出该反应的化学方程式_____ 。
(5)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

通过计算,可知系统(I)和系统(II)制氢的热化学方程式分别为_____ 、_____ ,制得等量H2所需能量较少的是____ 。
(1)砷在元素周期表中的位置
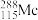 的中子数为
的中子数为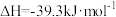 ;P(s,白磷)=P (s,红磷)
;P(s,白磷)=P (s,红磷)  ;由此推知,其中最稳定的磷单质是
;由此推知,其中最稳定的磷单质是(2)氮和磷氢化物性质的比较:热稳定性:NH3
(3)PH3和NH3与卤化氢的反应相似,产物的结构和性质也相似。下列对PH3与HI反应产物的推断正确的是
a.不能与NaOH反应 b.含离子键 c.含共价键
(4)SbCl3能发生较强烈的水解,生成难溶的SbOCl,写出该反应的化学方程式
(5)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

通过计算,可知系统(I)和系统(II)制氢的热化学方程式分别为
您最近一年使用:0次
【推荐2】
(1)已知:N2(g)+3H2(g) 2NH3(g)ΔH=﹣92.4 kJ•
2NH3(g)ΔH=﹣92.4 kJ• ,
,
2H2(g)+O2(g)=2H2O(l)ΔH=﹣571.6 kJ• ,
,
则2N2(g)+6H2O(l) 4NH3(g)+3O2(g) ΔH=
4NH3(g)+3O2(g) ΔH=_______ 。
(2)20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量过渡态。分析图中信息,回答下列问题:
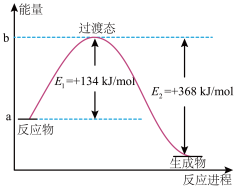
上图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出CO2和NO反应生成NO2和CO的热化学方程式:__________________________________ 。在反应体系中加入催化剂,E1和E2的变化是:E1__ ,E2__ (填“增大”“减小”或“不变”),对反应热是否有影响?__ (填“是”或“否”),原因是________________________________________ 。
(3)常温常压下断裂1 mol气体分子化学键所吸收的能量或形成1 mol气体分子化学键所放出的能量称为键能(单位为kJ·mol-1)。下表是一些键能数据(kJ·mol-1):请完成下列问题。
热化学方程式2H2(g)+S2(g)=2H2S(g) ΔH=-229 kJ·mol-1,则X=________ 。
(1)已知:N2(g)+3H2(g)
 2NH3(g)ΔH=﹣92.4 kJ•
2NH3(g)ΔH=﹣92.4 kJ• ,
,2H2(g)+O2(g)=2H2O(l)ΔH=﹣571.6 kJ•
 ,
,则2N2(g)+6H2O(l)
 4NH3(g)+3O2(g) ΔH=
4NH3(g)+3O2(g) ΔH=(2)20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量过渡态。分析图中信息,回答下列问题:

上图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出CO2和NO反应生成NO2和CO的热化学方程式:
(3)常温常压下断裂1 mol气体分子化学键所吸收的能量或形成1 mol气体分子化学键所放出的能量称为键能(单位为kJ·mol-1)。下表是一些键能数据(kJ·mol-1):请完成下列问题。
H—H | 436 | S=S | X | H—S | 339 |
热化学方程式2H2(g)+S2(g)=2H2S(g) ΔH=-229 kJ·mol-1,则X=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知下列反应:
i.

ii.
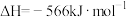
iii.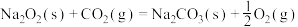

回答下列问题:
(1)CO的燃烧热为___________ 。
(2)根据上述信息,写出一氧化碳与过氧化钠在催化剂的作用下生成固体碳酸钠的热化学方程式___________ 。
(3)工业生产中CO2可用碱液吸收,发生如下反应:
i: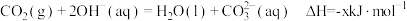
ii: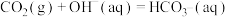
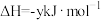
①反应的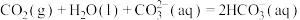 的
的
___________  ;
;
②标准状况下,1.12LCO2与足量的强碱溶液充分反应,放出的热量为___________ kJ(用含x、y的式子表示)。
i.


ii.

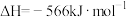
iii.
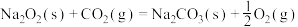

回答下列问题:
(1)CO的燃烧热为
(2)根据上述信息,写出一氧化碳与过氧化钠在催化剂的作用下生成固体碳酸钠的热化学方程式
(3)工业生产中CO2可用碱液吸收,发生如下反应:
i:
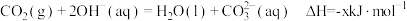
ii:
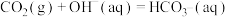
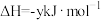
①反应的
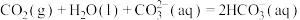 的
的
 ;
;②标准状况下,1.12LCO2与足量的强碱溶液充分反应,放出的热量为
您最近一年使用:0次




