我国正在推行垃圾分类,为研究废旧电池的再利用,实验室利用旧电池的铜帽(主要成分为Zn和Cu)回收Cu并制备ZnO的部分实验流程如图所示。下列说法错误的是
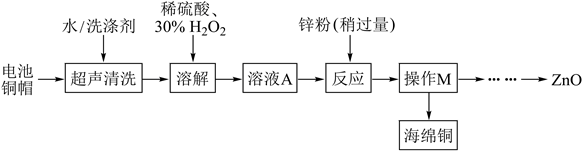

| A.“溶解”过程中,加入H2O2的目的是氧化铜单质 |
| B.溶液A中一定含有的溶质有ZnSO4和CuSO4 |
| C.通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥等操作,可得到ZnO |
| D.“溶解”过程中,温度不宜过高化学 |
更新时间:2021-11-01 15:55:11
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】以超细含铝废渣(主要成分为 ,含有少量
,含有少量 、PbO杂质)为原料制备钾冰晶石(
、PbO杂质)为原料制备钾冰晶石(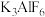 )的工艺流程如图所示,已知
)的工艺流程如图所示,已知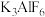 微溶于水,“萃取”过程可表示为
微溶于水,“萃取”过程可表示为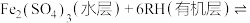
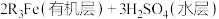 。下列有关说法中不正确的是
。下列有关说法中不正确的是

 ,含有少量
,含有少量 、PbO杂质)为原料制备钾冰晶石(
、PbO杂质)为原料制备钾冰晶石(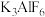 )的工艺流程如图所示,已知
)的工艺流程如图所示,已知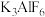 微溶于水,“萃取”过程可表示为
微溶于水,“萃取”过程可表示为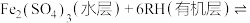
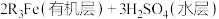 。下列有关说法中不正确的是
。下列有关说法中不正确的是
A.氧化时反应液的pH控制在较低水平的目的是抑制 、 、 的水解 的水解 |
B.由有机层获取 溶液的操作是向有机层中加入适量的 溶液的操作是向有机层中加入适量的 固体,充分振荡,静置,分离出水层 固体,充分振荡,静置,分离出水层 |
C.“合成”时发生反应的化学方程式为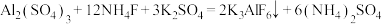 |
| D.“系列操作”后“滤液”的主要成分可作氮肥 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某白色粉末由两种物质组成,对其进行如下实验。
①取少量白色粉末加入足量水充分溶解,过滤并洗涤得到滤液和滤渣;
②取少量①的滤液,加入 溶液,有白色沉淀;
溶液,有白色沉淀;
③取少量①的滤渣,加入稀盐酸,滤渣溶解得无色溶液,同时有无色无味气体产生。
该白色粉末中可能存在的是
①取少量白色粉末加入足量水充分溶解,过滤并洗涤得到滤液和滤渣;
②取少量①的滤液,加入
 溶液,有白色沉淀;
溶液,有白色沉淀;③取少量①的滤渣,加入稀盐酸,滤渣溶解得无色溶液,同时有无色无味气体产生。
该白色粉末中可能存在的是
A. 、 、 | B.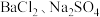 |
C.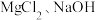 | D.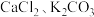 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验,能达到实验目的的是
| A | B | C | D |
| 观察钾元素的焰色 | 蒸发结晶NaCl | 实验室制备Fe(OH)2 | 制备氧化钠 |
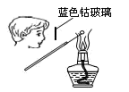 | 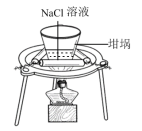 | 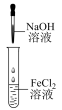 | 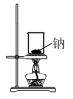 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验操作不正确 的是
| A.蒸发结晶时,应将蒸发皿中的NaCl溶液全部蒸干才停止加热 |
| B.蒸馏操作时,冷却水从冷凝管的下口通入,上口流出 |
| C.用托盘天平称量药品时,将砝码置于天平右盘 |
| D.用浓硫酸配制一定物质的量浓度的稀硫酸时,应冷却至室温再转移到容量瓶中 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】咖啡因是咖啡中一种生物碱,对人类的健康发挥着积极作用。随着生活水平的日益提高,很多人不喜欢喝速溶咖啡,喜欢自己现磨现冲咖啡。化学老师喜欢的一种冲泡咖啡的过程如图:
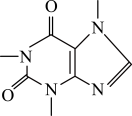 咖啡因
咖啡因
|
|
|
|
(1)放入适量咖啡粉 | (2)倒入适量的热水 | (3)静置3分钟按压滤网 | (4)倒入烧杯中 |
冲泡咖啡涉及了很多化学知识,下列说法不正确的是
| A.咖啡因的分子式为C8H10N4O2,一个分子中采取sp3杂化的原子数为6个 |
| B.将咖啡豆研磨成粉末,主要为了增大了咖啡的浸泡面积,冲泡出来的咖啡口感较浓郁 |
| C.咖啡中的咖啡因可通过热水浸泡溶解,与咖啡因能与水形成氢键有关 |
| D.步骤(2)(3)(4)涉及的主要操作等同于固-液萃取和分液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】由含硒废料(主要含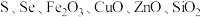 等)制取硒的流程如下:
等)制取硒的流程如下:
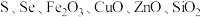 等)制取硒的流程如下:
等)制取硒的流程如下: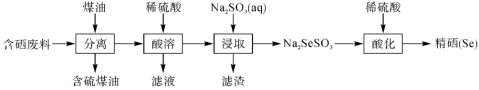

| A.流程中的“分离”的方法是过滤 |
B.“滤液”中主要存在的阴离子是 |
C.“酸化”时发生反应的离子方程式为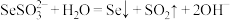 |
D. 晶胞如上图所示,1个 晶胞如上图所示,1个 晶胞中有16个 晶胞中有16个 原子 原子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】Li和 在450℃时反应制得储氢燃料
在450℃时反应制得储氢燃料 ,
, 易水解,在空气中加热可发生剧烈燃烧。下图是某实验小组设计的实验宊制备少量
易水解,在空气中加热可发生剧烈燃烧。下图是某实验小组设计的实验宊制备少量 装置图。下列有关说法不正确的是
装置图。下列有关说法不正确的是
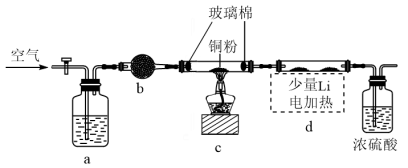
 在450℃时反应制得储氢燃料
在450℃时反应制得储氢燃料 ,
, 易水解,在空气中加热可发生剧烈燃烧。下图是某实验小组设计的实验宊制备少量
易水解,在空气中加热可发生剧烈燃烧。下图是某实验小组设计的实验宊制备少量 装置图。下列有关说法不正确的是
装置图。下列有关说法不正确的是
| A.洗气瓶a中盛放NaOH溶液 |
| B.反应时,先点燃c中酒精灯,再对d加热 |
C.取少量反应后固体,滴加酚酞溶液,若溶液变红说明反应后固体中一定含 |
D.浓硫酸的作用是防止空气中的水蒸气和氧气进入d,避免 水解和燃烧 水解和燃烧 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某兴趣小组查阅资料得知:碘化钠是白色晶体无嗅,味咸而微苦,在空气和水溶液中逐渐析出碘而变黄或棕色。工业上用NaOH溶液、水合肼制取碘化钠固体,其制备流程图如下,有关说法不正确的是( )

已知:N2H4·H2O在100℃以上分解。

已知:N2H4·H2O在100℃以上分解。
| A.已知在合成过程的反应产物中含有NaIO3,若合成过程中消耗了3mol I2,最多能生成NaIO3的物质的量为1 mol |
| B.上述还原过程中主要的离子方程式为2IO3-+3N2H4·H2O=2I-+3N2+9H2O |
| C.为了加快反应速率,上述还原反应最好在高温条件下进行 |
| D.工业上也可以用硫化钠或铁屑还原碘酸钠制备碘化钠,但水合肼还原法制得的产品纯度更高,因产物是N2和H2O,没有其他副产物,不会引入杂质 |
您最近一年使用:0次

 形式存在,实验小组通过以下实验检验菠菜中的铁元素,下列说法错误的是
形式存在,实验小组通过以下实验检验菠菜中的铁元素,下列说法错误的是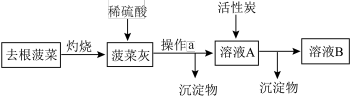
 后,滴加KSCN溶液可检验铁元素
后,滴加KSCN溶液可检验铁元素



 所示装置可分别制取少量CO2、NO和O2
所示装置可分别制取少量CO2、NO和O2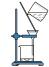 ),向漏斗中加适量水,搅拌并滤干
),向漏斗中加适量水,搅拌并滤干 还原
还原 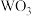 制备金属 W的装置如下图所示
制备金属 W的装置如下图所示 粒中往往含有硫等杂质,焦性没食子酸溶液用于吸收少量氧气
粒中往往含有硫等杂质,焦性没食子酸溶液用于吸收少量氧气 ,下列说法错误的是
,下列说法错误的是
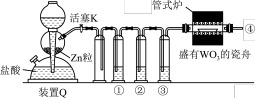
 ,可加快产生
,可加快产生  处收集气体并点燃,通过声音判断气体纯度
处收集气体并点燃,通过声音判断气体纯度 启普发生器
启普发生器

