用铋酸钠鉴定锰离子的原理可表示为: ,下列分析错误的是
,下列分析错误的是
 ,下列分析错误的是
,下列分析错误的是A.该反应中 被氧化为 被氧化为 | B.该反应中还原剂与氧化剂之比为5∶2 |
C.该反应中 的还原性强于 的还原性强于 | D.该反应每生成 还原产物,则转移 还原产物,则转移 电子 电子 |
更新时间:2021-11-06 11:13:54
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】CaH2可以作为供氢剂(其中CaH2中氢元素为-1价),反应方程式如下:CaH2+2H2O=Ca (OH)2+2H2↑,以下说法正确的是
| A.水既不是氧化剂也不是还原剂 | B.Ca (OH)2是氧化产物 |
| C.被氧化的原子与被还原的原子个数比为1:1 | D.水既是氧化剂又是还原剂 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】黄铜矿(CuFeS2)常用于提炼金属铜。黄铜矿焙烧过程中所发生的反应比较复杂,其中主要反应之一的化学方程式为:2CuFeS2+O2 □+2FeS+SO2(已配平),下列关于该反应的说法错误的是
□+2FeS+SO2(已配平),下列关于该反应的说法错误的是
 □+2FeS+SO2(已配平),下列关于该反应的说法错误的是
□+2FeS+SO2(已配平),下列关于该反应的说法错误的是| A.方框中的物质应为Cu2S |
| B.反应中的氧化剂为CuFeS2和O2 |
| C.反应中SO2既是氧化产物又是还原产物 |
| D.反应中若有1molSO2生成,则一定有4mol电子发生转移 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】已知在酸性溶液中的还原性强弱顺序为:SO2 >I– >H2O2> Fe2+>Cl–,下列反应不可能 发生的是
| A.H2O2+ H2SO4 = SO2↑+ O2↑+2H2O | B.2I– +2Fe3+= I2+2Fe2+ |
| C.2Fe3++ SO2 +2H2O= 2Fe2++SO42– +4H+ | D.SO2 +2H2O+ I2= H2SO4+2HI |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】根据反应:①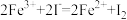 ,②
,②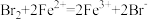 ,判断以下各物质的氧化性由强到弱的顺序正确的是
,判断以下各物质的氧化性由强到弱的顺序正确的是
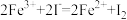 ,②
,②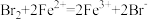 ,判断以下各物质的氧化性由强到弱的顺序正确的是
,判断以下各物质的氧化性由强到弱的顺序正确的是A.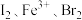 | B. |
C. | D.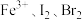 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】在相同条件下,下列反应在溶液中均可发生:
①3S2O +2Cr3++7H2O=Cr2O
+2Cr3++7H2O=Cr2O +6SO
+6SO +14H+
+14H+
②Cr2O +14H++6Cl-=2Cr3++3Cl2↑+7H2O
+14H++6Cl-=2Cr3++3Cl2↑+7H2O
③Cl2+2Fe2+=2Cl-+2Fe3+
④Sn2++2Fe3+=2Fe2++Sn4+
下列有关说法正确的是
①3S2O
 +2Cr3++7H2O=Cr2O
+2Cr3++7H2O=Cr2O +6SO
+6SO +14H+
+14H+②Cr2O
 +14H++6Cl-=2Cr3++3Cl2↑+7H2O
+14H++6Cl-=2Cr3++3Cl2↑+7H2O③Cl2+2Fe2+=2Cl-+2Fe3+
④Sn2++2Fe3+=2Fe2++Sn4+
下列有关说法正确的是
A.在溶液中Fe2+和S2O 能大量共存 能大量共存 |
| B.反应②中Cl元素被还原,反应③中Cl元素被氧化 |
| C.向FeCl2溶液中加入K2Cr2O7溶液时,Cl-先被氧化 |
D.离子的氧化性:S2O >Cr2O >Cr2O >Cl2>Fe3+>Sn4+ >Cl2>Fe3+>Sn4+ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】2021年,我国科学家利用 为原料人工合成淀粉,在未来具有极高的经济价值。已知合成淀粉过程中发生反应:
为原料人工合成淀粉,在未来具有极高的经济价值。已知合成淀粉过程中发生反应: ,设
,设 为阿伏加德罗常数,下列有关说法正确的是。
为阿伏加德罗常数,下列有关说法正确的是。
 为原料人工合成淀粉,在未来具有极高的经济价值。已知合成淀粉过程中发生反应:
为原料人工合成淀粉,在未来具有极高的经济价值。已知合成淀粉过程中发生反应: ,设
,设 为阿伏加德罗常数,下列有关说法正确的是。
为阿伏加德罗常数,下列有关说法正确的是。A. 中含有过氧键数目为 中含有过氧键数目为 |
B.标况下, 中含有的羟基数为 中含有的羟基数为 |
| C.反应过程中HCHO为还原产物 |
D.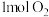 参与反应转移电子数为 参与反应转移电子数为 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】设NA为阿伏伽德罗常数的值,下列说法不正确的是
| A.标准状况下,2.24 L Cl2与足量铁粉反应转移的电子数为0.2 NA |
| B.2.8 g CO和N2的混合气中,所含原子总数为0.2 NA |
C.物质的量浓度为0.5 mol·L-1Al2(SO4)3溶液中,含有SO 数目为1.5 NA 数目为1.5 NA |
| D.2.3 g Na完全与氧气反应生成氧化钠和过氧化钠,失去的电子数为0.1 NA |
您最近一年使用:0次

 。下列说法正确的是
。下列说法正确的是 ,转移6个
,转移6个




