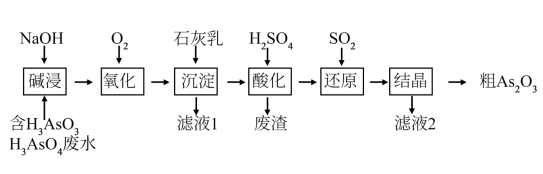
某含砷(As)的有毒工业废水经如图流程转化为粗 ,已知:亚砷酸钙微溶于水,砷酸钙难溶于水。
,已知:亚砷酸钙微溶于水,砷酸钙难溶于水。
(1)砷是氮的同族元素,且比氮多2个电子层,则As在元素周期表中的位置为___________ , 的电子式为
的电子式为___________ 。
(2)“碱浸”的目的是将废水中的 和
和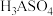 转化为盐,
转化为盐,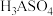 转化为
转化为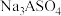 的离子方程式为
的离子方程式为___________ 。
(3)“氧化”时,1mol 转化为
转化为 至少需要
至少需要
___________ mol。
(4)通过对 溶液进行加热,再过滤可制得粗
溶液进行加热,再过滤可制得粗 。
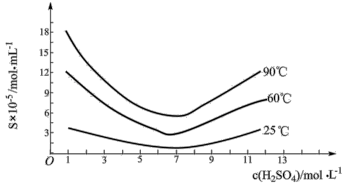
。 在不同温度和不同浓度硫酸中的溶解度(S)曲线如图所示。为提高粗
在不同温度和不同浓度硫酸中的溶解度(S)曲线如图所示。为提高粗 的沉淀率,则“结晶”过程应控制的最佳条件是温度
的沉淀率,则“结晶”过程应控制的最佳条件是温度___________ 、硫酸浓度___________ 。
(5)从绿色化学和综合利用的角度考虑,滤液2需要处理,可将滤液2返回___________ 环节循环使用。
 ,已知:亚砷酸钙微溶于水,砷酸钙难溶于水。
,已知:亚砷酸钙微溶于水,砷酸钙难溶于水。
(1)砷是氮的同族元素,且比氮多2个电子层,则As在元素周期表中的位置为
 的电子式为
的电子式为(2)“碱浸”的目的是将废水中的
 和
和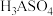 转化为盐,
转化为盐,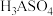 转化为
转化为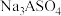 的离子方程式为
的离子方程式为(3)“氧化”时,1mol
 转化为
转化为 至少需要
至少需要
(4)通过对
 溶液进行加热,再过滤可制得粗
溶液进行加热,再过滤可制得粗 。
。 在不同温度和不同浓度硫酸中的溶解度(S)曲线如图所示。为提高粗
在不同温度和不同浓度硫酸中的溶解度(S)曲线如图所示。为提高粗 的沉淀率,则“结晶”过程应控制的最佳条件是温度
的沉淀率,则“结晶”过程应控制的最佳条件是温度
(5)从绿色化学和综合利用的角度考虑,滤液2需要处理,可将滤液2返回
更新时间:2021-11-23 12:49:22
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】元素周期表的一部分如图,根据①~⑨在元素周期表中的位置,按题目要求回答下列问题:
(1)在元素①~⑨中,金属性最强的元素是_____ (填元素符号)。
(2)③~⑥四种元素的原子半径由大到小的顺序是_____ (填元素符号)。
(3)⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较强的是_____ (填化学式)。
(4)写出由元素⑤和元素④形成的原子个数比为1:1的化合物的电子式:_____ 。
(5)写出元素⑦的单质与元素⑤的最高价氧化物对应的水化物之间反应的离子方程式:_____ 。
(6)高温灼烧仅由元素⑤和元素⑧形成的常见化合物时,火焰呈_____ 色。
| 族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(2)③~⑥四种元素的原子半径由大到小的顺序是
(3)⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较强的是
(4)写出由元素⑤和元素④形成的原子个数比为1:1的化合物的电子式:
(5)写出元素⑦的单质与元素⑤的最高价氧化物对应的水化物之间反应的离子方程式:
(6)高温灼烧仅由元素⑤和元素⑧形成的常见化合物时,火焰呈
您最近一年使用:0次
【推荐2】锂在有机合成、电池等领域中有重要的作用。
I. 的制备和应用如下图所示。
的制备和应用如下图所示。
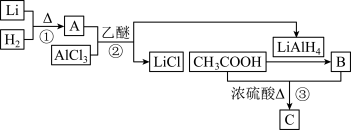
(1)锂元素在元素周期表中的位置_______________________ 。
(2)写出A的电子式___________________________ 。
(3) 是有机合成中常用的还原剂,试写出反应③的化学方程式
是有机合成中常用的还原剂,试写出反应③的化学方程式_________________ 。
II.磷酸亚铁锂是新型锂离子电池的首选电极材料,是以铁棒为阳极,石墨为阴极,电解磷酸二氢铵、氯化锂混合溶液,析出磷酸亚铁锂沉淀,在800℃左右、惰性气体氛围中煅烧制得。在锂离子电池中,需要一种有机聚合物作为正负极之间锂离子迁移的介质,该有机聚合物的单体之一(用M表示)的结构简式如下:
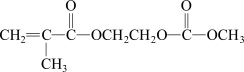
请回答下列问题:
(4)制备磷酸亚铁锂必须在惰性气体氛围中进行,其原因是_______________ 。
(5)阳极生成磷酸亚铁锂的电极反应式为___________________ 。
(6)写出M与足量氢氧化钠溶液反应的化学方程式_____________________ 。
(7)该电池充电时阳极的磷酸亚铁锂生成磷酸铁,则放电时正极的电极反应式为___________ 。
I.
 的制备和应用如下图所示。
的制备和应用如下图所示。
(1)锂元素在元素周期表中的位置
(2)写出A的电子式
(3)
 是有机合成中常用的还原剂,试写出反应③的化学方程式
是有机合成中常用的还原剂,试写出反应③的化学方程式II.磷酸亚铁锂是新型锂离子电池的首选电极材料,是以铁棒为阳极,石墨为阴极,电解磷酸二氢铵、氯化锂混合溶液,析出磷酸亚铁锂沉淀,在800℃左右、惰性气体氛围中煅烧制得。在锂离子电池中,需要一种有机聚合物作为正负极之间锂离子迁移的介质,该有机聚合物的单体之一(用M表示)的结构简式如下:
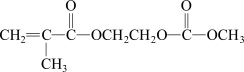
请回答下列问题:
(4)制备磷酸亚铁锂必须在惰性气体氛围中进行,其原因是
(5)阳极生成磷酸亚铁锂的电极反应式为
(6)写出M与足量氢氧化钠溶液反应的化学方程式
(7)该电池充电时阳极的磷酸亚铁锂生成磷酸铁,则放电时正极的电极反应式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表表示的是元素周期表中短周期元素,根据要求回答下列问题:
(1)④⑥元素气态氢化物的稳定性比较______ >_______ (写化学式);
(2)③号元素与其他元素可形成10个电子的阳离子和阴离子,其离子符号分别为______ 、______ 。
(3)用电子式表示⑧和③元素形成A2B型化合物的过程_____________________
(4)用电子式表示⑤和⑥元素形成A2B型化合物的过程________________________
| ⑧ | |||||||
| ① | ② | ③ | ④ | ||||
| ⑤ | ⑥ | ⑦ | |||||
(1)④⑥元素气态氢化物的稳定性比较
(2)③号元素与其他元素可形成10个电子的阳离子和阴离子,其离子符号分别为
(3)用电子式表示⑧和③元素形成A2B型化合物的过程
(4)用电子式表示⑤和⑥元素形成A2B型化合物的过程
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】锂辉石的主要成分有Li2O、Al2O3、SiO2,还含有少量Fe3O4、MgO等杂质,利用锂辉石制取Li2CO3的工艺流程如下:
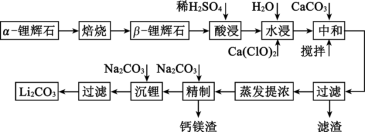
已知:ⅰ.α- 锂辉石是致密坚硬的固体,β- 锂辉石具有疏松多孔结构;
ⅱ.CaCO3的溶度积常数为1×10−9,MgCO3的溶度积常数为1×10−6。
回答下列问题:
(1)焙烧的目的是_______ 。
(2)为提高酸浸速率,可采取的措施是_______ (填一种即可)。
(3)水浸时加入少量Ca(ClO)2溶液,其目的是_______ ,发生反应的离子方程式为_______ ,该方案中不选择H2O2做氧化剂的原因是_______ 。
(4)中和过程中加入CaCO3,一方面是为了除去多余硫酸,另一方面是为了_______ 。
(5)精制过程是为了除去钙镁离子,钙镁渣中含CaCO3、Mg2(OH)2CO3和MgCO3,写出生成Mg2(OH)2CO3的离子方程式:_______ 。
(6)精制过程中,当钙离子刚好沉淀完全时[c(Ca2+)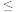 1×10−5 mol·L−1],溶液的pH为9,则CO
1×10−5 mol·L−1],溶液的pH为9,则CO 的一级水解常数约为
的一级水解常数约为_______ (忽略CO 的二级水解及其他离子的水解)。
的二级水解及其他离子的水解)。

已知:ⅰ.α- 锂辉石是致密坚硬的固体,β- 锂辉石具有疏松多孔结构;
ⅱ.CaCO3的溶度积常数为1×10−9,MgCO3的溶度积常数为1×10−6。
回答下列问题:
(1)焙烧的目的是
(2)为提高酸浸速率,可采取的措施是
(3)水浸时加入少量Ca(ClO)2溶液,其目的是
(4)中和过程中加入CaCO3,一方面是为了除去多余硫酸,另一方面是为了
(5)精制过程是为了除去钙镁离子,钙镁渣中含CaCO3、Mg2(OH)2CO3和MgCO3,写出生成Mg2(OH)2CO3的离子方程式:
(6)精制过程中,当钙离子刚好沉淀完全时[c(Ca2+)
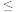 1×10−5 mol·L−1],溶液的pH为9,则CO
1×10−5 mol·L−1],溶液的pH为9,则CO 的一级水解常数约为
的一级水解常数约为 的二级水解及其他离子的水解)。
的二级水解及其他离子的水解)。
您最近一年使用:0次
【推荐2】下表为元素周期表的一部分,其中的编号代表对应的不同元素。
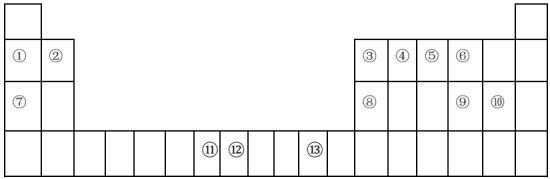
回答下列问题(涉及到元素序号用化学用语作答):
(1)写出基态⑥原子的电子排布式______
(2)基态③原子中电子占据最高能级的符号是______ ,该能级的电子云轮廓图为______ 形。基态⑦原子共有______ 种不同运动状态的电子。
(3)表中属于ds区的元素是______ 。
(4)写出⑧的氧化物与NaOH溶液反应的离子方程式______ 。
(5)从原子结构角度解释非金属性⑩>⑨的原因______ 。
(6)元素⑪(设为字母A)和元素⑫(设为字母B)的部分电离能数据(用 ,
, ,
, 表示)
表示)
如表:
比较两元素的 ,
, 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难,请解释原因
再失去一个电子难,请解释原因______ 。

回答下列问题(涉及到元素序号用化学用语作答):
(1)写出基态⑥原子的电子排布式
(2)基态③原子中电子占据最高能级的符号是
(3)表中属于ds区的元素是
(4)写出⑧的氧化物与NaOH溶液反应的离子方程式
(5)从原子结构角度解释非金属性⑩>⑨的原因
(6)元素⑪(设为字母A)和元素⑫(设为字母B)的部分电离能数据(用
 ,
, ,
, 表示)
表示)如表:
元素 | A | B | |
电离能/( |
| 717 | 759 |
| 1509 | 1561 | |
| 3248 | 257 | |
 ,
, 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难,请解释原因
再失去一个电子难,请解释原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】镁及其化合物是实验设计的热点载体。某学习小组设计实验探究镁与二氧化氮反应的产物,实验装置如图所示。 能与水反应;②反应完后E中有
能与水反应;②反应完后E中有 。
。
回答下列问题:
(1)仪器a的名称为___________ ;a中试剂是___________ 。
(2)实验时,为了防止Mg与空气中氧气等反应,操作为___________ 。
(3)实验测得Mg与 反应生成MgO、
反应生成MgO、 和
和 ,其中
,其中 和
和 的物质的量相等,则C中反应的化学方程式为
的物质的量相等,则C中反应的化学方程式为___________ 。装置D的作用是___________ 。
(4)E装置中发生反应的离子方程式为___________ 。
(5)写出氮化镁与水反应的化学方程式___________ 。
(6)已知浓硝酸分解反应为: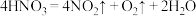 ,干燥生成的气体后,该气体混合物能使带火星的木条复燃,由此某同学得出
,干燥生成的气体后,该气体混合物能使带火星的木条复燃,由此某同学得出 气体能支持燃烧的说法,你认为该说法正确吗?并说明理由
气体能支持燃烧的说法,你认为该说法正确吗?并说明理由___________ 。
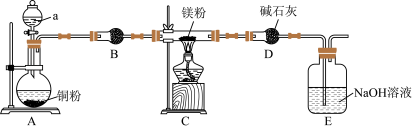
 能与水反应;②反应完后E中有
能与水反应;②反应完后E中有 。
。回答下列问题:
(1)仪器a的名称为
(2)实验时,为了防止Mg与空气中氧气等反应,操作为
(3)实验测得Mg与
 反应生成MgO、
反应生成MgO、 和
和 ,其中
,其中 和
和 的物质的量相等,则C中反应的化学方程式为
的物质的量相等,则C中反应的化学方程式为(4)E装置中发生反应的离子方程式为
(5)写出氮化镁与水反应的化学方程式
(6)已知浓硝酸分解反应为:
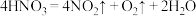 ,干燥生成的气体后,该气体混合物能使带火星的木条复燃,由此某同学得出
,干燥生成的气体后,该气体混合物能使带火星的木条复燃,由此某同学得出 气体能支持燃烧的说法,你认为该说法正确吗?并说明理由
气体能支持燃烧的说法,你认为该说法正确吗?并说明理由
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】以铁屑(表面含少量Fe2O3)为原料先制备FeC2O4•2H2O,再通过灼烧、还原制备高纯度还原铁粉的工艺流程如图:
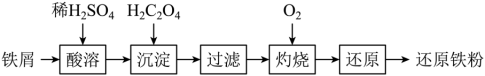
(1)酸溶。将铁屑溶于足量的稀H2SO4中过滤所得溶液经检验不含Fe3+。
①检验酸溶后的溶液是否含Fe3+的实验操作是_____ 。
②滤液中不存在Fe3+的原因是_____ 。
(2)沉淀、过滤。向酸溶后的溶液中滴加稍过量的H2C2O4(二元弱酸),过滤得FeC2O4•2H2O。
①沉淀反应的离子方程式为_____ 。
②沉淀中FeC2O4•2H2O含量的测定:准确称取6.300g沉淀,加入适量蒸馏水和稀硫酸溶解、酸化,并转移入250mL容量瓶中定容,取25.00mL溶液,向其中滴加0.1000mol•L-1KMnO4溶液,完全反应时,消耗KMnO4溶液20.00mL。过程中发生的反应为:3MnO +5FeC2O4+24H+=3Mn2++5Fe3++10CO2↑+12H2O(假设杂质不参与反应)。计算沉淀中FeC2O4•2H2O(相对分子质量为180)的质量分数
+5FeC2O4+24H+=3Mn2++5Fe3++10CO2↑+12H2O(假设杂质不参与反应)。计算沉淀中FeC2O4•2H2O(相对分子质量为180)的质量分数______ (保留四位有效数字,写出计算过程)。
(3)灼烧。在氧气流中灼烧FeC2O4•2H2O得Fe2O3、CO2。灼烧时发生反应的化学方程式为_____ 。
(4)还原。为制得高纯度的还原铁粉,以下还原剂最合适的是_____ 。
A.碳粉B.铝粉C.氢气

(1)酸溶。将铁屑溶于足量的稀H2SO4中过滤所得溶液经检验不含Fe3+。
①检验酸溶后的溶液是否含Fe3+的实验操作是
②滤液中不存在Fe3+的原因是
(2)沉淀、过滤。向酸溶后的溶液中滴加稍过量的H2C2O4(二元弱酸),过滤得FeC2O4•2H2O。
①沉淀反应的离子方程式为
②沉淀中FeC2O4•2H2O含量的测定:准确称取6.300g沉淀,加入适量蒸馏水和稀硫酸溶解、酸化,并转移入250mL容量瓶中定容,取25.00mL溶液,向其中滴加0.1000mol•L-1KMnO4溶液,完全反应时,消耗KMnO4溶液20.00mL。过程中发生的反应为:3MnO
 +5FeC2O4+24H+=3Mn2++5Fe3++10CO2↑+12H2O(假设杂质不参与反应)。计算沉淀中FeC2O4•2H2O(相对分子质量为180)的质量分数
+5FeC2O4+24H+=3Mn2++5Fe3++10CO2↑+12H2O(假设杂质不参与反应)。计算沉淀中FeC2O4•2H2O(相对分子质量为180)的质量分数(3)灼烧。在氧气流中灼烧FeC2O4•2H2O得Fe2O3、CO2。灼烧时发生反应的化学方程式为
(4)还原。为制得高纯度的还原铁粉,以下还原剂最合适的是
A.碳粉B.铝粉C.氢气
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】NaClO2是重要漂白剂和消毒剂,可用于水、砂糖、油脂的漂白杀菌。工业上NaClO2可由ClO2、H2O2和NaOH溶液混合制得。
(1)制备ClO2的部分实验装置如图所示。

①仪器a的名称是___________ 。
②该装置的作用是制备ClO2气体,该反应的离子方程式为___________ 。
(2)制备NaClO2的实验流程如下。

①吸收塔内发生反应的化学方程式为___________ 。
②吸收塔内的温度不能过高的原因为___________ 。
(3)NaClO2的应用。NaClO2具有强氧化性,可除烟气中的NO。其他条件相同时,以NaClO2溶液为吸收剂,测得相同时间内NO的氧化率随NaClO2的起始浓度的变化情况如图。
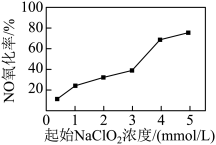
①NaClO2溶液在酸性条件下除NO的反应如下,请完成该离子方程式。___________
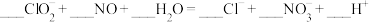
②NO的氧化率随起始NaClO2浓度的增大而增大的原因是___________ 。
(1)制备ClO2的部分实验装置如图所示。

①仪器a的名称是
②该装置的作用是制备ClO2气体,该反应的离子方程式为
(2)制备NaClO2的实验流程如下。

①吸收塔内发生反应的化学方程式为
②吸收塔内的温度不能过高的原因为
(3)NaClO2的应用。NaClO2具有强氧化性,可除烟气中的NO。其他条件相同时,以NaClO2溶液为吸收剂,测得相同时间内NO的氧化率随NaClO2的起始浓度的变化情况如图。

①NaClO2溶液在酸性条件下除NO的反应如下,请完成该离子方程式。
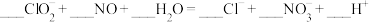
②NO的氧化率随起始NaClO2浓度的增大而增大的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】SO2是重要的化工原料,但其造成的环境问题也引起了人们的关注。开发寻找SO2的合理替代品是目前化工行业的新动态。
(1)SO2可以与水反应,反应的化学方程式为____________________________________ 。SO2是大气的主要污染物,是造成__________________ 的根源。
(2)工业上常用黄铁矿(FeS2)制备SO2,黄铁矿中S的化合价为____________ 。黄铁矿煅烧后生成1.6gFe2O3,转移的电子数为________ 。
(3)工业上使用碱液吸收SO2,使排放的尾气达到合格标准:
①将标准状况下11.2LSO2通入到2L0.5mol·L-1的氨水中,所得溶液中溶质是_________ (填化学式)。
②常温下,若用1LNaOH若用吸收0.01molSO2,完全吸收后溶液中c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3),则原NaOH溶液的pH值为________ 。
(4)连二亚硫酸钠(Na2S2O4)与SO2相似,具有极强的还原性,可用于保存水果食物。现可用如图所示方法通过吸收SO2和NO,获得Na2S2O4和NH4NO3(Ge为铈元素)

①装置II中,酸性条件下,NO被Ge4+氧化的产物主要是NO3-、NO2-,请写出生成等物质的量的NO3-和NO2-的离子方程式:_______________________________ 。
②装置III的作用之一是用质子交换膜电解槽电解使得Ge4+再生,同时在另一极生成S2O42-的电极反应式为___________________________ 。
(5)现今,科学家已研发出比SO2更安全的偏重亚硫酸盐(K2S2O5),工业上常用2KHSO3=K2S2O5+H2O的方法制备。我国要求红酒中添加K2S2O5的标准(按等硫元素质量的SO2计)为0.25g/L。今酿造500吨葡萄酒,需加入K2S2O5的质量为_______ 。(葡萄酒的密度近似为水,计算结果保留小数点后2位)
(1)SO2可以与水反应,反应的化学方程式为
(2)工业上常用黄铁矿(FeS2)制备SO2,黄铁矿中S的化合价为
(3)工业上使用碱液吸收SO2,使排放的尾气达到合格标准:
①将标准状况下11.2LSO2通入到2L0.5mol·L-1的氨水中,所得溶液中溶质是
②常温下,若用1LNaOH若用吸收0.01molSO2,完全吸收后溶液中c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3),则原NaOH溶液的pH值为
(4)连二亚硫酸钠(Na2S2O4)与SO2相似,具有极强的还原性,可用于保存水果食物。现可用如图所示方法通过吸收SO2和NO,获得Na2S2O4和NH4NO3(Ge为铈元素)

①装置II中,酸性条件下,NO被Ge4+氧化的产物主要是NO3-、NO2-,请写出生成等物质的量的NO3-和NO2-的离子方程式:
②装置III的作用之一是用质子交换膜电解槽电解使得Ge4+再生,同时在另一极生成S2O42-的电极反应式为
(5)现今,科学家已研发出比SO2更安全的偏重亚硫酸盐(K2S2O5),工业上常用2KHSO3=K2S2O5+H2O的方法制备。我国要求红酒中添加K2S2O5的标准(按等硫元素质量的SO2计)为0.25g/L。今酿造500吨葡萄酒,需加入K2S2O5的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】 (三氯化六氨合钴,
(三氯化六氨合钴,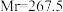 )是合成其他含钴配合物的重要原料,实验室中可由金属钴及其他原料制备
)是合成其他含钴配合物的重要原料,实验室中可由金属钴及其他原料制备 。
。
已知:①在 时,
时, 恰好完全沉淀为
恰好完全沉淀为 ;
;
②不同温度下 在水中的溶解度如图所示;
在水中的溶解度如图所示; 易潮解,Co(Ⅲ)的氧化性强于
易潮解,Co(Ⅲ)的氧化性强于 。
。
制备步骤如下:
Ⅰ. 的制备:用金属钴与氯气反应制备
的制备:用金属钴与氯气反应制备 ,实验中利用如图装置(连接处橡胶管省略)进行制备。
,实验中利用如图装置(连接处橡胶管省略)进行制备。 锥形瓶内加入
锥形瓶内加入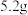 研细的
研细的 、
、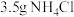 和
和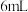 水,加热溶解后加入
水,加热溶解后加入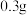 活性炭作催化剂。
活性炭作催化剂。
Ⅲ.冷却后,加入浓氨水混合均匀。控制温度在10℃以下并缓慢加入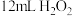 溶液。
溶液。
Ⅳ.在60℃下反应一段时间后,经过___________、过滤、洗涤、干燥等操作,得到橙黄色的 晶体
晶体 。
。
请回答下列问题:
(1)仪器a的名称为___________ 。
(2)用图中的装置组合制备 ,仪器的连接顺序为
,仪器的连接顺序为___________ 。装置B的作用是___________ 。
(3)制备三氯化六氨合钴的反应方程式为___________ 。
(4)在制备 时,加入浓氨水前,需在步骤Ⅱ中加入
时,加入浓氨水前,需在步骤Ⅱ中加入 ,请结合平衡移动原理解释原因
,请结合平衡移动原理解释原因___________ 。
(5)步骤Ⅲ中在加入 溶液时,控制温度在10℃以下缓慢加入的目的是
溶液时,控制温度在10℃以下缓慢加入的目的是___________ 。
(6)在步骤Ⅳ中过滤、洗涤、干燥之前的操作为___________ 、___________ 。
(7)制得 产品的产率为
产品的产率为___________ %(精确到0.1%)。
 (三氯化六氨合钴,
(三氯化六氨合钴,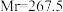 )是合成其他含钴配合物的重要原料,实验室中可由金属钴及其他原料制备
)是合成其他含钴配合物的重要原料,实验室中可由金属钴及其他原料制备 。
。已知:①在
 时,
时, 恰好完全沉淀为
恰好完全沉淀为 ;
;②不同温度下
 在水中的溶解度如图所示;
在水中的溶解度如图所示;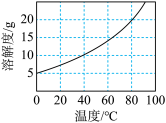
 易潮解,Co(Ⅲ)的氧化性强于
易潮解,Co(Ⅲ)的氧化性强于 。
。制备步骤如下:
Ⅰ.
 的制备:用金属钴与氯气反应制备
的制备:用金属钴与氯气反应制备 ,实验中利用如图装置(连接处橡胶管省略)进行制备。
,实验中利用如图装置(连接处橡胶管省略)进行制备。
 锥形瓶内加入
锥形瓶内加入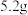 研细的
研细的 、
、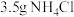 和
和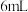 水,加热溶解后加入
水,加热溶解后加入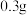 活性炭作催化剂。
活性炭作催化剂。Ⅲ.冷却后,加入浓氨水混合均匀。控制温度在10℃以下并缓慢加入
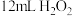 溶液。
溶液。Ⅳ.在60℃下反应一段时间后,经过___________、过滤、洗涤、干燥等操作,得到橙黄色的
 晶体
晶体 。
。请回答下列问题:
(1)仪器a的名称为
(2)用图中的装置组合制备
 ,仪器的连接顺序为
,仪器的连接顺序为(3)制备三氯化六氨合钴的反应方程式为
(4)在制备
 时,加入浓氨水前,需在步骤Ⅱ中加入
时,加入浓氨水前,需在步骤Ⅱ中加入 ,请结合平衡移动原理解释原因
,请结合平衡移动原理解释原因(5)步骤Ⅲ中在加入
 溶液时,控制温度在10℃以下缓慢加入的目的是
溶液时,控制温度在10℃以下缓慢加入的目的是(6)在步骤Ⅳ中过滤、洗涤、干燥之前的操作为
(7)制得
 产品的产率为
产品的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下图:
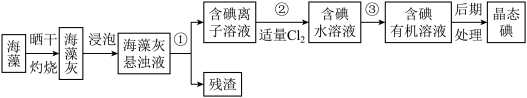
(1)指出提取碘的过程中有关的实验操作名称:①_________ ;③__________
(2)提取碘的过程中,可选择的有机试剂是:___________
A.酒精 B.四氯化碳 C.苯
(3)实验操作③中,实验室已有烧杯、玻璃棒以及必要的夹持仪器,尚缺少的玻璃仪器是__________ 。
(4)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,指出实验装置图中的错误之处:
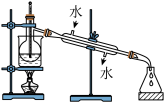
①____ ;②_________ ;③__________ 。
(5)最后晶态碘在_____________ 里聚集(填仪器名称)。

(1)指出提取碘的过程中有关的实验操作名称:①
(2)提取碘的过程中,可选择的有机试剂是:
A.酒精 B.四氯化碳 C.苯
(3)实验操作③中,实验室已有烧杯、玻璃棒以及必要的夹持仪器,尚缺少的玻璃仪器是
(4)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,指出实验装置图中的错误之处:

①
(5)最后晶态碘在
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】二氧化铈 是一种重要的稀土氧化物,平板电视显示屏生产过程中产生大量的废玻璃粉末(含
是一种重要的稀土氧化物,平板电视显示屏生产过程中产生大量的废玻璃粉末(含 、
、 、
、 、FeO等物质).某课题组以此粉末为原料,设计如图工艺流程对资源进行回收,得到纯净的
、FeO等物质).某课题组以此粉末为原料,设计如图工艺流程对资源进行回收,得到纯净的 和硫酸亚铁铵晶体。
和硫酸亚铁铵晶体。
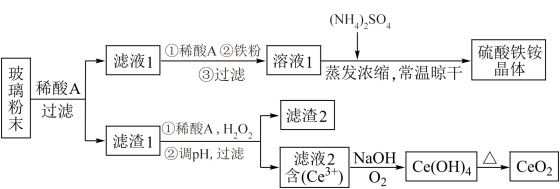
已知: 不溶于稀硫酸,也不溶于NaOH溶液。
不溶于稀硫酸,也不溶于NaOH溶液。
(1)稀酸A是_______ ,滤液1中加入铁粉的目的是_______ 。
(2)设计实验证明滤液1中含有 :
:_______ 。
(3)由滤渣1生成 的化学方程式为
的化学方程式为_______ 。
(4)由滤液2生成 的离子方程式为
的离子方程式为_______ 。
(5)硫酸铁铵晶体 广泛用于水的净化处理,但其在去除酸性废水中的悬浮物时效率降低,其原因是
广泛用于水的净化处理,但其在去除酸性废水中的悬浮物时效率降低,其原因是_______ 。
 是一种重要的稀土氧化物,平板电视显示屏生产过程中产生大量的废玻璃粉末(含
是一种重要的稀土氧化物,平板电视显示屏生产过程中产生大量的废玻璃粉末(含 、
、 、
、 、FeO等物质).某课题组以此粉末为原料,设计如图工艺流程对资源进行回收,得到纯净的
、FeO等物质).某课题组以此粉末为原料,设计如图工艺流程对资源进行回收,得到纯净的 和硫酸亚铁铵晶体。
和硫酸亚铁铵晶体。
已知:
 不溶于稀硫酸,也不溶于NaOH溶液。
不溶于稀硫酸,也不溶于NaOH溶液。(1)稀酸A是
(2)设计实验证明滤液1中含有
 :
:(3)由滤渣1生成
 的化学方程式为
的化学方程式为(4)由滤液2生成
 的离子方程式为
的离子方程式为(5)硫酸铁铵晶体
 广泛用于水的净化处理,但其在去除酸性废水中的悬浮物时效率降低,其原因是
广泛用于水的净化处理,但其在去除酸性废水中的悬浮物时效率降低,其原因是
您最近一年使用:0次

 )
)

