无水 是一种常用的还原剂和媒染剂,广泛用于织物印染。实验室用
是一种常用的还原剂和媒染剂,广泛用于织物印染。实验室用 还原无水氯化铁制备。
还原无水氯化铁制备。
(1)实验室利用如下装置制取干燥纯净的 。
。
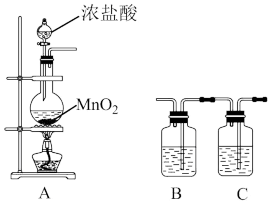
①装置A中盛放浓盐酸的仪器名称是___________ ;装置A中发生反应的离子方程式为___________ 。
②装置B中盛放的试剂为___________ (填试剂名称)。
(2)制取无水氯化铁(已知无水氯化铁易潮解,100℃以上升华)。
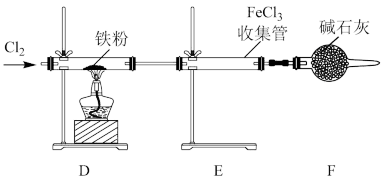
①实验过程中需用热源间歇性微热装置D和E处的连接管,其目的是___________ 。
②装置F的作用___________ 。
(3)取反应后(2)中装置E和F,用氢气还原氯化铁,制备无水氯化亚铁。

①通氢气前需先通入一段时间氮气,其目的是___________ 。
②E中装置未检验到铁单质,检测装置E管中反应产物,测得 ,则产物中
,则产物中 的物质的量分数为
的物质的量分数为___________ %。
 是一种常用的还原剂和媒染剂,广泛用于织物印染。实验室用
是一种常用的还原剂和媒染剂,广泛用于织物印染。实验室用 还原无水氯化铁制备。
还原无水氯化铁制备。(1)实验室利用如下装置制取干燥纯净的
 。
。
①装置A中盛放浓盐酸的仪器名称是
②装置B中盛放的试剂为
(2)制取无水氯化铁(已知无水氯化铁易潮解,100℃以上升华)。

①实验过程中需用热源间歇性微热装置D和E处的连接管,其目的是
②装置F的作用
(3)取反应后(2)中装置E和F,用氢气还原氯化铁,制备无水氯化亚铁。

①通氢气前需先通入一段时间氮气,其目的是
②E中装置未检验到铁单质,检测装置E管中反应产物,测得
 ,则产物中
,则产物中 的物质的量分数为
的物质的量分数为
更新时间:2021-11-21 22:30:56
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学兴趣小组设计了如图装置,该装置能制取Cl2,并进行相关性质实验,且可利用装置G储存多余的氯气。
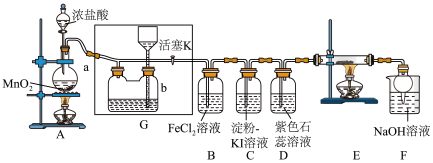
(1)A中发生反应的化学方程式为_______ 。
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯。回答下列问题:
①在装置D中能看到的实验现象是_______ 。
②在装置E的硬质玻璃管内盛有炭粉,发生氧化还原反应,产物为CO2和HCl,则E中发生反应的化学方程式为_______ 。
③装置F中球形干燥管的作用是_______ 。
(3)储气瓶b内盛放的试剂是_______ 。
(4)装置B中FeCl2被Cl2氧化,反应的化学方程式为_______ 。

(1)A中发生反应的化学方程式为
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯。回答下列问题:
①在装置D中能看到的实验现象是
②在装置E的硬质玻璃管内盛有炭粉,发生氧化还原反应,产物为CO2和HCl,则E中发生反应的化学方程式为
③装置F中球形干燥管的作用是
(3)储气瓶b内盛放的试剂是
(4)装置B中FeCl2被Cl2氧化,反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上,向500~600℃的铁屑中通入氯气生产无水氯化铁。现用如图所示的装置模拟上述过程进行实验。
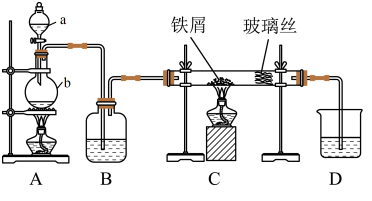
(1)写出仪器的名称:a_______________ ,b___________________ 。
(2)A中反应的化学方程式为____________ 。
(3)装置B中加入的试剂是_____________ 。
(4)已知:向热铁屑中通入氯化氢气体可以生产无水氯化亚铁。为防止有杂质FeCl2生成,可在装置______ 和 ________ (填字母)间增加一个盛有________ 的洗气瓶。
(5)装置D的作用是___________________ 。为防止水蒸气影响无水氯化铁的制取,请你提出一个对装置D的改进方案:___________ 。

(1)写出仪器的名称:a
(2)A中反应的化学方程式为
(3)装置B中加入的试剂是
(4)已知:向热铁屑中通入氯化氢气体可以生产无水氯化亚铁。为防止有杂质FeCl2生成,可在装置
(5)装置D的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】用如图装置(气密性好)探究 与
与 的反应。
的反应。
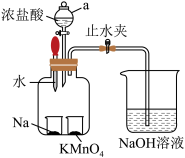
实验步骤:
①将一定量浓盐酸滴在 粉末上,立即产生黄绿色气体。
粉末上,立即产生黄绿色气体。
②待黄绿色气体均匀充满集气瓶时,关闭止水夹。
③再向钠粒上滴2滴水,片刻后钠燃烧,产生白烟,白色固体附着在集气瓶内壁上。
回答下列问题:
(1)仪器a的名称为_______ 。
(2)步骤①,黄绿色气体是 ,则
,则 的作用是
的作用是_______ (填“氧化剂”或“还原剂”)。
(3)实验室制备 的方程式为
的方程式为_______ ,用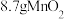 与足量的浓盐酸充分反应,生成
与足量的浓盐酸充分反应,生成 的体积为
的体积为_______ L(标准状况下)。
(4)钠粒与2滴水反应的化学方程式为_______ ,引起钠燃烧的原因是_______ 。
(5)写出生成白色固体的电子式:_______ 。
(6)右侧烧杯中发生反应的离子方程式为_______ 。
 与
与 的反应。
的反应。
实验步骤:
①将一定量浓盐酸滴在
 粉末上,立即产生黄绿色气体。
粉末上,立即产生黄绿色气体。②待黄绿色气体均匀充满集气瓶时,关闭止水夹。
③再向钠粒上滴2滴水,片刻后钠燃烧,产生白烟,白色固体附着在集气瓶内壁上。
回答下列问题:
(1)仪器a的名称为
(2)步骤①,黄绿色气体是
 ,则
,则 的作用是
的作用是(3)实验室制备
 的方程式为
的方程式为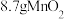 与足量的浓盐酸充分反应,生成
与足量的浓盐酸充分反应,生成 的体积为
的体积为(4)钠粒与2滴水反应的化学方程式为
(5)写出生成白色固体的电子式:
(6)右侧烧杯中发生反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】如图为实验室制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条;F中装有铁粉,其右端出气管口放有脱脂棉。

(1)仪器A的名称为_______ 。写出装置B中的化学反应方程式:_______ 。
(2)装置C中盛装的试剂是_______ ,D中试剂是_______ ,写出F中反应的化学反应方程式:_______ 。
(3)H中的试剂为氢氧化钠溶液,其作用是吸收多余的 ,防止污染空气,写出H中的反应的离子方程式
,防止污染空气,写出H中的反应的离子方程式_______ 。

(1)仪器A的名称为
(2)装置C中盛装的试剂是
(3)H中的试剂为氢氧化钠溶液,其作用是吸收多余的
 ,防止污染空气,写出H中的反应的离子方程式
,防止污染空气,写出H中的反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组同学为验证氯气的性质并制备少量干燥的氯化铁,设计并进行如图实验:
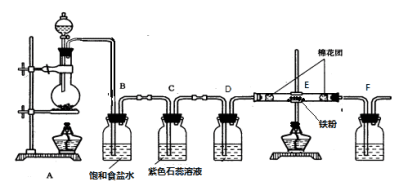
回答下列问题:
(1)写出A中制取氯气的化学方程式___ 。
(2)B装置的作用是___ 。
(3)实验时C中可观察到的现象是___ ,氯气与水发生反应的离子方程式是___ 。
(4)D瓶盛放的试剂是___ 。
(5)F瓶溶液的作用是___ ,写出发生反应的离子方程式___ 。

回答下列问题:
(1)写出A中制取氯气的化学方程式
(2)B装置的作用是
(3)实验时C中可观察到的现象是
(4)D瓶盛放的试剂是
(5)F瓶溶液的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】CuCl2、CuCl广泛用于有机合成的催化剂。CuCl2容易潮解; CuCl白色粉末,微溶于水,溶于浓盐酸和氨水生成络合物,不溶于乙醇。
已知:
i.CuCl2+Cu+2HCl(浓) 2H[CuCl2](无色)
2H[CuCl2](无色) 2CuCl↓(白色)+2HCl
2CuCl↓(白色)+2HCl
ii.副反应:CuCl+H2O CuOH+2HCl;CuCl+Cl-=[CuCl2]-
CuOH+2HCl;CuCl+Cl-=[CuCl2]-
(1)制取CuCl2装置如下:
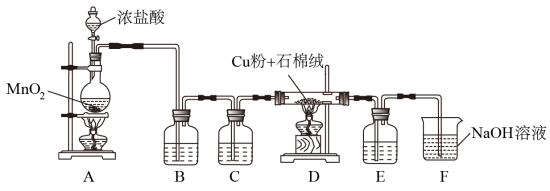
①A装置中发生反应的离子方程式是_________ 。
②C、E 装置中盛放的是浓硫酸,作用是_________ 。
③B中选择饱和食盐水而不用蒸馏水的原因是_________ 。
(2)制取CuCl流程如下:
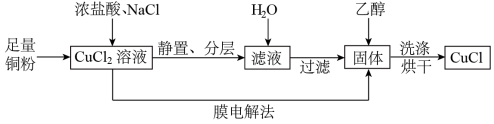
①反应①中加入NaCl的目的是_________ ;但是Cl—浓度过高,CuCl产率降低,原因是________________ 。
②CuCl在潮湿的环境中易被氧化为Cu2(OH)3Cl,反应的方程式为________________ 。
③利用膜电解法制取CuCl,阴极电极反应式为________________ 。
④用乙醇洗涤沉淀Y的原因为________________ 。
已知:
i.CuCl2+Cu+2HCl(浓)
 2H[CuCl2](无色)
2H[CuCl2](无色) 2CuCl↓(白色)+2HCl
2CuCl↓(白色)+2HClii.副反应:CuCl+H2O
 CuOH+2HCl;CuCl+Cl-=[CuCl2]-
CuOH+2HCl;CuCl+Cl-=[CuCl2]-(1)制取CuCl2装置如下:

①A装置中发生反应的离子方程式是
②C、E 装置中盛放的是浓硫酸,作用是
③B中选择饱和食盐水而不用蒸馏水的原因是
(2)制取CuCl流程如下:

①反应①中加入NaCl的目的是
②CuCl在潮湿的环境中易被氧化为Cu2(OH)3Cl,反应的方程式为
③利用膜电解法制取CuCl,阴极电极反应式为
④用乙醇洗涤沉淀Y的原因为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】叠氮化钠(NaN3)不溶于乙醚,微溶于乙醇,易溶于水,常用于汽车安全防护袋的气源,汽车发生剧烈碰撞时,立即自动充气。实验室模拟尿素法制备水合肼(N2H4•H2O)并利用其进一步反应制取NaN3的流程如图:
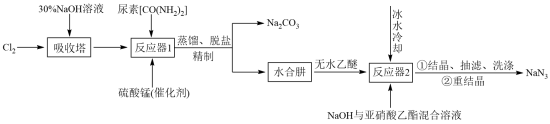
已知:①N2H4•H2O易溶于水,具有强还原性,易被氧化成N2;
②一定条件下,碱性NaClO溶液与尿素溶液反应生成N2H4•H2O。
回答下列问题:
(1)吸收塔内发生反应的离子方程式为____ 。
(2)写出反应器1中生成水合肼反应的化学方程式:_____ 。
(3)反应器2中加入无水乙醚的作用是____ 。
(4)已知亚硝酸乙酯的结构简式为CH3CH2ONO,写出反应器2中生成NaN3和CH3CH2OH的化学方程式:____ 。若生成39gNaN3,则该反应中转移电子的物质的量为____ 。

已知:①N2H4•H2O易溶于水,具有强还原性,易被氧化成N2;
②一定条件下,碱性NaClO溶液与尿素溶液反应生成N2H4•H2O。
回答下列问题:
(1)吸收塔内发生反应的离子方程式为
(2)写出反应器1中生成水合肼反应的化学方程式:
(3)反应器2中加入无水乙醚的作用是
(4)已知亚硝酸乙酯的结构简式为CH3CH2ONO,写出反应器2中生成NaN3和CH3CH2OH的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、D、E、F为短周期元素,非金属元素 A 最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的 2 倍。 B在 D中充分燃烧能生成其最高价化合物 BD2。E+与D2-具有相同的电子数。 A 在 F中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)A在周期表中的位置是____________ ,写出单质 F和NaOH的离子方程式____________ 。
(2)B、D、E 组成的一种盐中, E的质量分数为43%,其俗名为________ ,其水溶液与等物质的量的 F单质反应的化学方程式为___________________ ;
(3)由这些元素组成的物质,其组成和结构信息如下表:
a的化学式为_______ ;b与水反应的化学方程式为_______ ;
(1)A在周期表中的位置是
(2)B、D、E 组成的一种盐中, E的质量分数为43%,其俗名为
(3)由这些元素组成的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1:1 |
| c | 化学组成为 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】在下列各变化中,反应①为常温下的反应,A、C、D均含氯元素,且A中氯元素的化合价介于C与D之间,E常温下为无色无味的液体,F为淡黄色粉末,G为常见的无色气体。


回答下列问题:
(1)A、G的化学式分别为_____ 、_____ 。
(2)写出反应①的化学方程式_____ 。
(3)在反应②中,每生成2.24L气体G(标准状况)时,消耗F_____ g。
(4)A与石灰乳反应制得的漂白粉的有效成分是_____ (填化学式),该物质在空气中失效的原因是_____ (用化学方程式表示)。


回答下列问题:
(1)A、G的化学式分别为
(2)写出反应①的化学方程式
(3)在反应②中,每生成2.24L气体G(标准状况)时,消耗F
(4)A与石灰乳反应制得的漂白粉的有效成分是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】MnO2是一种重要的无机功能材料,粗MnO2的提纯是工业生产的重要环节。某研究性学习小组设计了将粗MnO2(含有较多的MnO和MnCO3)样品转化为纯MnO2的实验,其流程如下:

(1)第①步加稀H2SO4时,粗MnO2样品中的________ (写化学式)转化为可溶性物质。
(2)第②步反应的离子方程式:___________________________________ 。
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、______ 、______ 、______ ,已知蒸发得到的固体中有NaClO3和NaOH,则一定还有含有________ (写化学式)。
(4)若粗MnO2样品的质量为12.69g,第①步反应后,经过滤得到8.7g MnO2,并收集到0.224LCO2(标准状况下),则在第②步反应中至少需要___ molNaClO3。

(1)第①步加稀H2SO4时,粗MnO2样品中的
(2)第②步反应的离子方程式:
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、
(4)若粗MnO2样品的质量为12.69g,第①步反应后,经过滤得到8.7g MnO2,并收集到0.224LCO2(标准状况下),则在第②步反应中至少需要
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】溴化锂是一种高效的水汽吸收剂,其一种绿色工业合成工艺如下(部分操作和条件已略去)。

已知:碳酸锂微溶于水,水溶液显碱性。
(1)Br2的电子式是______ 。
(2)合成过程中发生的反应如下,请写出ii反应的化学方程式并将iii补充完整。
ⅰ. Br2 +H2O HBr +HBrO;
HBr +HBrO;
ⅱ._____ ;
ⅲ. 3LiBrO + CO(NH2)2(尿素)=3LiBr+_____ 。
(3)LiBrO3是生产过程中的副产物。
①用化学方程式表示生成改副产物的原因:______ 。
②为了提高原料的利用率,减少副产物的生成,必须调控体系的pH在3~5之间,通过合理的加料方法来实现:将碳酸锂粉末溶解于冷的溴水中至饱和,并一次性加入尿素,然后再______ ,直到尿素完全转化。
③常用硫脲除去LiBrO3,反应的化学方程式是4LiBrO3 +3CS(NH2)2(硫脲) +3H2O=4LiBr +3CO(NH2)2 +3H2SO4 ,选用硫脲除杂的优点是_______ ;缺点是引入新杂质且溶液酸性增强,为解决该问题需要加入的试剂是_______ 。

已知:碳酸锂微溶于水,水溶液显碱性。
(1)Br2的电子式是
(2)合成过程中发生的反应如下,请写出ii反应的化学方程式并将iii补充完整。
ⅰ. Br2 +H2O
 HBr +HBrO;
HBr +HBrO;ⅱ.
ⅲ. 3LiBrO + CO(NH2)2(尿素)=3LiBr+
(3)LiBrO3是生产过程中的副产物。
①用化学方程式表示生成改副产物的原因:
②为了提高原料的利用率,减少副产物的生成,必须调控体系的pH在3~5之间,通过合理的加料方法来实现:将碳酸锂粉末溶解于冷的溴水中至饱和,并一次性加入尿素,然后再
③常用硫脲除去LiBrO3,反应的化学方程式是4LiBrO3 +3CS(NH2)2(硫脲) +3H2O=4LiBr +3CO(NH2)2 +3H2SO4 ,选用硫脲除杂的优点是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】以硅藻土为载体的五氧化二钒(V2O5)是接触法生产硫酸的催化剂。从废矾催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为
以下是一种废钒催化剂回收工艺路线:
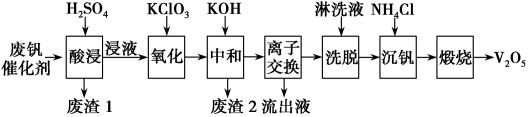
回答下列问题:
(1)“酸浸”时V2O5转化为VO ,反应的离子方程式为
,反应的离子方程式为___________ ,同时V2O4转化成VO2+。
(2)“氧化”中欲使3 mol的VO2+变为VO ,则需要氧化剂KClO3至少为
,则需要氧化剂KClO3至少为___________ mol。
(3)“中和”作用之一是使钒以V4O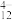 形式存在于溶液中,将Al和Fe元素转化为难溶物。“废渣2”中含有
形式存在于溶液中,将Al和Fe元素转化为难溶物。“废渣2”中含有___________ 。
(4)“离子交换”和“洗脱”可简单表示为4ROH+V4O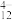
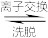 R4V4O12+4OH-(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈
R4V4O12+4OH-(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈___________ 性(填“酸”、“碱”或“中”)。
(5)“流出液”中阳离子最多的是___________ 。
(6)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式___________ 。
| 物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
| 质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:

回答下列问题:
(1)“酸浸”时V2O5转化为VO
 ,反应的离子方程式为
,反应的离子方程式为(2)“氧化”中欲使3 mol的VO2+变为VO
 ,则需要氧化剂KClO3至少为
,则需要氧化剂KClO3至少为(3)“中和”作用之一是使钒以V4O
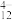 形式存在于溶液中,将Al和Fe元素转化为难溶物。“废渣2”中含有
形式存在于溶液中,将Al和Fe元素转化为难溶物。“废渣2”中含有(4)“离子交换”和“洗脱”可简单表示为4ROH+V4O
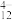
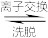 R4V4O12+4OH-(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈
R4V4O12+4OH-(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈(5)“流出液”中阳离子最多的是
(6)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式
您最近一年使用:0次



