铜和钴掺杂的含氮碳层材料是一种新型催化材料,具有氧还原催化性能。回答下列问题:
(1)下列状态的N原子或离子的核外电子在跃迁时,用光谱仪可捕捉到发射光谱的是_____(填序号)。
(2)已知氮的两种化合物N2H4和NH2OH都能结合H+而具有弱碱性,二者的碱性强弱:N2H4_____ NH2OH(填“强于”或“弱于”),理由是___ 。
(3)叠氮酸根N 的空间结构是
的空间结构是______ ,NO 中含有的价层电子对数目为
中含有的价层电子对数目为______ 。
(4)Co的第四电离能比铁的第四电离能______ (填“大”或“小”),理由是____ 。
(5)高导电紫铜常用硼化钙提高导电率,其晶胞如图所示,具有立方晶系的对称性,B原子全部组成正八面体,各个顶点通过B—B键连接成三维骨架,则该硼化钙的化学式是___________ ,B原子半径为r nm,阿伏加德罗常数的值为NA,则硼化钙的密度 为
为___________ g·cm-3。

(1)下列状态的N原子或离子的核外电子在跃迁时,用光谱仪可捕捉到发射光谱的是_____(填序号)。
| A.1s22s22p3 | B.1s22s2 | C.1s22s12p4 | D.1s22s22p6 |
(3)叠氮酸根N
 的空间结构是
的空间结构是 中含有的价层电子对数目为
中含有的价层电子对数目为(4)Co的第四电离能比铁的第四电离能
(5)高导电紫铜常用硼化钙提高导电率,其晶胞如图所示,具有立方晶系的对称性,B原子全部组成正八面体,各个顶点通过B—B键连接成三维骨架,则该硼化钙的化学式是
 为
为
21-22高三上·山东潍坊·阶段练习 查看更多[2]
更新时间:2021-12-21 20:28:51
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】寿山石被称为中华瑰宝,是中国传统四大印章石之一,其石质晶莹,脂润、色彩斑斓。色泽浑然天成。它主要由酸性火山凝灰岩经热液蚀变而成,化学式为 。回答下列问题:
。回答下列问题:
(1)下列状态的氧中,再失去一个电子所需要的能量最多的是_______(填字母)。
(2)硅可形成一系列硅氢化合物,但最长硅链长度远不及烃中碳链长度,原因是_______ , ……则该同系物中,含有n个硅原子的分子中,σ键数目为
……则该同系物中,含有n个硅原子的分子中,σ键数目为_______ (用含n的式子表示)。
(3)在硅酸盐中, 四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式,图(b)为一种无限长单链结构单元的多硅酸根,其中Si原子的杂化形式为
四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式,图(b)为一种无限长单链结构单元的多硅酸根,其中Si原子的杂化形式为_______ ,化学式为_______ 。

(4) 具有强还原性,其晶胞结构如图所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,则
具有强还原性,其晶胞结构如图所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,则 的空间构型为
的空间构型为_______ ,①处的原子分数坐标是_______ ,用 表示阿伏加德罗常数,则
表示阿伏加德罗常数,则 晶体密度为
晶体密度为_______  。
。

 。回答下列问题:
。回答下列问题:(1)下列状态的氧中,再失去一个电子所需要的能量最多的是_______(填字母)。
A. | B. | C. | D. |
 ……则该同系物中,含有n个硅原子的分子中,σ键数目为
……则该同系物中,含有n个硅原子的分子中,σ键数目为(3)在硅酸盐中,
 四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式,图(b)为一种无限长单链结构单元的多硅酸根,其中Si原子的杂化形式为
四面体[如下图(a)]通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式,图(b)为一种无限长单链结构单元的多硅酸根,其中Si原子的杂化形式为
(4)
 具有强还原性,其晶胞结构如图所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,则
具有强还原性,其晶胞结构如图所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,则 的空间构型为
的空间构型为 表示阿伏加德罗常数,则
表示阿伏加德罗常数,则 晶体密度为
晶体密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】A、B、C、D、E代表五种常见元素,它们的核电荷数依次增大。其中元素E的基态3d轨道上有2个电子,A的基态原子中有2个未成对电子,B是地壳中含量最多的元素,C是短周期中最活泼的金属元素,D与C可形成CD型离子化合物。请回答下列问题:
(1)E的基态原子价层电子排布式为_______ 。
(2)A、B及周期表中与A、B均紧邻的元素的第一电离能由大到小的顺序为_______ (用元素符号表示)。
(3)AB2分子中,A的杂化类型是_____ ;1个AB2分子中,含有______ 个π键;与AB2互为等电子体的分子有______ (写一种,下同),离子有_______ 。
(4)AB2形成的晶体的熔点______ (填“高于”、“低于”或“无法判断”)CD形成的晶体的熔点,原因是________ 。
(5)由化合物CD组成的晶体中,阴、阳离子都具有或近似具有球形对称结构,它们都可以看作刚性圆球,并彼此“相切”。如图所示为C、D形成化合物的晶胞结构图以及晶胞的剖面图:
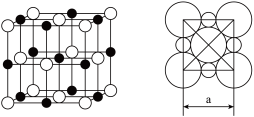
在该晶体中阴离子的配位数为______ ;若a=5.6×10−10 m,则该晶体的密度为______ g·cm−3(精确到小数点后1位)。
(1)E的基态原子价层电子排布式为
(2)A、B及周期表中与A、B均紧邻的元素的第一电离能由大到小的顺序为
(3)AB2分子中,A的杂化类型是
(4)AB2形成的晶体的熔点
(5)由化合物CD组成的晶体中,阴、阳离子都具有或近似具有球形对称结构,它们都可以看作刚性圆球,并彼此“相切”。如图所示为C、D形成化合物的晶胞结构图以及晶胞的剖面图:

在该晶体中阴离子的配位数为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】 是生物医药、太阳能电池等领域的理想荧光材料。回答下列问题:
是生物医药、太阳能电池等领域的理想荧光材料。回答下列问题:
(1)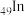 的价层电子排布式为
的价层电子排布式为_______ 。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋量子数,对于基态S原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋量子数,对于基态S原子,其价电子自旋磁量子数的代数和为_______ 。S可以形成两种常见含氧酸,其通式为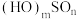 ,解释
,解释 酸性更强的原因
酸性更强的原因_______ 。
(3)矾土含 ,《诗经》言“缟衣茹藘(茜草)”,茜草中的茜素与矾土中的
,《诗经》言“缟衣茹藘(茜草)”,茜草中的茜素与矾土中的 、
、 生成的红色配合物X是最早的媒染染料。
生成的红色配合物X是最早的媒染染料。_______ 。
②X中C的杂化轨道类型是_______ ,X中不存在的作用力有_______ (填标号)。
A.配位键 B.离子键 C.共价键 D.氢键 F.范德华力
③茜素水溶性较好的原因是_______ 。
(4) (相对分子质量为Mr)的晶胞结构如图a所示,阿伏加德罗常数为
(相对分子质量为Mr)的晶胞结构如图a所示,阿伏加德罗常数为 ,则
,则 晶体的密度为
晶体的密度为_______  (列计算式),图b为Cu原子沿z轴方向向x-y平面投影的位置,在图b中画出S原子在该方向的投影位置
(列计算式),图b为Cu原子沿z轴方向向x-y平面投影的位置,在图b中画出S原子在该方向的投影位置_______ (用“ ”表示S原子)。
”表示S原子)。
 是生物医药、太阳能电池等领域的理想荧光材料。回答下列问题:
是生物医药、太阳能电池等领域的理想荧光材料。回答下列问题:(1)
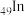 的价层电子排布式为
的价层电子排布式为(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋量子数,对于基态S原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋量子数,对于基态S原子,其价电子自旋磁量子数的代数和为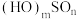 ,解释
,解释 酸性更强的原因
酸性更强的原因(3)矾土含
 ,《诗经》言“缟衣茹藘(茜草)”,茜草中的茜素与矾土中的
,《诗经》言“缟衣茹藘(茜草)”,茜草中的茜素与矾土中的 、
、 生成的红色配合物X是最早的媒染染料。
生成的红色配合物X是最早的媒染染料。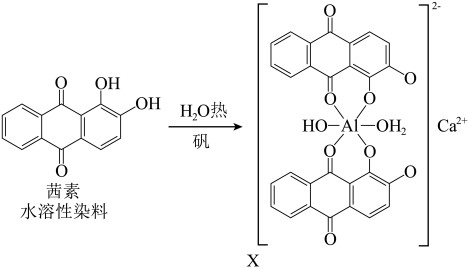
②X中C的杂化轨道类型是
A.配位键 B.离子键 C.共价键 D.氢键 F.范德华力
③茜素水溶性较好的原因是
(4)
 (相对分子质量为Mr)的晶胞结构如图a所示,阿伏加德罗常数为
(相对分子质量为Mr)的晶胞结构如图a所示,阿伏加德罗常数为 ,则
,则 晶体的密度为
晶体的密度为 (列计算式),图b为Cu原子沿z轴方向向x-y平面投影的位置,在图b中画出S原子在该方向的投影位置
(列计算式),图b为Cu原子沿z轴方向向x-y平面投影的位置,在图b中画出S原子在该方向的投影位置 ”表示S原子)。
”表示S原子)。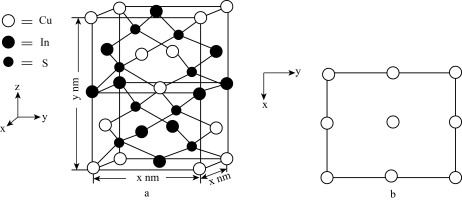
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】锰的氧化物主要有一氧化锰(MnO)、二氧化锰(MnO2)、三氧化二锰(Mn2O3)、四氧化三锰(Mn3O4)、亚锰酸酐( Mn2O5)、锰酸酐( MnO3 )和高锰酸酐(Mn2O7)。回答下列问题:
(1)基态Mn原子的核外电子排布式是___________ 。
(2)下列锰元素的不同微粒中,电离最外层一个电子所需能量最大的是___________(填编号)。
(3)以MnSO4为原料,六次甲基四胺为弱碱介质,通过水解氧化法可制备不同粒径的磁性纳米Mn3O4。
① 的空间构型是
的空间构型是___________ ,写出两种与 互为等电子体的离子
互为等电子体的离子_____ 。
②六次甲基四胺也称乌洛托品(结构如图甲所示),其所含元素的电负性从大到小的顺序是___________ ,中心原子N的杂化方式是___________ ,N原子数与σ键数目之比为___________ 。

(4)实验室可利用硝酸锰受热分解的方式制备锰的一种氧化物(晶胞结构如图乙所示)和NO2。

①该锰的氧化物中Mn的化合价为___________ 。
②请画出z方向投影图_____ 。
③已知Mn和O的离子半径分别是mpm和npm,则该晶体的空间利用率为___________ ; (列出计算式即可)。
(1)基态Mn原子的核外电子排布式是
(2)下列锰元素的不同微粒中,电离最外层一个电子所需能量最大的是___________(填编号)。
A.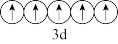 | B.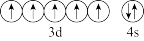 |
C.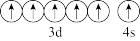 | D.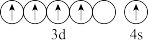 |
①
 的空间构型是
的空间构型是 互为等电子体的离子
互为等电子体的离子②六次甲基四胺也称乌洛托品(结构如图甲所示),其所含元素的电负性从大到小的顺序是

(4)实验室可利用硝酸锰受热分解的方式制备锰的一种氧化物(晶胞结构如图乙所示)和NO2。

①该锰的氧化物中Mn的化合价为
②请画出z方向投影图
③已知Mn和O的离子半径分别是mpm和npm,则该晶体的空间利用率为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】硼的无机化学问题比周期表里任何一种元素都更复杂和变化多端。
(1)基态B原子的价电子轨道表达式为__ ,第二周期第一电离能比B高的元素有__ 种。
(2)B易形成配离子,如[B(OH)4]-、[BH4]-等。[B(OH)4]-的结构式为__ (标出配位键),其中心原子的VSEPR模型名称为__ ,写出[BH4]-的两种等电子体__ 。
(3)图1表示偏硼酸根的一种无限长的链式结构,其化学式可表示为__ (以n表示硼原子的个数),图2表示的是一种五硼酸根离子,其中B原子的杂化方式为__ 。
(4)硼酸晶体是片层结构,图3表示的是其中一层的结构。同一层微粒间存在的作用力有__ 。
(5)1892年,化学家已用Mg还原B2O3制得硼单质。Mg属六方最密堆积,其晶胞结构如图4所示,若在晶胞中建立如图5所示的坐标系,以A为坐标原点,把晶胞的底边边长和高都视作单位1,则B、E、C的坐标分别为B(1,0,0)、E(0,1,0)、C(0,0,1),请写出D点的坐标:D:___ 。

(1)基态B原子的价电子轨道表达式为
(2)B易形成配离子,如[B(OH)4]-、[BH4]-等。[B(OH)4]-的结构式为
(3)图1表示偏硼酸根的一种无限长的链式结构,其化学式可表示为
| 图1 | 图2 | 图3 |
 |  |  |
(4)硼酸晶体是片层结构,图3表示的是其中一层的结构。同一层微粒间存在的作用力有
(5)1892年,化学家已用Mg还原B2O3制得硼单质。Mg属六方最密堆积,其晶胞结构如图4所示,若在晶胞中建立如图5所示的坐标系,以A为坐标原点,把晶胞的底边边长和高都视作单位1,则B、E、C的坐标分别为B(1,0,0)、E(0,1,0)、C(0,0,1),请写出D点的坐标:D:

您最近一年使用:0次
【推荐3】硼(B)及其化合物在化学中有重要的地位。请回答下列问题:
(1)硼酸(H3BO3)是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
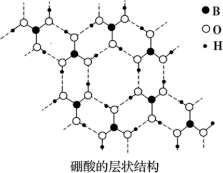
①硼酸中B原子的杂化轨道类型为_______ 。
②硼酸晶体中存在的作用力有范德华力和_______ 。
③加热时,硼酸的溶解度增大,主要原因是_______ 。
④硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的OH-而呈酸性。写出硼酸的电离方程式:_______ 。
(2)硼氢化钠(NaBH4)是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理:_______ 。[BH4]-的空间构型是_______ 。
(3)B3N3H6可用来制造具有耐油、耐高温性能的特殊材料。写出它的一种等电子体物质的分子式:_______ 。
(4)硼化镁晶体在39 K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,如图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为_______ 。

(5)金刚石的晶胞如图。立方氮化硼的结构与金刚石相似,已知晶胞边长为361.5 pm,则立方氮化硼的密度是_______ g· cm-3(只要求列算式,不必计算出数值,阿伏加德罗常数用NA表示)。
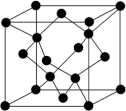
(1)硼酸(H3BO3)是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。

①硼酸中B原子的杂化轨道类型为
②硼酸晶体中存在的作用力有范德华力和
③加热时,硼酸的溶解度增大,主要原因是
④硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的OH-而呈酸性。写出硼酸的电离方程式:
(2)硼氢化钠(NaBH4)是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理:
(3)B3N3H6可用来制造具有耐油、耐高温性能的特殊材料。写出它的一种等电子体物质的分子式:
(4)硼化镁晶体在39 K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,如图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为

(5)金刚石的晶胞如图。立方氮化硼的结构与金刚石相似,已知晶胞边长为361.5 pm,则立方氮化硼的密度是

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】金属簇合物是含有金属-金属键、具有精确组成的一类物质,常表现出优美的化学结构和独特的光物理性能。
图6-1-a示出一种电中性银硫簇(简记为Ag12S6)的结构,包含12个银原子和6个硫原子(图中未区分原子大小)。6个银原子位于同一平面(称为赤道面),形成正六边形,彼此之间不成键。赤道面上、下方各有3个银原子,皆呈正三角形排布,彼此之间形成Ag-Ag键,并分别与赤道面。上的两个银原子形成Ag-Ag键。6个硫原子的位置如图所示。

(1)计算Ag12S6中Ag-Ag键的个数________ 。
(2)计算Ag12S6中三角形面的个数___________ 。
(3)Ag12S6的硫原子来自于叔丁巯基,银为正一价。在Ag12S6上还连接有若干个CF3COO-,计算CF3COO-的个数__________ 。
(4)聚集诱导发光(AIE)现象是一种由中国科学家首先发现的光致发光现象。具有AIE特性的有机分子在聚集状态下表现出远强于分散状态的光致发光性能。四苯乙烯(TPE)是一种典型的AIE分子。将TPE完全溶解于乙醇中,分别取等量的该溶液加入到等体积的水和甲苯中,判断哪一个体系的光致发光较强并简要解释原因__________ 。
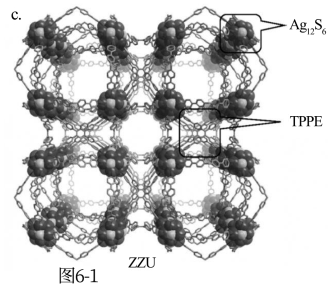
(5)利用上述Ag12S6和图6-1-b所示的TPPE配体组装,得到一种晶体框架材料ZZU(图6-1-c)。ZZU中,每个Ag12S6连接6个TPPE,每个TPPE连接4个Ag12S6.ZZU属于立方晶系,正当晶胞参数a=4.209mm,密度为0.618g·cm-3.ZZU沿着晶轴方向的投影如图6-2所示,在图6-2中用粗虚线画出ZZU正当晶胞的投影________ 。计算每个正当晶胞中Ag12S6和TPPE的数目_______ 、________ 。
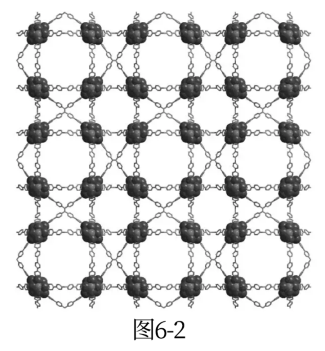
图6-1-a示出一种电中性银硫簇(简记为Ag12S6)的结构,包含12个银原子和6个硫原子(图中未区分原子大小)。6个银原子位于同一平面(称为赤道面),形成正六边形,彼此之间不成键。赤道面上、下方各有3个银原子,皆呈正三角形排布,彼此之间形成Ag-Ag键,并分别与赤道面。上的两个银原子形成Ag-Ag键。6个硫原子的位置如图所示。


(1)计算Ag12S6中Ag-Ag键的个数
(2)计算Ag12S6中三角形面的个数
(3)Ag12S6的硫原子来自于叔丁巯基,银为正一价。在Ag12S6上还连接有若干个CF3COO-,计算CF3COO-的个数
(4)聚集诱导发光(AIE)现象是一种由中国科学家首先发现的光致发光现象。具有AIE特性的有机分子在聚集状态下表现出远强于分散状态的光致发光性能。四苯乙烯(TPE)是一种典型的AIE分子。将TPE完全溶解于乙醇中,分别取等量的该溶液加入到等体积的水和甲苯中,判断哪一个体系的光致发光较强并简要解释原因
(5)利用上述Ag12S6和图6-1-b所示的TPPE配体组装,得到一种晶体框架材料ZZU(图6-1-c)。ZZU中,每个Ag12S6连接6个TPPE,每个TPPE连接4个Ag12S6.ZZU属于立方晶系,正当晶胞参数a=4.209mm,密度为0.618g·cm-3.ZZU沿着晶轴方向的投影如图6-2所示,在图6-2中用粗虚线画出ZZU正当晶胞的投影

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】自然界中,纯粹的典型晶体是不多的,大多数晶体是分子晶体、共价晶体、金属晶体和离子晶体之间的过渡晶体。以下列出了第三周期几种氧化物晶体中离子键的百分数。
提示:离子键的百分数是通过电负性的差值计算出来的,电负性的差值越大,离子键的百分数越大。
(1)从原子结构角度解释,为什么一般认为氧化镁属于离子晶体,而二氧化硅属于共价晶体:___________ 。
(2)硅元素位于元素周期表的___________ 区。基态硅原子的价层电子排布式为___________ 。
(3)一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,已知该晶体中晶胞各边长度分别为apm、apm和cpm,两条底边夹角为120°,距离最近的两个B原子之间距离为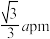 。
。
①该物质化学式为___________ ;
②距离每个B原子最近的Mg原子有___________ 个;
③该晶体密度为___________  。
。 含量。
含量。
(ⅰ)称取m克硅酸钠样品加热溶解后,配置为250mL待测液。
(ⅱ)移取50mL待测液至250mL锥形瓶中,加入10滴甲基红指示剂【HIn(红色) (黄色)】,摇匀后用0.2000mol/L HCl标准溶液滴定至体系为玫瑰红色,消耗盐酸体积为
(黄色)】,摇匀后用0.2000mol/L HCl标准溶液滴定至体系为玫瑰红色,消耗盐酸体积为 ,体系中有沉淀。
,体系中有沉淀。
(ⅲ)加入3.0g氟化钠固体,充分反应。
(ⅳ)用0.5000mol/L HCl标准溶液滴定至溶液为玫瑰红色并继续加入至过量,共加入 。
。
(ⅴ)用0.5000mol/L NaOH标准溶液滴定至溶液变为亮黄色,消耗NaOH溶液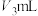 。
。
已知: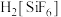 为强电解质,回答问题:
为强电解质,回答问题:
①步骤(ⅲ)中加入NaF后发生化学反应的离子方程式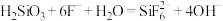 ,则加入NaF后的实验现象为
,则加入NaF后的实验现象为___________ 。
②样品中硅酸钠的纯度为___________ (用质量分数表示)。
| 氧化物 |  | MgO |  |  |
| 离子键百分数 | 62 | 50 | 41 | 33 |
(1)从原子结构角度解释,为什么一般认为氧化镁属于离子晶体,而二氧化硅属于共价晶体:
(2)硅元素位于元素周期表的
(3)一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,已知该晶体中晶胞各边长度分别为apm、apm和cpm,两条底边夹角为120°,距离最近的两个B原子之间距离为
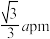 。
。①该物质化学式为
②距离每个B原子最近的Mg原子有
③该晶体密度为
 。
。
 含量。
含量。(ⅰ)称取m克硅酸钠样品加热溶解后,配置为250mL待测液。
(ⅱ)移取50mL待测液至250mL锥形瓶中,加入10滴甲基红指示剂【HIn(红色)
 (黄色)】,摇匀后用0.2000mol/L HCl标准溶液滴定至体系为玫瑰红色,消耗盐酸体积为
(黄色)】,摇匀后用0.2000mol/L HCl标准溶液滴定至体系为玫瑰红色,消耗盐酸体积为 ,体系中有沉淀。
,体系中有沉淀。(ⅲ)加入3.0g氟化钠固体,充分反应。
(ⅳ)用0.5000mol/L HCl标准溶液滴定至溶液为玫瑰红色并继续加入至过量,共加入
 。
。(ⅴ)用0.5000mol/L NaOH标准溶液滴定至溶液变为亮黄色,消耗NaOH溶液
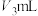 。
。已知:
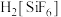 为强电解质,回答问题:
为强电解质,回答问题:①步骤(ⅲ)中加入NaF后发生化学反应的离子方程式
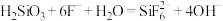 ,则加入NaF后的实验现象为
,则加入NaF后的实验现象为②样品中硅酸钠的纯度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】磷化硼是一种超硬耐磨涂层材料,结构与金刚石相似,其晶胞结构如图所示。请回答下列问题:___________ ,基态磷原子中电子的运动状态有___________ 种,与硼同主族的第四周期元素的基态原子价层电子的轨道表示式为___________ 。
(2) 为一元弱酸,
为一元弱酸, 分子中
分子中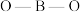 的键角
的键角___________ (填“ ”“
”“ ”或“
”或“ ”)
”) (中的
(中的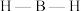 的键角,原因为
的键角,原因为___________ 。
(3)磷化硼晶体属于___________ 晶体,其中硼原子的配位数为___________ 。
(4)磷化硼的化学式为___________ ,该晶体的密度为___________  (用含a、
(用含a、 的代数式表示,阿伏加德罗常数的值为
的代数式表示,阿伏加德罗常数的值为 )。
)。

(2)
 为一元弱酸,
为一元弱酸, 分子中
分子中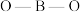 的键角
的键角 ”“
”“ ”或“
”或“ ”)
”) (中的
(中的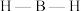 的键角,原因为
的键角,原因为(3)磷化硼晶体属于
(4)磷化硼的化学式为
 (用含a、
(用含a、 的代数式表示,阿伏加德罗常数的值为
的代数式表示,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】材料是人类文明进步的阶梯,第IIIA、IVA、VA族元素是组成特殊材料的重要元素。请回答下列问题:
(1)根据价层电子对互斥理论, 、
、 、
、 中,中心原子价层电子对数不同于其他两种粒子的是
中,中心原子价层电子对数不同于其他两种粒子的是_______ ,已知 与
与 互为等电子体,推算HCN分子中σ键与π键的数目比为
互为等电子体,推算HCN分子中σ键与π键的数目比为_______ 。
(2)M与Ga位于同周期, 的一种配合物组成为
的一种配合物组成为 。
。
①下列有关 、
、 的说法正确的是
的说法正确的是_______ (填字母)。
a.分子空间构型相同 b.中心原子杂化类型相同 c.键角大小相同
② 配体是
配体是_______ 。
③配合物T与 组成元素相同,中心离子的配位数相同。1moT溶于水,加入足量
组成元素相同,中心离子的配位数相同。1moT溶于水,加入足量 溶液只生成2molAgCl沉淀,则T的化学式为
溶液只生成2molAgCl沉淀,则T的化学式为_______ 。
(3)磷化硼(BP)是受高度关注的耐磨材料,可作为金属农面的保护层,其结构与金刚石类似,晶胞结构如图所示,磷化硼晶胞沿z轴在平面的投影图中,B原子构成的几何形状是_______ 。
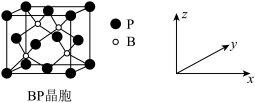
(4)已知晶胞中B与P原子最短距离为a pm,则磷化硼晶体的密度是_______  (仅列式不计算)。
(仅列式不计算)。
(1)根据价层电子对互斥理论,
 、
、 、
、 中,中心原子价层电子对数不同于其他两种粒子的是
中,中心原子价层电子对数不同于其他两种粒子的是 与
与 互为等电子体,推算HCN分子中σ键与π键的数目比为
互为等电子体,推算HCN分子中σ键与π键的数目比为(2)M与Ga位于同周期,
 的一种配合物组成为
的一种配合物组成为 。
。①下列有关
 、
、 的说法正确的是
的说法正确的是a.分子空间构型相同 b.中心原子杂化类型相同 c.键角大小相同
②
 配体是
配体是③配合物T与
 组成元素相同,中心离子的配位数相同。1moT溶于水,加入足量
组成元素相同,中心离子的配位数相同。1moT溶于水,加入足量 溶液只生成2molAgCl沉淀,则T的化学式为
溶液只生成2molAgCl沉淀,则T的化学式为(3)磷化硼(BP)是受高度关注的耐磨材料,可作为金属农面的保护层,其结构与金刚石类似,晶胞结构如图所示,磷化硼晶胞沿z轴在平面的投影图中,B原子构成的几何形状是

(4)已知晶胞中B与P原子最短距离为a pm,则磷化硼晶体的密度是
 (仅列式不计算)。
(仅列式不计算)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】硼、碳、氮、铜形成的单质及它们形成的化合物有重要研究和应用价值,回答下列问题:
(1)邻氨基吡啶的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。

①基态Cu原子的价电子排布式为___________ ,在元素周期表中铜位于___________ 区(填“s”“p”“d”或“ds”)。
②C、N、O三种元素的第一电离能由大到小的顺序为___________ 。
③邻氨基吡啶的铜配合物中,Cu2+的配位数是___________ ,N原子的杂化类型为___________ 。
(2)晶体硼单质的基本结构单元为正二十面体,其能自发地呈现多面体外形,这种性质称为晶体的___________ 。
(3)氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是___________ ,写出一种与氨硼烷互为等电子体的分子___________ (填化学式)。
(4)以硼酸(H3BO3)为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂。BH 的键角是
的键角是___________ 。
(5)磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,晶胞结构如图所示。磷化硼晶胞沿z轴在平面的投影图中,B原子构成的几何形状是___________ ;已知晶胞边长为a pm,则磷化硼晶体的密度是___________ g·cm-3(列出计算式,用NA来表示阿伏加德罗常数)。

(1)邻氨基吡啶的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。

①基态Cu原子的价电子排布式为
②C、N、O三种元素的第一电离能由大到小的顺序为
③邻氨基吡啶的铜配合物中,Cu2+的配位数是
(2)晶体硼单质的基本结构单元为正二十面体,其能自发地呈现多面体外形,这种性质称为晶体的
(3)氨硼烷(NH3BH3)被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是
(4)以硼酸(H3BO3)为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂。BH
 的键角是
的键角是(5)磷化硼(BP)是受高度关注的耐磨材料,可作为金属表面的保护层,其结构与金刚石类似,晶胞结构如图所示。磷化硼晶胞沿z轴在平面的投影图中,B原子构成的几何形状是

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐3】AA7075合金(含Al、Zn、Mg和Cu)几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳等的制作。但这种合金很难被焊接。最近,科学家将碳化钛纳米颗粒(大小仅为十亿分之一米)注入AA7075的焊丝内,让这些纳米颗粒充当连接件之间的填充材料,注入了纳米粒子的填充焊丝也可以更容易地连接其他难以焊接的金属和金属合金。回答下列问题:
(1)基态铜原子的价电子排布式为_______ 。
(2)第三周期某元素的前5个电子的电离能如图1所示。
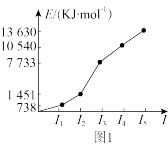
该元素是_______ (填元素符号)。
(3) 、
、 、
、 和
和 等配体都能与
等配体都能与 形成配离子。1mol
形成配离子。1mol 含
含_______ mol 键,其中的H-N-H键角
键,其中的H-N-H键角_______ (填“>”、“<”或“=”), 分子中的H-N-H键角。
分子中的H-N-H键角。
(4)铝镁合金是优质储钠材料,原子位于面心和顶点,其晶胞如图2所示。
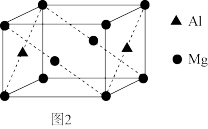
1个铝原子周围有_______ 个镁原子最近且等距离。
(5)在碱性溶液中,缩二脲 与
与 反应得到一种特征紫色物质,其结构如图所示,该反应原理可用于检验蛋白质或其他含多肽的化合物、缩二脲分子中氮原子的杂化类型为
反应得到一种特征紫色物质,其结构如图所示,该反应原理可用于检验蛋白质或其他含多肽的化合物、缩二脲分子中氮原子的杂化类型为_______ 。
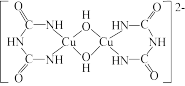
(6)钛晶体有两种晶胞,如图所示。
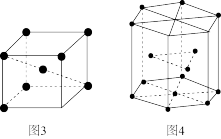
①如图3所示,晶胞的空间利用率为_______ (用含 的式子表示)。
的式子表示)。
②已知图4中,六棱柱边长为xcm,高为ycm。该钛晶胞密度为 ,
, 为
为_______  (用含x、y和D的式子表示)。
(用含x、y和D的式子表示)。
(1)基态铜原子的价电子排布式为
(2)第三周期某元素的前5个电子的电离能如图1所示。

该元素是
(3)
 、
、 、
、 和
和 等配体都能与
等配体都能与 形成配离子。1mol
形成配离子。1mol 含
含 键,其中的H-N-H键角
键,其中的H-N-H键角 分子中的H-N-H键角。
分子中的H-N-H键角。(4)铝镁合金是优质储钠材料,原子位于面心和顶点,其晶胞如图2所示。

1个铝原子周围有
(5)在碱性溶液中,缩二脲
 与
与 反应得到一种特征紫色物质,其结构如图所示,该反应原理可用于检验蛋白质或其他含多肽的化合物、缩二脲分子中氮原子的杂化类型为
反应得到一种特征紫色物质,其结构如图所示,该反应原理可用于检验蛋白质或其他含多肽的化合物、缩二脲分子中氮原子的杂化类型为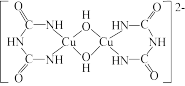
(6)钛晶体有两种晶胞,如图所示。

①如图3所示,晶胞的空间利用率为
 的式子表示)。
的式子表示)。②已知图4中,六棱柱边长为xcm,高为ycm。该钛晶胞密度为
 ,
, 为
为 (用含x、y和D的式子表示)。
(用含x、y和D的式子表示)。
您最近一年使用:0次



