硫酸的工业用途非常广泛,可用于制造化肥、除铁锈、作电解液等。工业制硫酸的关键一步是将SO2氧化为SO3,该反应为2SO2+O2 2SO3。但该反应速率小,无法投入工业化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造硫酸的生产工艺。材料中的反应为放热反应,下列说法正确的是
2SO3。但该反应速率小,无法投入工业化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造硫酸的生产工艺。材料中的反应为放热反应,下列说法正确的是
 2SO3。但该反应速率小,无法投入工业化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造硫酸的生产工艺。材料中的反应为放热反应,下列说法正确的是
2SO3。但该反应速率小,无法投入工业化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造硫酸的生产工艺。材料中的反应为放热反应,下列说法正确的是| A.断开化学键放出能量 |
| B.放热反应都不需要加热 |
| C.及时移走部分产物能加快反应速率 |
| D.该反应的反应物总能量大于生成物的总能量 |
更新时间:2021-12-22 12:54:03
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】 和
和 在催化剂表面合成氨的微观历程及能量变化的示意图如下,用
在催化剂表面合成氨的微观历程及能量变化的示意图如下,用 、
、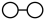 、
、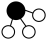 分别表示
分别表示 、
、 、
、 ,已知:
,已知: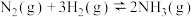
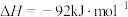 。下列说法正确的是
。下列说法正确的是
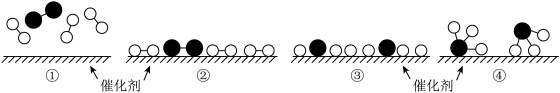
 和
和 在催化剂表面合成氨的微观历程及能量变化的示意图如下,用
在催化剂表面合成氨的微观历程及能量变化的示意图如下,用 、
、 、
、 分别表示
分别表示 、
、 、
、 ,已知:
,已知: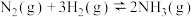
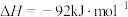 。下列说法正确的是
。下列说法正确的是
| A.使用催化剂,合成氨反应正向进行的程度增大 |
| B.②→③过程,是吸热过程且只有H-H键的断裂 |
C.③→④过程,N原子和H原子形成了含有非极性键的 |
| D.合成氨反应中,反应物断键吸收能量小于生成物形成新键释放的能量 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知白磷和P4O6的分子结构如图所示,又知化学键的键能是形成(或断开)1 mol化学键时释放(或吸收)的能量,现查知P—P键能为198 kJ·mol-1、P—O键能为360 kJ·mol-1、O=O键能为498 kJ·mol-1。若生成1 mol P4O6,则反应P4(白磷)+3O2=P4O6中的能量变化为


| A.吸收1 638 kJ能量 | B.放出1 638 kJ能量 |
| C.吸收126 kJ能量 | D.放出126 kJ能量 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
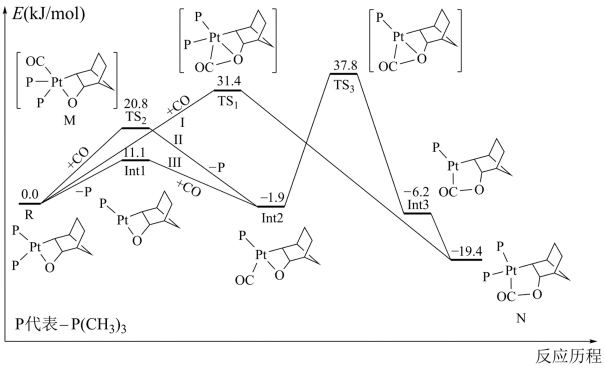
【推荐1】科研工作者通过计算机模拟和数学计算,设计出两条在含 结构的化合物中插入CO的反应路径,其相对能量变化如图所示,下列说法错误的是
结构的化合物中插入CO的反应路径,其相对能量变化如图所示,下列说法错误的是
 结构的化合物中插入CO的反应路径,其相对能量变化如图所示,下列说法错误的是
结构的化合物中插入CO的反应路径,其相对能量变化如图所示,下列说法错误的是
| A.该反应为放热反应 |
B.路径Ⅱ中的最大能垒(活化能)为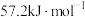 |
| C.反应过程中Pt的成键数目发生了改变 |
| D.图中M与N互为同分异构体 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列过程都与能量变化有关,其中表述不正确 的是( )
A.CO(g)的燃烧热是283.0kJ·mol-1,则表示CO(g)燃烧热的热化学方程式为CO(g)+ O2(g)=CO2(g) ΔH=-283.0kJ·mol-1 O2(g)=CO2(g) ΔH=-283.0kJ·mol-1 |
| B.铝热反应会放出大量的热,因此常温下就能顺利发生 |
| C.拆开化学键需要吸收能量,形成化学键会释放能量 |
| D.化学电池是把化学能转化为电能的装置 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知化合物A与H2O在一定条件下反应生成化合物B与HCOO-,其反应历程如图所示,其中TS表示过渡态,I表示中间体。下列说法正确的是


| A.化合物A与H2O之间的碰撞均为有效碰撞 |
| B.过渡态为活化配合物,其性质极不稳定 |
| C.该历程中TS2时活化分子百分数最大 |
| D.使用催化剂可以加快该反应速率,改变该反应进行的方向 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知某化学反应A2(g)+2B2(g)=2AB2(g)的能量变化如图所示,下列有关叙述中正确的是
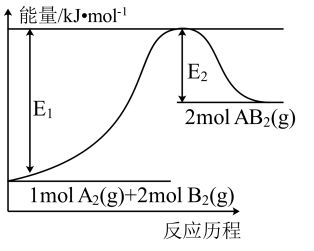

| A.该反应是熵增的反应 |
| B.该反应的ΔH=(E2-E1)kJ·mol-1 |
| C.该反应的活化能为E2 |
| D.该反应中,反应物分子的键能总和大于生成物分子的键能总和 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】我国科学工作者首次实现二氧化碳到淀粉人工合成研究并取得原创性突破,相关成果于9月24日在线发表在国际学术期刊《科学》上。转化涉及的第一步反应的化学方程式为CO2(g) + 3H2(g) ⇌CH3OH(g) + H2O(g)。下列叙述正确的是
| A.平衡后,其他条件不变,缩小容器体积,可提高CO2和H2的转化率 |
| B.当v(CO2) = v(CH3OH)时,反应一定达到平衡状态 |
| C.其他条件不变移去水蒸气,可增大正反应速率 |
| D.恒容条件下,向容器中充入少量氦气,可加快反应速率 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验装置及其应用的描述均正确的是


| A.用①装置验证铁钉的析氢腐蚀 |
| B.用②装置进行强酸强碱稀溶液的中和热测定 |
| C.用③装置测定未知稀盐酸的物质的量浓度 |
| D.用④装置探究反应物浓度对反应速率的影响 |
您最近半年使用:0次

 的能量变化曲线如图所示,判断下列叙述中正确的是
的能量变化曲线如图所示,判断下列叙述中正确的是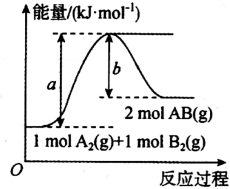

 时吸收b
时吸收b 热量
热量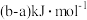
 键和1
键和1 键,并且旧化学键断裂放出能量,然后再形成2
键,并且旧化学键断裂放出能量,然后再形成2 键,形成新的化学键吸收能量
键,形成新的化学键吸收能量 分子,其结构与白磷
分子,其结构与白磷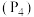 相同。已知断裂
相同。已知断裂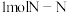 键吸收
键吸收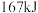 能量,断裂
能量,断裂 键吸收
键吸收 能量。下列说法正确的是
能量。下列说法正确的是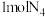 转化为
转化为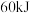 能量
能量 分子中含有
分子中含有 个
个 键
键 2NH3(g) ΔH<0 选择加热到500 ℃
2NH3(g) ΔH<0 选择加热到500 ℃ ,采取下列措施不能改变反应速率的是(
,采取下列措施不能改变反应速率的是( 的量
的量

