有四种短周期元素,它们的结构或性质等信息如表所述。
请根据表中信息填写:
(1)A原子的核外电子排布式:_______ 。
(2)B元素在周期表中的位置:_______ ;离子半径:B_______ (填“大于”或“小于”)A。
(3)C原子的核外电子轨道表示式是_______ ,其原子核外有_______ 个未成对电子,能量最高的电子为_______ 轨道上的电子,其电子云形状呈_______ 形。
(4)D原子的核外电子排布式为_______ ,D-的结构示意图是_______ 。
| 元素 | 结构或性质 |
| A | A是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是快中子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,其单质可用作制冷剂 |
| D | D是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
(1)A原子的核外电子排布式:
(2)B元素在周期表中的位置:
(3)C原子的核外电子轨道表示式是
(4)D原子的核外电子排布式为
21-22高二·全国·课时练习 查看更多[4]
(已下线)1.2.1 原子结构与元素周期表(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)1.2.1 原子结构与元素周期表-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)(已下线)1.2.1 原子结构与元素周期表-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)(已下线)BBWYhjhx1113.pdf
更新时间:2021-12-25 16:18:36
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】下表列出了①~⑩10种元素在周期表中的位置,请回答下列问题:
(1)元素⑩名称为___________ ,⑦的原子结构示意图为___________ 。
(2)最高价氧化物是两性氧化物的元素是___________ (填元素符号)。
(3)最高价氧化物的水化物中,酸性最强的化合物的化学式是___________ 。
(4)③、⑤、⑥三种元素的原子半径最大的是___________ (填符号,下同),三种元素所形成的离子中,离子半径由大到小的顺序是___________ ;④、⑤、⑨的最高价氧化物对应水化物的碱性由强到弱的顺序是___________ ;①、②、③的简单氢化物的稳定性由弱到强的顺序是___________ 。
(5)用一个离子方程式说明单质⑦的氧化性比单质⑩的氧化性强:___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)最高价氧化物是两性氧化物的元素是
(3)最高价氧化物的水化物中,酸性最强的化合物的化学式是
(4)③、⑤、⑥三种元素的原子半径最大的是
(5)用一个离子方程式说明单质⑦的氧化性比单质⑩的氧化性强:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
(1)地壳中含量居于第二位的元素在周期表中的位置是_______ 。
(2)用电子式表示②的最高价氧化物的形成过程为_______ 。
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:_______ 。
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是_______ (填字母)。
A.最高正化合价为+6
B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱
D.单质在常温下可与氢气化合
(5)已知Cs元素位于元素周期表中第六周期第IA族,请回答下列问题:
①铯的原子序数为_______ 。
②铯单质与H2O反应的化学反应方程式为_______ 。
③预测铯单质的还原性比钠单质的还原性_______ (填“弱”或“强”)。
④下列推断正确的是_______ (填字母)。
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(6)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为_______ 。

(1)地壳中含量居于第二位的元素在周期表中的位置是
(2)用电子式表示②的最高价氧化物的形成过程为
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是
A.最高正化合价为+6
B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱
D.单质在常温下可与氢气化合
(5)已知Cs元素位于元素周期表中第六周期第IA族,请回答下列问题:
①铯的原子序数为
②铯单质与H2O反应的化学反应方程式为
③预测铯单质的还原性比钠单质的还原性
④下列推断正确的是
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(6)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
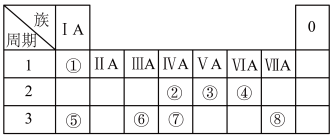
【推荐3】下表是元素周期表的一部分,请用化学用语回答有关问题:
(1)⑥的氢氧化物中,所含化学键的类型是______ 。
(2)①和④可形成化合物,用电子式表示其形成过程______ 。
(3)⑦的最高价氧化物的水化物与⑧的最高价氧化物的水化物反应的离子方程式为_____ 。
(4)研究物质的性质差异性是学习的重要方法之一。②、③、⑧、⑨四种元素的最高价氧化物的水化物中,化学性质明显不同于其它三种酸的是______ 。
(5)能说明元素⑤的非金属性强于元素⑨的非金属性的实验事实是_____ (填字母)。
A.两种单质的熔沸点不同
B.两种单质与氢气化合的难易程度
C.比较这两种元素的最高价氧化物的水化物的酸性
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ |
(1)⑥的氢氧化物中,所含化学键的类型是
(2)①和④可形成化合物,用电子式表示其形成过程
(3)⑦的最高价氧化物的水化物与⑧的最高价氧化物的水化物反应的离子方程式为
(4)研究物质的性质差异性是学习的重要方法之一。②、③、⑧、⑨四种元素的最高价氧化物的水化物中,化学性质明显不同于其它三种酸的是
(5)能说明元素⑤的非金属性强于元素⑨的非金属性的实验事实是
A.两种单质的熔沸点不同
B.两种单质与氢气化合的难易程度
C.比较这两种元素的最高价氧化物的水化物的酸性
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
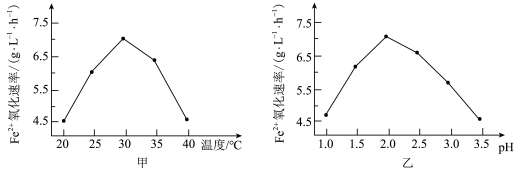
【推荐1】铜和三氧化二铁在工农业生产中用途广泛。用黄铜矿(主要成分为 ,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:
,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:
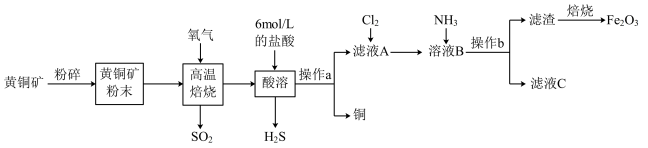
回答下列问题:
(1)铜的价电子排布式____________ 。
(2)高温焙烧时发生的反应是 ,1mol
,1mol  参加反应时,反应中转移电子
参加反应时,反应中转移电子____________ mol。
(3)向滤液A中通入 的目的是
的目的是________________________________________________ 。
(4)向溶液B中通入 后发生反应的离子方程式为
后发生反应的离子方程式为_____________________________________________ 。
(5)工业上用生物法处理 的原理为:(硫杆菌作催化剂)
的原理为:(硫杆菌作催化剂)
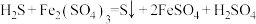
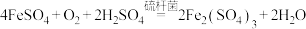
由图甲和图乙判断使用硫杆菌的最佳条件为___________________ 。若反应温度过高,反应速率下降,其原因是_______________________________________________ 。
 ,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:
,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:
回答下列问题:
(1)铜的价电子排布式
(2)高温焙烧时发生的反应是
 ,1mol
,1mol  参加反应时,反应中转移电子
参加反应时,反应中转移电子(3)向滤液A中通入
 的目的是
的目的是(4)向溶液B中通入
 后发生反应的离子方程式为
后发生反应的离子方程式为(5)工业上用生物法处理
 的原理为:(硫杆菌作催化剂)
的原理为:(硫杆菌作催化剂)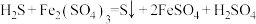
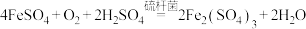
由图甲和图乙判断使用硫杆菌的最佳条件为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
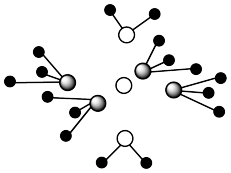
【推荐2】铜离子可与含N、含O的微粒形成多种结构。向CuSO4溶液中滴加氨水可最终形成如图所示的配离子。

(1)图中微粒的化学式为
A.1mol该微粒中有22mol共价键
B.该微粒中的N、O原子构成了立方体结构
C.电负性N>O>H
D.该微粒中可与溶剂水分子形成氢键的只有N、O原子
(2)铜元素位于元素周期表的
A.s区 B.p区 C.ds区 D.f区
铜原子
(3)Cu2+无法与BF3中的B原子形成配位键的原因是
(4)请在图中用规范的化学符号表示该微粒中的所有配位键
(5)Cu2+可形成如图所示晶体。该晶胞中

①该晶体中距Fe3+最近且等距的Cu2+有
②已知相邻的Fe3+与Cu2+核间距为apm,则相邻的Fe3+与K+核间距为
③该晶体的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】近年来,我国从顶层设计层面做出了多项举措,十四五规划中明确要求降低碳排放强度,新能源汽车能显著减少碳的排放,而新能源汽车电池主要有磷酸铁锂电池和三元锂电池,三元锂电是指正极材料使用镍钴锰酸锂[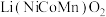 ],请回答下列关于镍钴铁的相关问题。
],请回答下列关于镍钴铁的相关问题。
(1)Ni原子的价电子排布式为___________ 。
(2) 常温下为无色液体,沸点42.1℃,熔点-19.3℃,难溶于水,易溶于有机溶剂。推测
常温下为无色液体,沸点42.1℃,熔点-19.3℃,难溶于水,易溶于有机溶剂。推测 的晶体类型为
的晶体类型为___________ ,是___________ 分子(填“极性”或“非极性”)。
(3)实验室常用KSCN溶液或苯酚( )检验溶液中存在
)检验溶液中存在 ,现象分别是
,现象分别是___________ 、___________ 。
(4)配位化合物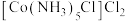 中心原子Co的配位数为
中心原子Co的配位数为___________ ,配位原子为___________ 。
(5)NiO的晶体结构如图甲所示,其中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为___________ 。

(6)已知Ni可以形成多种氧化物,其中一种NixO晶体的晶胞结构为NaCl型,由于晶体缺陷导致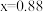 ,晶胞参数为a nm,则晶体密度为
,晶胞参数为a nm,则晶体密度为___________ g·cm (
( 表示阿伏加德罗常数的值,只需列出计算式,无须化简)。
表示阿伏加德罗常数的值,只需列出计算式,无须化简)。
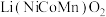 ],请回答下列关于镍钴铁的相关问题。
],请回答下列关于镍钴铁的相关问题。(1)Ni原子的价电子排布式为
(2)
 常温下为无色液体,沸点42.1℃,熔点-19.3℃,难溶于水,易溶于有机溶剂。推测
常温下为无色液体,沸点42.1℃,熔点-19.3℃,难溶于水,易溶于有机溶剂。推测 的晶体类型为
的晶体类型为(3)实验室常用KSCN溶液或苯酚(
 )检验溶液中存在
)检验溶液中存在 ,现象分别是
,现象分别是(4)配位化合物
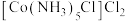 中心原子Co的配位数为
中心原子Co的配位数为(5)NiO的晶体结构如图甲所示,其中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为

(6)已知Ni可以形成多种氧化物,其中一种NixO晶体的晶胞结构为NaCl型,由于晶体缺陷导致
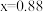 ,晶胞参数为a nm,则晶体密度为
,晶胞参数为a nm,则晶体密度为 (
( 表示阿伏加德罗常数的值,只需列出计算式,无须化简)。
表示阿伏加德罗常数的值,只需列出计算式,无须化简)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】I:氨硼烷(NH3BH3)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。
(1)写出基态N原子的核外电子排布图_______________________ 。
(2)NH3BH3分子中,N-B化学键称为配位键,其电子对由___ 原 子提供。氨硼烷在催化剂作用下与水反应放出氢气:3NH3BH3+6H2O=3NH +B3O
+B3O +9H2↑
+9H2↑
B3O 的结构为
的结构为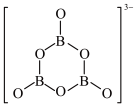 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由_____ 变为______ 。
II:如图是某化合物的晶胞示意图,硅原子与铝原子之间都以共价键连接。该立方体晶胞边长为a pm。
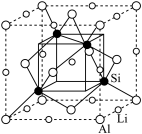
(3)该化合物的化学式是___________________ 。
(4)该晶体晶胞沿z轴在平面的投影图中,Al 原子构成的图为下列图形中的_______ 。

(5)求出Si与Al之间的共价键键长是____ pm。
(1)写出基态N原子的核外电子排布图
(2)NH3BH3分子中,N-B化学键称为配位键,其电子对由
 +B3O
+B3O +9H2↑
+9H2↑B3O
 的结构为
的结构为 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由II:如图是某化合物的晶胞示意图,硅原子与铝原子之间都以共价键连接。该立方体晶胞边长为a pm。

(3)该化合物的化学式是
(4)该晶体晶胞沿z轴在平面的投影图中,Al 原子构成的图为下列图形中的

(5)求出Si与Al之间的共价键键长是
您最近一年使用:0次
【推荐2】钕铁硼磁铁是目前为止具有最强磁力的永久磁铁。生产钕铁硼磁铁的主要原材料有稀土金属钕、高纯铁、铝、硼等。回答下列问题:
(1)钕(Nd)为60号元素,在周期表中位于第___________ 周期。基态硼原子中占据最高能级的电子,电子云轮廓图形状为___________ 。Fe2+的价电子排布图___________
(2)铜能与类卤素(CN)2反应生成Cu(CN)2,1 mol (CN)2分子中含有π键的数目为___________ 。
(3)Cu2+能与NH3、H2O、Cl-等形成配位数为4的配合物。
①[Cu(NH3)4]SO4中,N、O、S三种元素的第一电离能从大到小的顺序为___________ 。
②[Cu(NH3)4]SO4中,不存在的化学键的类型有___________ (填选项)。
A.离子键 B.配位键 C.非极性键 D.极性键
③[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为___________ 。
(1)钕(Nd)为60号元素,在周期表中位于第
(2)铜能与类卤素(CN)2反应生成Cu(CN)2,1 mol (CN)2分子中含有π键的数目为
(3)Cu2+能与NH3、H2O、Cl-等形成配位数为4的配合物。
①[Cu(NH3)4]SO4中,N、O、S三种元素的第一电离能从大到小的顺序为
②[Cu(NH3)4]SO4中,不存在的化学键的类型有
A.离子键 B.配位键 C.非极性键 D.极性键
③[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】新型超高能材料是国家核心军事力量制高点的重要标志,高性能炸药BNCP的结构如图,回答下列问题:

(1)BNCP中Co3+的基态价层电子轨道表示式是__ ,Co3+的配位数是__ ,阴离子ClO4-的中心原子杂化类型是__ 。
(2)1mol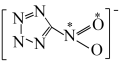 配体中的σ键的数目是
配体中的σ键的数目是__ ,已知该配体是平面结构,图中标记的N原子与O原子之间的σ键是由N原子的__ 杂化轨道与O原子的__ 轨道重叠形成的。
(3)比较NO2+、NO2、NO2-的键角大小:__ ,与NO2-互为等电子体的单质是___ 。
(4)比较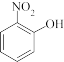 、
、 的沸点并说明理由:
的沸点并说明理由:__ 。
(5)比较H2O与OF2的极性大小并说明理由:__ 。
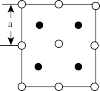
(6)2018年南京理工大学胡炳成团队合成全国首个全氮阴离子,全氮阴离子的盐AgN5的晶体结构中:N5-采取面心立方最密堆积,Ag+填在正四面体空隙中,从晶胞上方的俯视投影图如图。每个晶胞中含有的N5-的数目是__ 。Ag+与N5-最近的距离是__ (用a表示)。

(1)BNCP中Co3+的基态价层电子轨道表示式是
(2)1mol
 配体中的σ键的数目是
配体中的σ键的数目是(3)比较NO2+、NO2、NO2-的键角大小:
(4)比较
 、
、 的沸点并说明理由:
的沸点并说明理由:(5)比较H2O与OF2的极性大小并说明理由:
(6)2018年南京理工大学胡炳成团队合成全国首个全氮阴离子,全氮阴离子的盐AgN5的晶体结构中:N5-采取面心立方最密堆积,Ag+填在正四面体空隙中,从晶胞上方的俯视投影图如图。每个晶胞中含有的N5-的数目是

您最近一年使用:0次



