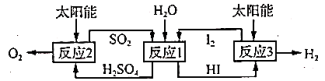
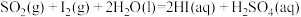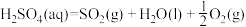下列有关说法正确的是
A. 溶液中: 溶液中: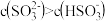 |
B.常温下,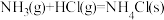 能自发的原因是 能自发的原因是 |
C.已知: ,保持温度不变,增大压强, ,保持温度不变,增大压强, 的浓度减小 的浓度减小 |
D.向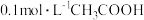 溶液中加适量水,导致溶液中 溶液中加适量水,导致溶液中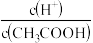 减小 减小 |
更新时间:2021-12-25 13:40:02
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】25℃和 时,
时,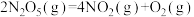
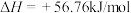 ,该反应能自发进行的原因是
,该反应能自发进行的原因是
| A.是吸热反应 | B.是放热反应 |
| C.是熵减少的反应 | D.熵增大效应大于焓效应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】人体内的血红蛋白(Hb)可与O2结合,Hb 也可以与CO结合,涉及原理如下:
①Hb(aq)+O2(g) HbO2(aq) ΔH1<0
HbO2(aq) ΔH1<0
②Hb(aq)+CO(g) HbCO(aq) ΔH2<0
HbCO(aq) ΔH2<0
③HbO2(aq) +CO(g) HbCO(aq)+ O2(g) ΔH3<0
HbCO(aq)+ O2(g) ΔH3<0
下列说法不正确的是
①Hb(aq)+O2(g)
 HbO2(aq) ΔH1<0
HbO2(aq) ΔH1<0②Hb(aq)+CO(g)
 HbCO(aq) ΔH2<0
HbCO(aq) ΔH2<0③HbO2(aq) +CO(g)
 HbCO(aq)+ O2(g) ΔH3<0
HbCO(aq)+ O2(g) ΔH3<0下列说法不正确的是
| A.ΔH1>ΔH2 |
| B.反应①与反应②在较低温度能自发进行 |
| C.从平原初到高原,人体血液中c(HbO2)将降低造成缺氧 |
| D.把CO中毒的人转到高压氧仓中治疗,反应①平衡正移,c(HbO2)增大, 反应③平衡正移 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】室温下,甲、乙两烧杯均盛有5 mL pH=3的某一元酸溶液,向乙烧杯中加水稀释至pH=4。关于甲、乙两烧杯中溶液的描述正确的是( )
①溶液的体积:10V甲≤V乙
②水电离出的OH-浓度:10c(OH-)甲≤c(OH-)乙
③若分别用等浓度的NaOH溶液完全中和,所得溶液的pH:甲≤乙
④若分别与5 mL pH=11的NaOH溶液反应,所得溶液的pH:甲≤乙
①溶液的体积:10V甲≤V乙
②水电离出的OH-浓度:10c(OH-)甲≤c(OH-)乙
③若分别用等浓度的NaOH溶液完全中和,所得溶液的pH:甲≤乙
④若分别与5 mL pH=11的NaOH溶液反应,所得溶液的pH:甲≤乙
| A.①② | B.②③ | C.③④ | D.①④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关电解质溶液的说法正确的是
| A.向0.1 mol·L-1 CH3COOH溶液中加入少量水,溶液中导电粒子的数目减少 |
B.升高CH3COONa溶液的温度,溶液中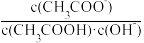 增大 增大 |
| C.盐酸与氨水恰好完全反应,则溶液中c(H+)=c(OH-) |
| D.向AgCl的饱和溶液中加入少量AgNO3溶液,则溶液中c(Ag+)·c(Cl-)保持不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】取浓度相等的NaOH和HCl溶液,以体积比为3∶2的比例相混合,所得溶液中的
c(OH-)=0.01mol/L,则原溶液中溶质的物质的量浓度为(溶液混合体积变化忽略)( )
c(OH-)=0.01mol/L,则原溶液中溶质的物质的量浓度为(溶液混合体积变化忽略)( )
| A.0.01 mol/L | B.0.015 mol/L | C.0.017 mol/L | D.0.05 mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,向 和NaOH混合溶液中缓慢通入
和NaOH混合溶液中缓慢通入 至过量
至过量 溶液温度变化忽略不计
溶液温度变化忽略不计 ,生成沉淀物质的量与通入
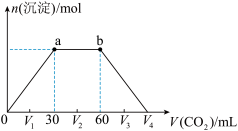
,生成沉淀物质的量与通入 体积的关系如图所示。下列说法不正确的是
体积的关系如图所示。下列说法不正确的是
 和NaOH混合溶液中缓慢通入
和NaOH混合溶液中缓慢通入 至过量
至过量 溶液温度变化忽略不计
溶液温度变化忽略不计 ,生成沉淀物质的量与通入
,生成沉淀物质的量与通入 体积的关系如图所示。下列说法不正确的是
体积的关系如图所示。下列说法不正确的是

A.b点时溶质为 |
B.横坐标轴上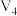 的值为90 的值为90 |
C.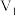 、 、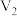 、 、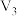 时,溶液 时,溶液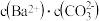 中相等 中相等 |
D.原混合物中 : : ;2 ;2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知25 ℃时部分弱酸的电离常数如下表所示,下列说法错误的是
| 弱酸 | CH3COOH | H2CO3 | HNO2 | HCN |
| 电离常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=5.0×10-4 | Ka=6.2×10-10 |
| A.电离常数与温度有关 |
| B.CO2通入NaNO2溶液中可以生成HNO2 |
C.少量CO2通入足量NaCN溶液中,离子方程式为CO2+H2O+CN-=HCN+HCO |
D.足量CH3COOH与少量Na2CO3溶液反应,离子方程式为2CH3COOH+CO =2CH3COO-+CO2↑+H2O =2CH3COO-+CO2↑+H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某温度下硫酸钡与水组成的混合物中加入少量硫酸钠固体,下列说法错误的是
| A.BaSO4的电离程度减小 | B.BaSO4溶解的量减小 |
C.c(Ba2+)与c(SO )的乘积不变 )的乘积不变 | D.溶液的导电能力增强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】如图所示,有T1、T2两种温度下两条BaSO4在水中的沉淀溶解平衡曲线,在T1温度下,下列说法不正确的是

| A.加入Na2SO4可使溶液由a点变到b点 |
| B.在T1曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成 |
| C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b) |
| D.升温可使溶液由b点变为d点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】已知Ksp(AgCl)=1.8×10-10。向盛有0.1 mol/L AgNO3溶液的试管中滴加等体积0.1 mol/L NaCl溶液,静置沉降,取上层清液和下层悬浊液分别进行实验。下列判断正确的是
| A.上层清液为AgCl的饱和溶液 |
| B.向清液中滴加0.1 mol/L AgNO3溶液,c(Cl-)不变 |
| C.向悬浊液中滴加0.1 mol/L KI溶液,不会有明显变化 |
| D.向悬浊液中加入适量浓氨水,混合液变澄清,说明AgCl可溶于强碱 |
您最近一年使用:0次

 ,
, ,再用浓硫酸吸收
,再用浓硫酸吸收 ),发烟硫酸与水反应可得硫酸。“热化学硫碘循环分解水”是一种利用硫酸、碘等来获取氢能源方法。以太阳能为热源,“热化学硫碘循环分解水”的反应过程如下:
),发烟硫酸与水反应可得硫酸。“热化学硫碘循环分解水”是一种利用硫酸、碘等来获取氢能源方法。以太阳能为热源,“热化学硫碘循环分解水”的反应过程如下: