在一个V升的密闭容器中放入2L A气体和1L B气体,在一定条件下发生反应:
3A(g)+ B(g) nC(g) + 2D(g),达到平衡后,A的浓度减小,混合气体的平均分子量增大,则该反应方程式中n值是
nC(g) + 2D(g),达到平衡后,A的浓度减小,混合气体的平均分子量增大,则该反应方程式中n值是
3A(g)+ B(g)
 nC(g) + 2D(g),达到平衡后,A的浓度减小,混合气体的平均分子量增大,则该反应方程式中n值是
nC(g) + 2D(g),达到平衡后,A的浓度减小,混合气体的平均分子量增大,则该反应方程式中n值是| A.1 | B.2 | C.3 | D.4 |
11-12高二上·山西大同·期中 查看更多[4]
四川省南充市阆中中学2020届高三化学选择题专项训练(7)(已下线)2011-2012学年山西省大同一中高二上学期期中考试化学试卷2014-2015山西省大同市一中高二上学期期中化学试卷(已下线)2013届黑龙江省大庆铁人中学高三第三次阶段化学试卷
更新时间:2016-12-09 04:01:40
|
【知识点】 化学平衡的有关计算
相似题推荐
单选题
|
适中
(0.65)
【推荐1】为倡导“低碳”,减小CO2对环境的影响,需对CO2进行创新利用研究。T1℃使,将将9 mol CO2和12 mol H2充入3 L密闭容器中,发生反应CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH<0,容器中CH3OH的物质的量随时间变化如曲线Ⅰ所示,平衡时容器内压强为p0。改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线Ⅱ所示。下列说法错误的是
CH3OH(g)+H2O(g) ΔH<0,容器中CH3OH的物质的量随时间变化如曲线Ⅰ所示,平衡时容器内压强为p0。改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线Ⅱ所示。下列说法错误的是
 CH3OH(g)+H2O(g) ΔH<0,容器中CH3OH的物质的量随时间变化如曲线Ⅰ所示,平衡时容器内压强为p0。改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线Ⅱ所示。下列说法错误的是
CH3OH(g)+H2O(g) ΔH<0,容器中CH3OH的物质的量随时间变化如曲线Ⅰ所示,平衡时容器内压强为p0。改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线Ⅱ所示。下列说法错误的是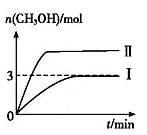
| A.曲线Ⅱ对应的条件改变是增大压强 |
| B.T2℃时,上述反应平衡常数为0.52,则T2>T1 |
| C.在T1℃,若起始时向容器充入4.5 mol CO2、6 mol H2,平衡时容器内压强P1>P0/2 |
| D.在T1℃,若起始时向容器中充入4.5 mol CO2、5 mol H2、5 mol CH3OH(g)和5 mol H2O(g),则达平衡前v(正)>v(逆) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某温度下,在恒容(2 L)密闭容器中发生反应:N2(g)+3H2(g)⇌2NH3(g)。甲、乙、丙三种情况下,起始充入N2和H2的物质的量如表所示,其中甲经2 min达平衡时,N2的转化率为50%。下列判断正确的是
| 起始物质的量mol | 甲 | 乙 | 丙 |
| n(N2) | 1 | 2 | 2 |
| n(H2) | 3 | 3 | 6 |
| A.容器中气体的密度可作为判断反应是否达到平衡状态的标志 |
| B.平衡时,乙中H2转化率大于50% |
| C.反应达平衡时,丙中H2的物质的量浓度c(H2)等于甲中的2倍 |
| D.甲、乙、丙三种条件下的化学平衡常数之间的关系为K甲<K乙<K丙 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】把2.5molA和2.5molB混合盛入容积为2L的密闭容器里,发生如下反应:3A(g)+B(g) xC(g)+2D(g),经5s反应达平衡状态,在此5s内C的平均反应速率为0.2mol·L-1·s-1,同时生成1molD,下列叙述中错误的是
xC(g)+2D(g),经5s反应达平衡状态,在此5s内C的平均反应速率为0.2mol·L-1·s-1,同时生成1molD,下列叙述中错误的是
 xC(g)+2D(g),经5s反应达平衡状态,在此5s内C的平均反应速率为0.2mol·L-1·s-1,同时生成1molD,下列叙述中错误的是
xC(g)+2D(g),经5s反应达平衡状态,在此5s内C的平均反应速率为0.2mol·L-1·s-1,同时生成1molD,下列叙述中错误的是| A.x=4 |
| B.达到平衡状态时容器内气体的压强与起始时压强之比为6∶5 |
| C.5s内B的反应速率v(B)=0.05mol·L-1·s-1 |
| D.达到平衡状态时A的转化率为40% |
您最近一年使用:0次



