测定硫酸铜晶体(CuSO4·xH2O)结晶水含量的实验流程如下,回答下列问题:
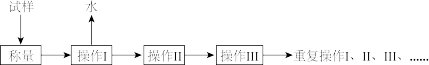
(1)以下是实验中可能用到的几种仪器,请在图下方横线上写出仪器名称。
a. 电子天平 b.
电子天平 b.
___________ c.
___________ d. 酒精灯
酒精灯
①“操作Ⅰ”是灼烧硫酸铜晶体,用到上述___________ (填序号)仪器。
②“操作Ⅱ”的操作是___________ ,必须在___________ (填序号)中进行。
(2)“重复操作Ⅰ、Ⅱ、Ⅲ”,称为恒重操作。判断达到恒重的依据是___________ ;进行恒重操作的目的是___________ 。
(3)某学生实验后得到以下数据:
①根据以上数据计算该硫酸铜晶体中结晶水x的值为___________ (精确到0.1)。
②该学生测定结果___________ (填“偏高”、“偏低”或“正确”)。
③从下列分析中选出该学生产生实验误差的原因可能是(填序号)___________ 。
a. 没有进行恒重操作 b. 加热固体到白色后,露置在空气中冷却
c. 加热过程中晶体有少量溅失 d. 加热后在干燥器中冷却至室温后称重

(1)以下是实验中可能用到的几种仪器,请在图下方横线上写出仪器名称。
a.
 电子天平 b.
电子天平 b.

 酒精灯
酒精灯①“操作Ⅰ”是灼烧硫酸铜晶体,用到上述
②“操作Ⅱ”的操作是
(2)“重复操作Ⅰ、Ⅱ、Ⅲ”,称为恒重操作。判断达到恒重的依据是
(3)某学生实验后得到以下数据:
| 加热前质量 | 加热后质量 | |
| m1(容器) | m2(容器+晶体) | m3(容器+无水硫酸铜) |
| 5.200g | 7.900g | 6.900g |
②该学生测定结果
③从下列分析中选出该学生产生实验误差的原因可能是(填序号)
a. 没有进行恒重操作 b. 加热固体到白色后,露置在空气中冷却
c. 加热过程中晶体有少量溅失 d. 加热后在干燥器中冷却至室温后称重
更新时间:2021-12-18 14:37:38
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】草木灰中含有可溶性钾盐(主要成分是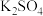 、
、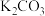 、KCl)。某学生按下列操作提取草木灰中的钾盐。
、KCl)。某学生按下列操作提取草木灰中的钾盐。
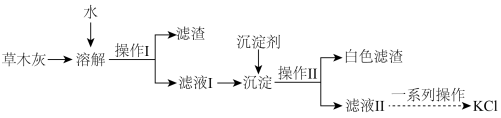
回答下列问题:
(1)“操作Ⅰ”的名称为___________ 。
(2)已知加入的“沉淀剂”为 ,则“白色滤渣”的主要成分为
,则“白色滤渣”的主要成分为___________ (填化学式),若向“白色滤渣”中加入稀盐酸,可观察到的实验现象为___________ ,写出加盐酸发生反应的化学方程式:___________ 。
(3)判断加入的“沉淀剂”已足量的方法为___________ 。
(4)经过“一系列操作”可获得KCl,则“一系列操作”为___________ 、过滤、洗涤、干燥。
(5)检验“滤液Ⅱ”中含有钾离子的实验方法为___________ 。
(6)钾元素有多种核素,其中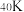 的质子数与中子数之差为
的质子数与中子数之差为___________ ;写出K原子的结构示意图:___________ 。
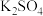 、
、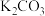 、KCl)。某学生按下列操作提取草木灰中的钾盐。
、KCl)。某学生按下列操作提取草木灰中的钾盐。
回答下列问题:
(1)“操作Ⅰ”的名称为
(2)已知加入的“沉淀剂”为
 ,则“白色滤渣”的主要成分为
,则“白色滤渣”的主要成分为(3)判断加入的“沉淀剂”已足量的方法为
(4)经过“一系列操作”可获得KCl,则“一系列操作”为
(5)检验“滤液Ⅱ”中含有钾离子的实验方法为
(6)钾元素有多种核素,其中
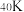 的质子数与中子数之差为
的质子数与中子数之差为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】重晶石矿的主要成分为硫酸钡,纯净的硫酸钡才能供医用作“钡餐”,在对某些内脏器官进行X 射线透视时服用。硫化钡是可溶于水的盐。讨论用重晶石矿制硫酸钡,设计流程如下:
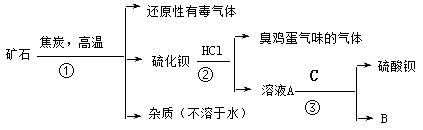
(1)写出步骤①的化学反应方程式___________ ,该反应产生的气体具有____ 、_____ 等用途。
(2)为进行②反应先要分离出硫化钡溶液,采用的方法是__________ 。在此之前要在溶液中滴入少量Ba(OH)2溶液,其作用是___________ 。
(3)若B物质在该生产过程中可循环使用,则③反应的化学方程式是:___________ 。
(4)有人提出②反应产生了有臭有毒的气体,可采用改变反应物的方法使无该气体产生,则②反应的化学方程式是:__________________________ 。
此时若要B物质还能循环使用,则C为__________ (写化学式)。
(5)BaSO4是因为具有_________ 、_________ 等性质而可用作“钡餐”的。

(1)写出步骤①的化学反应方程式
(2)为进行②反应先要分离出硫化钡溶液,采用的方法是
(3)若B物质在该生产过程中可循环使用,则③反应的化学方程式是:
(4)有人提出②反应产生了有臭有毒的气体,可采用改变反应物的方法使无该气体产生,则②反应的化学方程式是:
此时若要B物质还能循环使用,则C为
(5)BaSO4是因为具有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.现有一定量含有 杂质的
杂质的 试样,用如图的实验装置测定
试样,用如图的实验装置测定 试样的纯度(可供选用的反应物只有
试样的纯度(可供选用的反应物只有 固体、
固体、 盐酸、
盐酸、 硫酸和蒸馏水)。
硫酸和蒸馏水)。
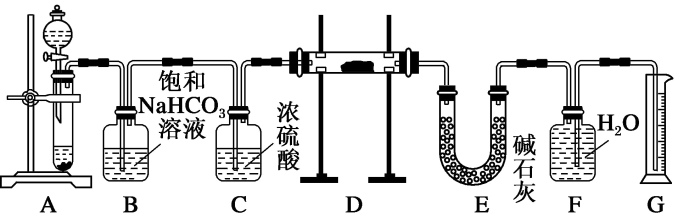
回答下列问题:
(1)装置A中液体试剂选用 盐酸而不选用
盐酸而不选用 硫酸,理由是
硫酸,理由是_______ 。
(2)装置B的作用是_______ ,装置C的作用是_______ ,装置E中碱石灰的作用是_______ 。
(3)装置D中发生反应的化学方程式是_______ 、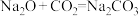 。
。
(4)若开始时测得样品的质量为2.0g,反应结束后测得气体体积为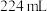 (标准状况),则
(标准状况),则 试样的纯度为
试样的纯度为_______ 。
Ⅱ.某溶液的溶质可能由下列离子组成: 、
、 、
、 、
、 、
、 、
、 ,某同学进行了如下实验:
,某同学进行了如下实验:
①向溶液中加入过量的 溶液,有白色沉淀产生,过滤;
溶液,有白色沉淀产生,过滤;
②向①中滤液里加入 溶液,有白色沉淀产生;
溶液,有白色沉淀产生;
③将①中的沉淀加入稀盐酸中,沉淀部分消失,有气体产生。
(5)依据以上实验可以推断,原溶液中一定含有_______ ;一定没有_______ ;可能含有_______ 。
 杂质的
杂质的 试样,用如图的实验装置测定
试样,用如图的实验装置测定 试样的纯度(可供选用的反应物只有
试样的纯度(可供选用的反应物只有 固体、
固体、 盐酸、
盐酸、 硫酸和蒸馏水)。
硫酸和蒸馏水)。
回答下列问题:
(1)装置A中液体试剂选用
 盐酸而不选用
盐酸而不选用 硫酸,理由是
硫酸,理由是(2)装置B的作用是
(3)装置D中发生反应的化学方程式是
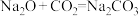 。
。(4)若开始时测得样品的质量为2.0g,反应结束后测得气体体积为
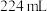 (标准状况),则
(标准状况),则 试样的纯度为
试样的纯度为Ⅱ.某溶液的溶质可能由下列离子组成:
 、
、 、
、 、
、 、
、 、
、 ,某同学进行了如下实验:
,某同学进行了如下实验:①向溶液中加入过量的
 溶液,有白色沉淀产生,过滤;
溶液,有白色沉淀产生,过滤;②向①中滤液里加入
 溶液,有白色沉淀产生;
溶液,有白色沉淀产生;③将①中的沉淀加入稀盐酸中,沉淀部分消失,有气体产生。
(5)依据以上实验可以推断,原溶液中一定含有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】水是一种重要的自然资源,水质优劣直接影响人体健康,水处理技术在生产、生活中应用广泛。聚合硫酸铁(PFS)是水处理中重要的絮凝剂。以黄铁矿的烧渣(主要成分为Fe2O3、FeO、SiO2等)和废铁屑为原料制取聚合硫酸铁([Fe2(OH)x(SO4)3-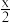 ]m)的工艺流程如图:
]m)的工艺流程如图:
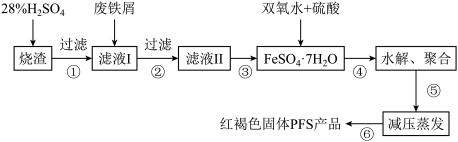
(1)用98%的硫酸配制28%的硫酸,所需的玻璃仪器除量筒外,还有______ (填标号)。
a.容量瓶 b.烧杯 c.玻璃棒 d.分液漏斗
(2)废铁屑表面附有铁锈,铁锈的主要成分为______ ,步骤③的具体实验操作有____ 。
(3)水解、聚合要严控pH和温度。pH偏小时Fe3+水解程度弱,pH偏大时则______ 。写出水解、聚合反应生成PFS的化学方程式:_________ 。
(4)步骤⑥相对于常压蒸发,减压蒸发的优点是_________ 。
(5)污水经过一级、二级处理后,还含有少量Cu2+、Hg2+、Pb2+等重金属离子,可加入沉淀剂使其沉淀。下列物质能作为沉淀剂的是_______ (填标号)。
a.氨水 b.硫化氢气体 c.硫酸钠溶液 d.纯碱溶液
(6)硬度为1°的水是指每升水含10mgCaO或与之相当的物质(如7.1mgMgO)。若某天然水中c(Ca2+)=1.5×10-3mol/L,c(Mg2+)=6.4×10-4mol/L,则此水的硬度为______ 。
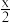 ]m)的工艺流程如图:
]m)的工艺流程如图:
(1)用98%的硫酸配制28%的硫酸,所需的玻璃仪器除量筒外,还有
a.容量瓶 b.烧杯 c.玻璃棒 d.分液漏斗
(2)废铁屑表面附有铁锈,铁锈的主要成分为
(3)水解、聚合要严控pH和温度。pH偏小时Fe3+水解程度弱,pH偏大时则
(4)步骤⑥相对于常压蒸发,减压蒸发的优点是
(5)污水经过一级、二级处理后,还含有少量Cu2+、Hg2+、Pb2+等重金属离子,可加入沉淀剂使其沉淀。下列物质能作为沉淀剂的是
a.氨水 b.硫化氢气体 c.硫酸钠溶液 d.纯碱溶液
(6)硬度为1°的水是指每升水含10mgCaO或与之相当的物质(如7.1mgMgO)。若某天然水中c(Ca2+)=1.5×10-3mol/L,c(Mg2+)=6.4×10-4mol/L,则此水的硬度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】已知: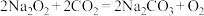 ,某兴趣小组用下图中的实验装置进行实验,验证过氧化钠可作供氧剂。
,某兴趣小组用下图中的实验装置进行实验,验证过氧化钠可作供氧剂。
(1)仪器a的名称为______ 。
(2)A为制取 的装置,锥形瓶中盛放石灰石,则a中盛放的药品为
的装置,锥形瓶中盛放石灰石,则a中盛放的药品为______ (填“盐酸”或“硫酸”)。
(3)B中盛放饱和 溶液,其作用为
溶液,其作用为______ 。
(4)D中盛放NaOH溶液,其作用为______ 。
(5)若有7.8g 参加反应,则理论上可收集到气体的体积为
参加反应,则理论上可收集到气体的体积为______ L(标准状况)。
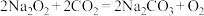 ,某兴趣小组用下图中的实验装置进行实验,验证过氧化钠可作供氧剂。
,某兴趣小组用下图中的实验装置进行实验,验证过氧化钠可作供氧剂。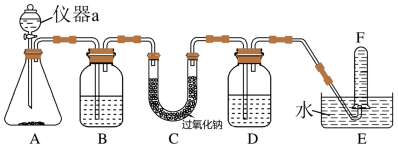
(1)仪器a的名称为
(2)A为制取
 的装置,锥形瓶中盛放石灰石,则a中盛放的药品为
的装置,锥形瓶中盛放石灰石,则a中盛放的药品为(3)B中盛放饱和
 溶液,其作用为
溶液,其作用为(4)D中盛放NaOH溶液,其作用为
(5)若有7.8g
 参加反应,则理论上可收集到气体的体积为
参加反应,则理论上可收集到气体的体积为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】现对0.1 mol/L的纯碱溶液进行相关研究。
(1)用pH试纸测定该溶液的pH,其正确的操作______________________________ 。
(2)由上测得纯碱溶液呈碱性,请用离子方程式表示其原因:_________________ 。
(3)某同学根据所学知识对溶液进行分析,写出了以下四个关系式。请你判断:在正确的关系式后面打“√”,在错误的后面写出正确的关系式。
①c(Na+)=2c( )+2c(
)+2c( )
)________________________________________ ;
②c(Na+)+ c(H+)=2 c( )+ c(
)+ c( )+ c(OH-)
)+ c(OH-)____________________________ ;
③c(OH-)=c( )+c(H2CO3)+c(H+)
)+c(H2CO3)+c(H+)_________________________________ ;
④c(Na+)>c( )> c(OH-)> c(
)> c(OH-)> c( )
) __________________________________ 。
(1)用pH试纸测定该溶液的pH,其正确的操作
(2)由上测得纯碱溶液呈碱性,请用离子方程式表示其原因:
(3)某同学根据所学知识对溶液进行分析,写出了以下四个关系式。请你判断:在正确的关系式后面打“√”,在错误的后面写出正确的关系式。
①c(Na+)=2c(
 )+2c(
)+2c( )
)②c(Na+)+ c(H+)=2 c(
 )+ c(
)+ c( )+ c(OH-)
)+ c(OH-)③c(OH-)=c(
 )+c(H2CO3)+c(H+)
)+c(H2CO3)+c(H+)④c(Na+)>c(
 )> c(OH-)> c(
)> c(OH-)> c( )
)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】I.氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。
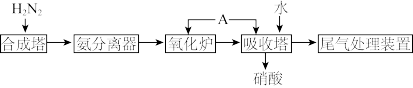
(1)写出氧化炉中的化学反应方程式_______ 。
(2)向吸收塔中通入A的作用_______ 。
(3)工业制硝酸的尾气是酸性气体,实验室模拟该流程时,为防止环境污染,最好选用_______ (填化学式)溶液吸收。
II.为除去KCl溶液中少量的Mg2+、 ,可选用Ba(OH)2、HCl和K2CO3三种溶液按如下步骤操作:
,可选用Ba(OH)2、HCl和K2CO3三种溶液按如下步骤操作:
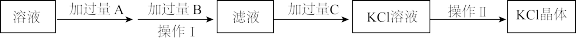
(4)上述试剂中,A是_______ ,C是_______ 。(填化学式)
(5)操作I的名称是_______ 。
(6)加过量A时发生有关反应的离子方程式为_______ 、_______ 。
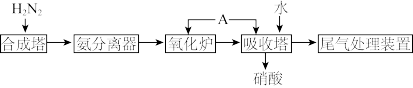
(1)写出氧化炉中的化学反应方程式
(2)向吸收塔中通入A的作用
(3)工业制硝酸的尾气是酸性气体,实验室模拟该流程时,为防止环境污染,最好选用
II.为除去KCl溶液中少量的Mg2+、
 ,可选用Ba(OH)2、HCl和K2CO3三种溶液按如下步骤操作:
,可选用Ba(OH)2、HCl和K2CO3三种溶液按如下步骤操作: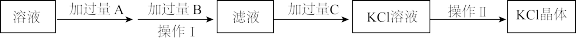
(4)上述试剂中,A是
(5)操作I的名称是
(6)加过量A时发生有关反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学兴趣小组拟采用如下图所示装置(部分夹持装置略去)制取氨基钾(KNH2)。已知氨基钾很容易与空气中的水和二氧化碳反应。
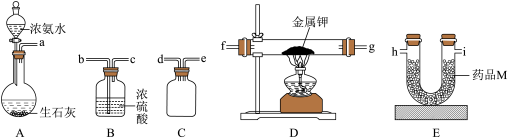
回答下列问题:
(1)A装置装药品前应检验气密性,操作是_______ 。浓氨水与生石灰混合能迅速产生氨气,主要原因是_______ 。
(2)整套装置的连接顺序为a-_______ (装置不重复使用)。
(3)实验开始时应先打开分液漏斗的活塞,再点燃酒精灯,目的是_______ 。药品M为_______ (填字母标号)。
A.无水氯化钙 B.碱石灰 C.五氧化二磷 D.浓硫酸
(4)D中硬质玻璃管内发生反应化学方程式为_______ 。
(5)B装置的作用是_______ 。

回答下列问题:
(1)A装置装药品前应检验气密性,操作是
(2)整套装置的连接顺序为a-
(3)实验开始时应先打开分液漏斗的活塞,再点燃酒精灯,目的是
A.无水氯化钙 B.碱石灰 C.五氧化二磷 D.浓硫酸
(4)D中硬质玻璃管内发生反应化学方程式为
(5)B装置的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】实验室在模拟工业制备和提纯硅时,利用氯气、石英砂和碳粉(过量)等原料按以下装置制备了SiCl4,已知SiCl4熔点-70°C,沸点57.6°C,遇水极易水解。请回答:
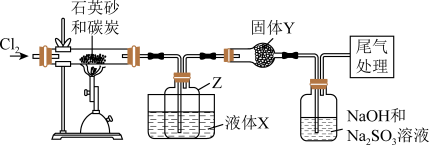
(1)硬质玻璃管中发生的化学反应方程式是___________ 。
(2)液体X可以是冰水吗?___________ (填“可以”或“不可以”),其作用是___________ 。
(3)若缺少干燥管和固体Y,则会造成___________ 。
(4)“尾气处理”的方法是___________ 。

(1)硬质玻璃管中发生的化学反应方程式是
(2)液体X可以是冰水吗?
(3)若缺少干燥管和固体Y,则会造成
(4)“尾气处理”的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】BaCl2·xH2O中结晶水数目可通过重量法来确定:
①称取1.222g样品,置于小烧杯中,加入适量稀盐酸,加热溶解,边搅拌边滴加稀硫酸到沉淀完全,静置;
②过滤并洗涤沉淀;
③将盛有沉淀的滤纸包烘干并中温灼烧;转入高温炉中,反复灼烧到恒重,称得沉淀质量为1.165g。
回答下列问题:
(1)在操作②中,需要先后用稀硫酸和___________ 洗涤沉淀;检验沉淀中氯离子是否洗净的方法是___________ 。
(2)计算BaCl2·xH2O中的x=_________ (要求写出计算过程)。
(3)操作③中,如果空气不充足和温度过高,可能会有部分沉淀被滤纸中的碳还原为BaS,这使x的测定结果_________ (填“偏低”、“偏高”或“不变”)。
①称取1.222g样品,置于小烧杯中,加入适量稀盐酸,加热溶解,边搅拌边滴加稀硫酸到沉淀完全,静置;
②过滤并洗涤沉淀;
③将盛有沉淀的滤纸包烘干并中温灼烧;转入高温炉中,反复灼烧到恒重,称得沉淀质量为1.165g。
回答下列问题:
(1)在操作②中,需要先后用稀硫酸和
(2)计算BaCl2·xH2O中的x=
(3)操作③中,如果空气不充足和温度过高,可能会有部分沉淀被滤纸中的碳还原为BaS,这使x的测定结果
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组同学,用下列各仪器装置制取乙烯,并用过量的氧气将C2H4氧化成CO2和H2O,测定乙烯中碳、氢两种元素的质量比。
回答下列问题:
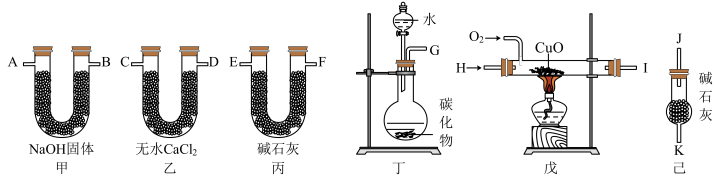
(1)该同学受实验室制备C2H2的启发,拟从CaC2、ZnC2、Al4C3、Mg2C2、Li2C2中选择一种试剂与水反应来制备乙烯,写出该反应的化学方程式:_________________ 。
(2)若产生的气体由左向右流向,各装置导管的连接顺序是:G接E、F接______ 、______ 接______ 、______ 接A、B接J。
(3)装置甲的作用是__________________________________ ;装置己的作用是_________________________________ 。
(4)装置戊中CuO的作用是___________________________ 。
(5)实验前称得甲、乙两装置的质量分别为m1 g和n1 g,实验完毕,称得甲、乙两装置的质量分别变为m2 g和n2 g,则乙烯分子中碳原子和氢原子的原子个数比为______ (列出算式)。
(6)若戊中没有CuO,则测定结果______ (填“偏高”、“偏低”或“不变”,下同);若不接丙装置,则测定结果_____________ 。
回答下列问题:

(1)该同学受实验室制备C2H2的启发,拟从CaC2、ZnC2、Al4C3、Mg2C2、Li2C2中选择一种试剂与水反应来制备乙烯,写出该反应的化学方程式:
(2)若产生的气体由左向右流向,各装置导管的连接顺序是:G接E、F接
(3)装置甲的作用是
(4)装置戊中CuO的作用是
(5)实验前称得甲、乙两装置的质量分别为m1 g和n1 g,实验完毕,称得甲、乙两装置的质量分别变为m2 g和n2 g,则乙烯分子中碳原子和氢原子的原子个数比为
(6)若戊中没有CuO,则测定结果
您最近一年使用:0次
【推荐3】尿素 合成的发展体现了化学科学与技术的不断进步。
合成的发展体现了化学科学与技术的不断进步。
(1)十九世纪初,用氰酸银 与
与 在一定条件下反应制得
在一定条件下反应制得 ,实现了由无机物到有机物的合成。该反应的化学方程式是
,实现了由无机物到有机物的合成。该反应的化学方程式是____________________ 。
(2)二十世纪初,工业上以 和
和 为原料在一定温度和压强下合成尿素。反应分两步:
为原料在一定温度和压强下合成尿素。反应分两步:
ⅰ. 和
和 生成
生成 ;
;
ⅱ. 分解生成尿素。
分解生成尿素。
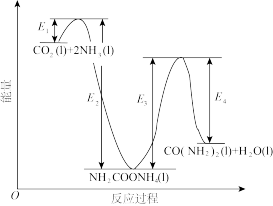
结合反应过程中能量变化示意图,下列说法正确的是__________ (填序号)。
a.活化能:反应ⅰ<反应ⅱ
b.ⅰ为放热反应,ⅱ为吸热反应
c.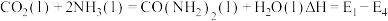
(3)近年研究发现,电催化 和含氮物质(
和含氮物质( 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的
等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的 溶液通
溶液通 至饱和,在电极上反应生成
至饱和,在电极上反应生成 ,电解原理如图所示。
,电解原理如图所示。
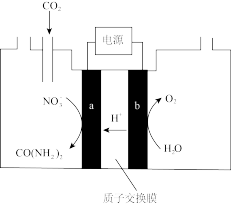
①电极 是电解池的
是电解池的__________ 极。
②电解过程中生成尿素的电极反应式是_____________ 。
(4)尿素样品含氮量的测定方法如下。
已知:溶液中 不能直接用
不能直接用 溶液准确滴定。
溶液准确滴定。

①消化液中的含氮粒子是__________ 。
②步骤ⅳ中标准 溶液的浓度和消耗的体积分别为
溶液的浓度和消耗的体积分别为 和
和 ,计算样品含氮量还需要的实验数据有
,计算样品含氮量还需要的实验数据有__________ 。
 合成的发展体现了化学科学与技术的不断进步。
合成的发展体现了化学科学与技术的不断进步。(1)十九世纪初,用氰酸银
 与
与 在一定条件下反应制得
在一定条件下反应制得 ,实现了由无机物到有机物的合成。该反应的化学方程式是
,实现了由无机物到有机物的合成。该反应的化学方程式是(2)二十世纪初,工业上以
 和
和 为原料在一定温度和压强下合成尿素。反应分两步:
为原料在一定温度和压强下合成尿素。反应分两步:ⅰ.
 和
和 生成
生成 ;
;ⅱ.
 分解生成尿素。
分解生成尿素。
结合反应过程中能量变化示意图,下列说法正确的是
a.活化能:反应ⅰ<反应ⅱ
b.ⅰ为放热反应,ⅱ为吸热反应
c.
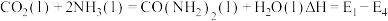
(3)近年研究发现,电催化
 和含氮物质(
和含氮物质( 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的
等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的 溶液通
溶液通 至饱和,在电极上反应生成
至饱和,在电极上反应生成 ,电解原理如图所示。
,电解原理如图所示。
①电极
 是电解池的
是电解池的②电解过程中生成尿素的电极反应式是
(4)尿素样品含氮量的测定方法如下。
已知:溶液中
 不能直接用
不能直接用 溶液准确滴定。
溶液准确滴定。
①消化液中的含氮粒子是
②步骤ⅳ中标准
 溶液的浓度和消耗的体积分别为
溶液的浓度和消耗的体积分别为 和
和 ,计算样品含氮量还需要的实验数据有
,计算样品含氮量还需要的实验数据有
您最近一年使用:0次



