下列叙述不正确的是
| A.同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH相同 |
| B.灼热的铂丝与NH3、O2的混合气接触,铂丝继续保持红热,说明氨的氧化反应是放热反应 |
| C.水结冰的过程不能自发进行的原因是熵减的过程,改变条件也不可能自发进行 |
| D.混乱度减小的吸热反应一定不能自发进行 |
更新时间:2022-01-19 11:16:29
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于反应能量的说法中正确的是
| A.化学反应中的能量变化,都表现为热量的变化 |
| B.化学键的断裂和形成是化学反应中能量变化的主要原因 |
| C.已知4CO(g)+2NO2(g)=4CO2(g)+N2(g)为放热反应,则反应物总能量<生成物总能量 |
| D.相同条件下,如果1mol氢原子所具有的能量为E1, 1 mol 氢分子的能量为E2,则2E1=E2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.放热过程均发生化学反应 |
| B.周期表中第13列元素均为金属元素 |
| C.在过渡元素中可寻找催化剂和耐高温、耐腐蚀的合金材料 |
| D.合成氨反应达到平衡时,正、逆反应速率相等且均为0 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知:如图所指关系,下列关系式正确的是
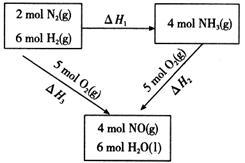

| A.ΔH3=ΔH1+ ΔH2 | B.ΔH1=ΔH2+ΔH3 | C.ΔH3=ΔH1=ΔH2 | D.ΔH2=ΔH1+ ΔH3 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列与化学反应能量变化相关的叙述正确的是
| A.生成物总能量一定低于反应物总能量 |
| B.应用盖斯定律,可计算某些难以直接测量的反应热 |
| C.放热反应的反应速率总是大于吸热反应的反应速率 |
| D.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH不同 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知可逆反应A2(g)+B2(g)  2AB(g) Δ H<0 ΔS<0, ΔG<0,下列说法不正确的是
2AB(g) Δ H<0 ΔS<0, ΔG<0,下列说法不正确的是
 2AB(g) Δ H<0 ΔS<0, ΔG<0,下列说法不正确的是
2AB(g) Δ H<0 ΔS<0, ΔG<0,下列说法不正确的是| A.一般情况下,相同物质的量的不同气体。它们的熵不一样 |
| B.该反应的逆反应ΔG>0,不能自发进行 |
| C.混合气体相对分子质量不变,不能作为判断达到平衡的标准 |
| D.增大压强,平衡可能会发生移动 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列推论正确的是
| A.S(g)+O2(g)=SO2(g)ΔH1,S(s)+O2(g)=SO2(g) ΔH2,则:ΔH1>ΔH2 |
| B.石墨燃烧热为393.5kJ·mol-1,则有2C(s)+O2(g)=2CO(g)ΔH=-393.5kJ·mol-1 |
| C.中和热为57.4kJ/mol,则有Ba(OH)2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(l) ΔH<-114.8kJ/mol |
| D.已知CaCO3(s)=CaO(s)+CO2(g)ΔH>0,该反应任何温度下都能自发进行 |
您最近半年使用:0次



