从废旧铅蓄电池铅膏(含 和
和 等)中回收铅的工艺流程如下:
等)中回收铅的工艺流程如下:

下列说法错误的是
 和
和 等)中回收铅的工艺流程如下:
等)中回收铅的工艺流程如下:
下列说法错误的是
A.流程中 作氧化剂 作氧化剂 |
B.向废铅膏中加入 和 和 后,溶液温度不宜过高 后,溶液温度不宜过高 |
C.“滤液”中溶质主要是 |
| D.电解时,阳极、阴极材料可分别用石墨、铅 |
更新时间:2022-01-19 14:58:13
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】对于下列实验,能正确描述其反应的离子方程式是
| A.硫酸酸化的KI淀粉溶液久置后变蓝:4I-+O2 + 4H+ = 2I2+2H2O |
| B.向CaCl2溶液中通入CO2:Ca2++H2O+CO2 = CaCO3↓+2H+ |
| C.水垢上滴入CH3COOH溶液有气泡产生:CaCO3+2H+ = Ca2++CO2↑+ H2O |
| D.SO2通入漂白粉溶液中产生白色浑浊:SO2+Ca2++2ClO-+H2O = CaSO3↓+2HClO |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知反应4P+CuSO4+H2O→Cu3P+H3PO4+H2SO4(未配平)。下列说法正确的是
| A.Cu3P既是氧化产物又是还原产物 |
| B.7.5molCuSO4可氧化P的物质的量为5.5mol |
| C.还原性:CuSO4>H3PO4 |
| D.参与反应的P和CuSO4的物质的量之比为11:15 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】羟胺(NH2OH)是白色片状晶体,熔点为32.05℃,极易溶于水,受热易分解生成NH3和N2,常用作还原剂,也用作合成抗癌药和农药的原料。羟胺结构可看做是氨分子内的1个氢原子被羟基取代而形成。
已知: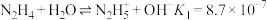 ;
;
 。
。
有关反应的方程式错误的是
已知:
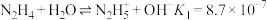 ;
; 。
。有关反应的方程式错误的是
A.羟胺还原 的反应: 的反应: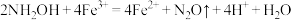 |
B.羟胺分解的反应: |
C.向羟胺溶液中滴加过量稀硫酸: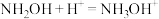 |
D.向(NH4)2SO4溶液中加入NH2OH: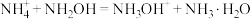 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】基于硫化学的金属硫电池有望替代当前离子电池技术,满足人类社会快速增长的能源需求,该电池的结构及原理如图所示。下列有关叙述正确的是
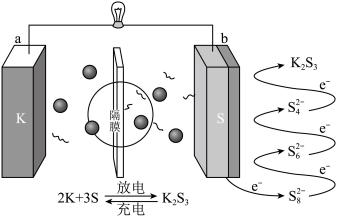

A.充电时,阳极区可能发生的反应有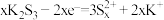 |
| B.充电时,电路中转移1mol电子时,阴极质量增加39g |
C.该电池可采用含有 的水溶液或有机物为电解质 的水溶液或有机物为电解质 |
| D.放电时,a极电势高于b极电势 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知甲、乙都为单质,丙为化合物,能实现下述转化关系。下列说法错误的是
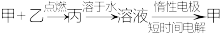
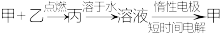
| A.若丙溶于水后得到强碱溶液,则甲可能是O2 |
| B.若溶液丙遇Na2CO3放出气体CO2,则甲可能是H2 |
| C.若溶液丙中滴加NaOH溶液有蓝色沉淀生成,则甲可能为Cu |
| D.若溶液丙中滴加NaOH溶液有白色沉淀生成后沉淀溶解,则甲可能为Al |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】用于测量放射性的NaI晶体需要高纯度,某仪器厂研发了用I2和Na2CO3合成高纯度碘化钠的方法,部分工艺流程如下,已知I2+I-  I
I ,下列说法不正确的是
,下列说法不正确的是
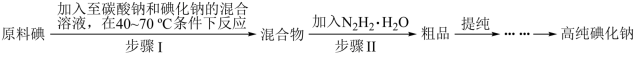
 I
I ,下列说法不正确的是
,下列说法不正确的是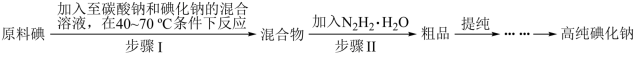
| A.步骤I碘化钠不可多加,否则会降低I2的转化率,且会引入杂质NaI3 |
B.步骤I可能发生的反应的是3I2+3 =5I-+ =5I-+ +3CO2↑ +3CO2↑ |
| C.步骤II使用N2H4·H2O进行还原的原因之一是其产物无毒无害,且不会引入新的杂质 |
| D.步骤I需严格控制温度的原因是:若低于40℃,反应过慢,若高于70 ℃,反应过于激烈难以控制,且碘大量挥发造成损失 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】FeCO3与砂糖混用可以作补血剂,实验室里制备FeCO3的流程如图所示.下列说法错误的是


| A.产品FeCO3在空气中高温分解可得到纯净的FeO |
| B.可利用KSCN溶液检验FeSO4溶液是否变质 |
| C.沉淀过程中有CO2气体放出 |
| D.检验沉淀是否洗涤干净可用盐酸酸化的BaCl2溶液 |
您最近一年使用:0次


 H2↑+Cl2↑
H2↑+Cl2↑ 、
、 、
、 的工业废液中回收铜并制备氯化铁晶体的流程如下,下列说法正确的是
的工业废液中回收铜并制备氯化铁晶体的流程如下,下列说法正确的是
 ,只发生反应
,只发生反应
 ,发生反应的离子方程式为
,发生反应的离子方程式为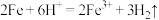
 能与
能与 反应生成
反应生成


