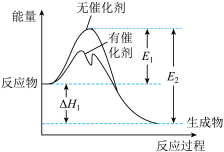
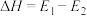下列影响化学反应速率的说法不正确 的是
| A.能发生有效碰撞的分子,一定是活化分子 |
| B.升高温度可以增大活化分子百分数,从而增大单位时间内有效碰撞的次数 |
| C.减小容器体积使压强增大,活化分子百分数不变,单位体积内活化分子数增多 |
| D.增大反应物浓度,反应物中的活化分子百分数增大,单位体积内活化分子数增多 |
更新时间:2022-01-20 11:01:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有关碰撞理论的说法正确的是
| A.增大压强(体积减小)或升高温度,均能增大活化分子百分数,从而加快化学反应速率 |
| B.活化能接近于零的反应,当反应物相互接触时,反应瞬间完成 |
| C.人们把能够发生有效碰撞的分子叫做活化分子,把活化分子具有的能量叫活化能 |
| D.增大反应物浓度,可增大活化分子的百分数,从而使单位时间有效碰撞次数增多 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列因素中,对发生在溶液中且无气体参加的反应的速率不产生显著影响的是
| A.浓度 | B.压强 | C.温度 | D.反应物的性质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某温度下,体积一定的密闭容器中进行如下反应: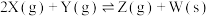
 ,下列叙述正确的是
,下列叙述正确的是
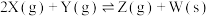
 ,下列叙述正确的是
,下列叙述正确的是| A.加入少量W,逆反应速率增大 |
| B.升高温度,可增大活化分子的百分数,正反应和逆反应速率都增大 |
| C.在容器中加入氦气,压强增大,反应速率增大 |
| D.将容器的体积压缩,可增大活化分子的百分数,有效碰撞次数增大 |
您最近一年使用:0次
【推荐2】CO2和 CH4催化重整可制备合成气,对减缓燃料危机具有重要意义,其反应历程示意图如图:
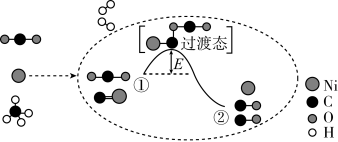
下列说法正确的是

下列说法正确的是
| A.合成气的主要成分为 CO | B.①→②过程可表示为 CO2+NiC=2CO+Ni |
| C.①→②过程吸收能量 | D.Ni在该反应中是中间产物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】某反应的能量与反应历程关系如图所示。下列说法错误的是
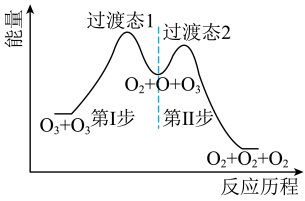

| A.O是反应的中间体 | B.两步反应均为放热反应 |
C. 的稳定性小于 的稳定性小于 | D.第Ⅰ步反应速率比第Ⅱ步的慢 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知分解1 mol H2O2放出热量98 kJ。在含少量I-的溶液中,H2O2分解的机理为:
H2O2+I-→H2O+IO- 慢 H2O2+IO-→H2O+O2+I- 快
下列有关该反应的说法正确的是:
H2O2+I-→H2O+IO- 慢 H2O2+IO-→H2O+O2+I- 快
下列有关该反应的说法正确的是:
| A.I-是该反应的催化剂,所以反应速率与I-浓度无关 |
B.该反应的 =-98 kJ/mol,所以该反应的逆反应活化能一定大于98 kJ/ mol =-98 kJ/mol,所以该反应的逆反应活化能一定大于98 kJ/ mol |
| C.该反应物质之间的速率关系为:v(H2O2)正=v(H2O)正=2v(O2)正 |
D.该反应在通常条件下能够自发进行,是因为 <0,所以一定有 <0,所以一定有 <0 <0 |
您最近一年使用:0次

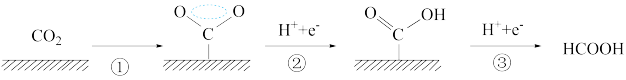
 ,其反应历程的相对能量变化如图所示:
,其反应历程的相对能量变化如图所示:
 代表
代表 吸附在催化剂表面。
吸附在催化剂表面。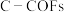 、
、 不影响焓变
不影响焓变 的作用力大于
的作用力大于
 反应过程中的能量变化如图所示,下列有关叙述不正确的是
反应过程中的能量变化如图所示,下列有关叙述不正确的是