实验室有不纯的过氧化钠,欲用排水法测量其纯度,准确称量该样品8.0克装入C装置中。实验操作如下,请完成下列问题:
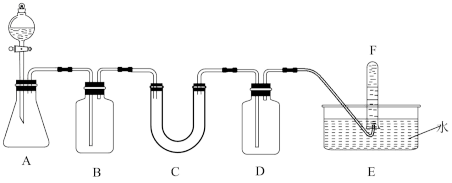
(1)A是实验室常见制备 的装置,锥形瓶内盛有某不溶于水的块状固体,锥形瓶上方盛装盐酸的仪器名称:
的装置,锥形瓶内盛有某不溶于水的块状固体,锥形瓶上方盛装盐酸的仪器名称:_______ , 锥形瓶内发生反应的离子方程式为_______ 。
(2)填写下表中的空白
(3)写出C装置中主要反应的化学方程式:_______ 。
(4)欲检验F中收集的气体,其具体操作步骤及现象:_______ 。
(5)缓缓通入过量的 后,收集到气体为1120.0mL(标准状况下),则过氧化钠的纯度为
后,收集到气体为1120.0mL(标准状况下),则过氧化钠的纯度为_______ %(三位有效数字)。

(1)A是实验室常见制备
 的装置,锥形瓶内盛有某不溶于水的块状固体,锥形瓶上方盛装盐酸的仪器名称:
的装置,锥形瓶内盛有某不溶于水的块状固体,锥形瓶上方盛装盐酸的仪器名称:(2)填写下表中的空白
| 装置编号 | 加入试剂 | 加入该试剂的目的 |
| B | ||
| D |
(4)欲检验F中收集的气体,其具体操作步骤及现象:
(5)缓缓通入过量的
 后,收集到气体为1120.0mL(标准状况下),则过氧化钠的纯度为
后,收集到气体为1120.0mL(标准状况下),则过氧化钠的纯度为
21-22高一上·湖北襄阳·期末 查看更多[3]
湖北省部分市州2021-2022学年高一上学期期末联合调研考试化学试题(已下线)考点13 钠及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)河南省沈丘县长安高级中学2022-2023学年高一上学期期中考试化学试题
更新时间:2022-01-25 08:33:55
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
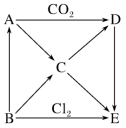
【推荐1】已知A、B、C、D是中学化学中常见物质,它们在一定条件下能发生反应A+B→C+D。
(1)若A是一种能使湿润的红色石蕊试纸变蓝的气体,且该反应是工业上制取硝酸的重要反应之一,该反应的化学方程式为_______ 。
(2)若A是淡黄色粉末,常用作供氧剂,C为强碱,则该反应的化学方程式为_______ 。
(1)若A是一种能使湿润的红色石蕊试纸变蓝的气体,且该反应是工业上制取硝酸的重要反应之一,该反应的化学方程式为
(2)若A是淡黄色粉末,常用作供氧剂,C为强碱,则该反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】有A、B、C三种常见的金属单质,A在空气中燃烧生成淡黄色固体甲;B在空气中加热熔化但不滴落;C在一定条件下与水蒸气反应生成H2和一种黑色固体。
请根据以上信息回答下列问题:
(1)写出下列物质化学式:A_________ B_________ C_________ 甲_________
(2)按要求写出方程式:
①A在空气中燃烧的化学方程式:___________________________________________
②B与氢氧化钠溶液反应的离子方程式:_____________________________________
③C与水蒸气反应的化学方程式:___________________________________________
④甲与水反应的化学方程式:_______________________________________________
请根据以上信息回答下列问题:
(1)写出下列物质化学式:A
(2)按要求写出方程式:
①A在空气中燃烧的化学方程式:
②B与氢氧化钠溶液反应的离子方程式:
③C与水蒸气反应的化学方程式:
④甲与水反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】钠的化合物在生活、生产中有重要应用。化学兴趣小组的同学们为探究 与
与 的性质,设计了如下实验(部分夹持仪器已省略)。
的性质,设计了如下实验(部分夹持仪器已省略)。

请回答下列问题:
(1)装置A中发生反应的化学方程式是_____ ,该实验能验证 具有
具有_____ 的性质。
(2)装置C中所盛放的干燥剂应该选用___________ (填序号)。
A.浓硫酸 B. 固体 C.
固体 C. 固体
固体
(3)U形管内发生反应的化学方程式是___________ ,观察到的现象是___________ 。欲证明该反应中生成的气体,应进行的操作是___________ 。
 与
与 的性质,设计了如下实验(部分夹持仪器已省略)。
的性质,设计了如下实验(部分夹持仪器已省略)。
请回答下列问题:
(1)装置A中发生反应的化学方程式是
 具有
具有(2)装置C中所盛放的干燥剂应该选用
A.浓硫酸 B.
 固体 C.
固体 C. 固体
固体(3)U形管内发生反应的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】将少量稀盐酸滴加到盛有碳酸钙的U形管中,可观察到U形管中的脱脂棉剧烈燃烧。实验装置如图所示,回答下列问题:

(1)稀盐酸与碳酸钙反应的化学方程式是__________________________________________ 。
(2)从脱脂棉的燃烧可以推出 与
与 反应的结论是:
反应的结论是:
a.________________________________________________________________________ ;
b.________________________________________________________________________ 。
(3) 与
与 反应的化学方程式是
反应的化学方程式是___________________________________________ 。

(1)稀盐酸与碳酸钙反应的化学方程式是
(2)从脱脂棉的燃烧可以推出
 与
与 反应的结论是:
反应的结论是:a.
b.
(3)
 与
与 反应的化学方程式是
反应的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某课外活动小组模拟呼吸面具中的反应原理(2Na2O2+2CO2=2Na2CO3+O2)设计并用如图所示的装置(连接胶管及夹持装置均省略)来刺取氧气并测量氧气的体积。图中量气装置E由甲、乙两根玻璃管组成,它们由橡皮管连通,并装入适量水。甲管有刻度(0~50 mL)。供量气用;乙管可上下移动调节液面高低。实验可供选用的药品还有:稀硫酸、盐酸、过氧化钠、碳酸钠、 大理石、水,(已知玻璃纤维可以固定碳酸钙)
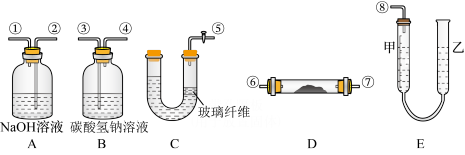
试完成下列问题:
(1)图中各装置接口连接顺序是:⑤_______ ⑧。
(2)装置C中反应的化学反应方程式________ 。
(3)装置A的作用是________ ,反应的方程式为_________ 。
(4)装置B的作用是________ ,反应的方程式为_________ 。
(5)实验结束读取氧气体积时要注意恢复到室温、量气管两端的液面相平,若乙管液面高于甲管液面,会使测得的氧气体积_________ (填“偏大”“偏小”或“无影响”)。若有影响,应向________ (填“上”“下”)移动乙管,使甲乙液面相平(若第一空填无影响,第二空不用填写)。

试完成下列问题:
(1)图中各装置接口连接顺序是:⑤
(2)装置C中反应的化学反应方程式
(3)装置A的作用是
(4)装置B的作用是
(5)实验结束读取氧气体积时要注意恢复到室温、量气管两端的液面相平,若乙管液面高于甲管液面,会使测得的氧气体积
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】某化学兴趣小组查阅文献资料了解到湿法合成高铁酸钾(K2FeO4)是目前人工成本最低、产品纯度最高的合成方法,其合成路线如图:
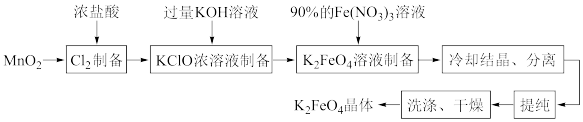
该兴趣小组根据文献资料设计了如图所示装置(部分夹持仪器已省略)制取K2FeO4。
已知:K2FeO4为紫色固体,具有强氧化性;在酸性或中性溶液中快速产生O2,在0℃~5℃、强碱性溶液中较稳定。
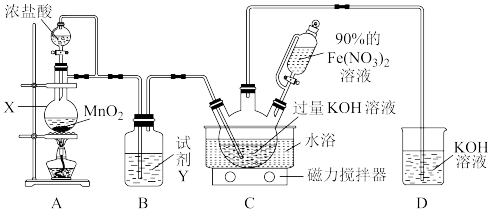
(1)仪器X的名称是_______ 。试剂Y的作用为_______ 。
(2)水浴方式是_______ (填“冷水浴”或“热水浴”)。
(3)装置C中KOH过量的原因是_______ 。
(4)上述流程中,“提纯”所用的方法是_______ 。
(5)称取1.98 g高铁酸钾样品,完全溶解于浓KOH溶液中,再加入足量亚铬酸钾{K[Cr(OH)4]}反应后配成100.00 mL溶液;取上述溶液20.00 mL于锥形瓶中,加入稀硫酸调至pH=2,并加入1 mL苯二胺磺酸钠作指示剂,用1.00 mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定,消耗(NH4)2Fe(SO4)2溶液5.76 mL。测定过程中发生反应:
a. Cr(OH) +FeO
+FeO =Fe(OH)3+CrO
=Fe(OH)3+CrO +OH-
+OH-
b. 2CrO +2H+=Cr2O
+2H+=Cr2O +H2O
+H2O
c. Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O
+6Fe2++14H+=2Cr3++6Fe3++7H2O
则K2FeO4样品的纯度是_______ 。
(6)K2FeO4是一种新型、高效、多功能水处理剂,既能杀菌消毒,又能净化水中悬浮杂质,请解释K2FeO4作为多功能水处理剂的原理:_______ 。
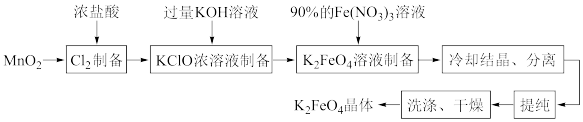
该兴趣小组根据文献资料设计了如图所示装置(部分夹持仪器已省略)制取K2FeO4。
已知:K2FeO4为紫色固体,具有强氧化性;在酸性或中性溶液中快速产生O2,在0℃~5℃、强碱性溶液中较稳定。

(1)仪器X的名称是
(2)水浴方式是
(3)装置C中KOH过量的原因是
(4)上述流程中,“提纯”所用的方法是
(5)称取1.98 g高铁酸钾样品,完全溶解于浓KOH溶液中,再加入足量亚铬酸钾{K[Cr(OH)4]}反应后配成100.00 mL溶液;取上述溶液20.00 mL于锥形瓶中,加入稀硫酸调至pH=2,并加入1 mL苯二胺磺酸钠作指示剂,用1.00 mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定,消耗(NH4)2Fe(SO4)2溶液5.76 mL。测定过程中发生反应:
a. Cr(OH)
 +FeO
+FeO =Fe(OH)3+CrO
=Fe(OH)3+CrO +OH-
+OH-b. 2CrO
 +2H+=Cr2O
+2H+=Cr2O +H2O
+H2Oc. Cr2O
 +6Fe2++14H+=2Cr3++6Fe3++7H2O
+6Fe2++14H+=2Cr3++6Fe3++7H2O则K2FeO4样品的纯度是
(6)K2FeO4是一种新型、高效、多功能水处理剂,既能杀菌消毒,又能净化水中悬浮杂质,请解释K2FeO4作为多功能水处理剂的原理:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】我国长征系列火箭所用的推进剂中的燃料属肼类燃料。某小组在实验室用 溶液和
溶液和 反应制备肼
反应制备肼 ,并进行相关的性质探究实验。
,并进行相关的性质探究实验。
I.制备 (如图所示)
(如图所示) 的名称是
的名称是_______ ,装置A中发生反应的化学方程式为_______ 。
(2)装置C中盛放的试剂是_______ 。写出装置D中产生的氨气的电子式_______ 。
(3)制备 的离子方程式为
的离子方程式为_______ 。
Ⅱ.测定产品中水合肼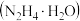 的含量
的含量
(4)称取产品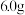 ,加入适量
,加入适量 固体(滴定过程中,调节溶液的
固体(滴定过程中,调节溶液的 保持在6.5左右),加水配成
保持在6.5左右),加水配成 溶液,移取
溶液,移取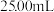 置于锥形瓶中,并滴加2~3滴淀粉溶液,用
置于锥形瓶中,并滴加2~3滴淀粉溶液,用 的碘标准溶液滴定(已知:
的碘标准溶液滴定(已知: )。
)。
①滴定到达终点的现象是_______ 。
②实验测得消耗碘标准溶液的平均值为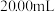 ,产品中水合肼的质量分数为
,产品中水合肼的质量分数为_______ 。
Ⅲ.探究水合肼的还原性与碱性。
将制得的肼分离提纯后,进行如图所示实验。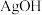 在溶液中不稳定,易分解生成黑色的
在溶液中不稳定,易分解生成黑色的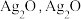 可溶于氨水。
可溶于氨水。
【提出假设】黑色固体可能是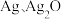 中的一种或两种。
中的一种或两种。
【实验验证】设计如下方案,进行实验:
(5)请完成表中的空白部分。
 溶液和
溶液和 反应制备肼
反应制备肼 ,并进行相关的性质探究实验。
,并进行相关的性质探究实验。I.制备
 (如图所示)
(如图所示)
 的名称是
的名称是(2)装置C中盛放的试剂是
(3)制备
 的离子方程式为
的离子方程式为Ⅱ.测定产品中水合肼
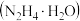 的含量
的含量(4)称取产品
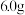 ,加入适量
,加入适量 固体(滴定过程中,调节溶液的
固体(滴定过程中,调节溶液的 保持在6.5左右),加水配成
保持在6.5左右),加水配成 溶液,移取
溶液,移取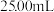 置于锥形瓶中,并滴加2~3滴淀粉溶液,用
置于锥形瓶中,并滴加2~3滴淀粉溶液,用 的碘标准溶液滴定(已知:
的碘标准溶液滴定(已知: )。
)。①滴定到达终点的现象是
②实验测得消耗碘标准溶液的平均值为
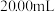 ,产品中水合肼的质量分数为
,产品中水合肼的质量分数为Ⅲ.探究水合肼的还原性与碱性。
将制得的肼分离提纯后,进行如图所示实验。
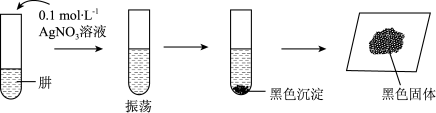
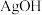 在溶液中不稳定,易分解生成黑色的
在溶液中不稳定,易分解生成黑色的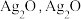 可溶于氨水。
可溶于氨水。【提出假设】黑色固体可能是
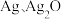 中的一种或两种。
中的一种或两种。【实验验证】设计如下方案,进行实验:
(5)请完成表中的空白部分。
| 操作 | 现象 | 实验结论 |
| i.取少量黑色固体于试管中,加入少量① | 黑色固体部分溶解 | 黑色固体有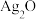 |
| ii.另取少量黑色固体于试管中加入足量稀硝酸,振荡。 | ② | 黑色固体是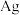 和 和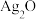 |
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】磷化氢(PH3)是一种剧毒气体,是常用的高效熏蒸杀虫剂,也是一种电子工业原料.
(1)在密闭粮仓放置的磷化铝(AIP)片剂,遇水蒸气放出PH3气体,化学方程式为______
(2)利用反应PH3+3HgCl2=P(HgCl)3↓+3HCl,通过测定溶液______ 变化,可准确测定空气中微量的PH3;其中HgCl2溶于水,所得溶液几乎不导电,则HgCl2属于 ______ (填“共价”或“离子”)化合物.
(3)工业制备PH3的流程如图1所示:

图1
①亚磷酸属于______ 元酸;
②当反应I生成的n(NaH2PO2):n(Na2HPO3)=3:1时,参加反应的n(P4):n(NaOH)=______ .
(4)用漂白粉可将PH3氧化为H3PO4,化学方程式为______ ;含有水蒸气时可加快PH3的氧化过程,用离子方程式表示原因: ______ .
(5)从(4)中的反应产物中回收磷酸氢钙(CaHPO4)的方法如图2:
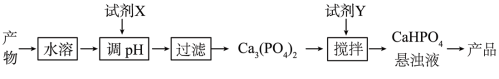
图2
①试剂X为______ (填化学式);
②已知25℃时,H3PO4的Ka1=7.5×10-3、Ka2=6.3×10-8、Ka3=4.4×10-13.
CaHPO4悬浊液pH______ 7(填“>”、“=”或“<”),通过计算说明理由 ______ .
(1)在密闭粮仓放置的磷化铝(AIP)片剂,遇水蒸气放出PH3气体,化学方程式为
(2)利用反应PH3+3HgCl2=P(HgCl)3↓+3HCl,通过测定溶液
(3)工业制备PH3的流程如图1所示:

图1
①亚磷酸属于
②当反应I生成的n(NaH2PO2):n(Na2HPO3)=3:1时,参加反应的n(P4):n(NaOH)=
(4)用漂白粉可将PH3氧化为H3PO4,化学方程式为
(5)从(4)中的反应产物中回收磷酸氢钙(CaHPO4)的方法如图2:
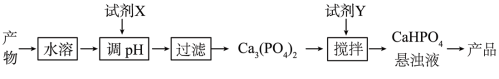
图2
①试剂X为
②已知25℃时,H3PO4的Ka1=7.5×10-3、Ka2=6.3×10-8、Ka3=4.4×10-13.
CaHPO4悬浊液pH
您最近一年使用:0次