电子排布的轨道表示式
(1)电子排布的轨道表示式的定义_______ 。
(2)H、O的基态原子的轨道表示式_______ 。
(3)电子排布的轨道表示式的书写方法_______ 。
(4)概念辨析:简并轨道、单电子、电子对、自旋平行、自旋相反_______ 。
(1)电子排布的轨道表示式的定义
(2)H、O的基态原子的轨道表示式
(3)电子排布的轨道表示式的书写方法
(4)概念辨析:简并轨道、单电子、电子对、自旋平行、自旋相反
更新时间:2022-02-16 18:37:36
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】SOCl2(氯化亚砜)是一种重要的化工原料,是常用的氯化剂,也是制造电池的重要原料。
(1)SOCl2是一种液态化合物,沸点为78.4℃,在水中会剧烈水解。在水解得到的溶液中加入AgNO3溶液可得到白色沉淀,水解产生的气体能使品红溶液褪色。
①SOCl2分子的中心原子杂化方式为___________ 。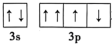 不能表示基态硫原子的价电子轨道表示式,因为违背了
不能表示基态硫原子的价电子轨道表示式,因为违背了___________ 。
②SOCl2的水解方程式为___________ 。
③AlCl3·6H2O加热时得不到AlCl3,但在加入:SOCl2并加热时可得到无水AlCl3,其原因是___________ 。
(2)SOCl2可用于制造心脏起搏器的微型电池。将等物质的量的LiCl、AlCl3溶解在SOCl2溶液中形成电解质溶液,以石墨和锂为电极材料,电池总反应为4Li+2SOCl2=4LiCl+SO2+S,硫和二氧化硫溶解在过量的氯化亚砜电解液中。该电池放电时,Li+移向___________ 极(填“正”或“负”),正极反应式为___________ 。该电池为可充电电池,充电时阴极反应式为___________ 。
(1)SOCl2是一种液态化合物,沸点为78.4℃,在水中会剧烈水解。在水解得到的溶液中加入AgNO3溶液可得到白色沉淀,水解产生的气体能使品红溶液褪色。
①SOCl2分子的中心原子杂化方式为
 不能表示基态硫原子的价电子轨道表示式,因为违背了
不能表示基态硫原子的价电子轨道表示式,因为违背了②SOCl2的水解方程式为
③AlCl3·6H2O加热时得不到AlCl3,但在加入:SOCl2并加热时可得到无水AlCl3,其原因是
(2)SOCl2可用于制造心脏起搏器的微型电池。将等物质的量的LiCl、AlCl3溶解在SOCl2溶液中形成电解质溶液,以石墨和锂为电极材料,电池总反应为4Li+2SOCl2=4LiCl+SO2+S,硫和二氧化硫溶解在过量的氯化亚砜电解液中。该电池放电时,Li+移向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铁是工业部门不可缺少的一种金属,几乎无处不在。根据所学知识回答下列问题:
(1)与铁同周期的所有副族元素的基态原子中,最外层电子数与铁相同的元素有_____ 种。
(2)下列关于铁的说法,正确的是_______ (填选项字母)
A.钢铁的腐蚀以化学腐蚀为主
B. Fe能与很多分子或离子形成配位键
C.基态铁原子的电子排布式不是1s22s22p63s23p103d24s2因为该排布式违反了泡利原理
D.铁属于黑色金属,在周期表中属下ds区元素
(3)某铁的化合物结构简式如下图所示
① 组成上述化合物中属于p区元素的原子第一电离能由大到小的顺序为_________ 。
② 上述化合物中氮原子的杂化方式为_____________ 。
(4)类卤素离子SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是_______ ,原因是___________ ;
(1)与铁同周期的所有副族元素的基态原子中,最外层电子数与铁相同的元素有
(2)下列关于铁的说法,正确的是
A.钢铁的腐蚀以化学腐蚀为主
B. Fe能与很多分子或离子形成配位键
C.基态铁原子的电子排布式不是1s22s22p63s23p103d24s2因为该排布式违反了泡利原理
D.铁属于黑色金属,在周期表中属下ds区元素
(3)某铁的化合物结构简式如下图所示

① 组成上述化合物中属于p区元素的原子第一电离能由大到小的顺序为
② 上述化合物中氮原子的杂化方式为
(4)类卤素离子SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是
您最近一年使用:0次
【推荐1】C、Si元素组成的一些单质或化合物在科研领域中具有重要的作用。请回答下列问题。
(1)硅原子价层电子的轨道表示式中能量最低的是___________。
(2)由C、H、N可以形成化合物 ,C、H、N电负性大小顺序为
,C、H、N电负性大小顺序为___________ 。
(3)Si与一些金属可以形成不同化合物,如图是Si与Al、Li形成的某化合物的晶胞示意图。已知晶胞棱长为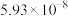 cm,Si与Al之间的共价键键长是
cm,Si与Al之间的共价键键长是___________ cm(只要求列算式,不必计算出数值)。
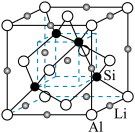
(1)硅原子价层电子的轨道表示式中能量最低的是___________。
A. | B. | C. | D. |
 ,C、H、N电负性大小顺序为
,C、H、N电负性大小顺序为(3)Si与一些金属可以形成不同化合物,如图是Si与Al、Li形成的某化合物的晶胞示意图。已知晶胞棱长为
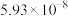 cm,Si与Al之间的共价键键长是
cm,Si与Al之间的共价键键长是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】I.N和Li、Na形成的Li3N、NaN3等化合物具有重要的用途。完成下列填空:
(1)氮原子核外能量最高的电子所处的轨道是:____________ 。锂离子核外电子的轨道表示式是:____________ 。
(2)已知Li3N熔点为845℃,NH3熔点﹣77.7℃,用物质结构的知识说明这两种含氮化合物熔点差异的可能原因____________ 。
II.研究者发明了利用锂循环合成氨的工艺,其流程如下:
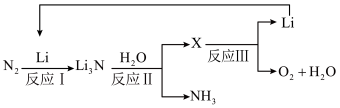
(3)每合成1mol氨,转移电子____________ mol;该过程最终得到的氧化产物是____________ 。
(4)写出反应Ⅱ的化学反应方程式:____________ 。向0.35gLi3N中加入40mL1mol/L的盐酸,所得溶液中离子浓度由大到小的顺序是:____________ 。
(5)由元素周期律能得到____________ (填序号)。
A.碱性:LiOH<NaOH B.与水反应的剧烈程度:Li<Na
C.溶解度:LiOH<NaOH D.密度:Li<Na
(6)NaN3可用于汽车安全气囊,冲撞时发生如下反应:□NaN3+□KNO3→□K2O+□Na2O+□N2↑,配平此反应的化学方程式,并标出电子转移的数目和方向。____________
(1)氮原子核外能量最高的电子所处的轨道是:
(2)已知Li3N熔点为845℃,NH3熔点﹣77.7℃,用物质结构的知识说明这两种含氮化合物熔点差异的可能原因
II.研究者发明了利用锂循环合成氨的工艺,其流程如下:

(3)每合成1mol氨,转移电子
(4)写出反应Ⅱ的化学反应方程式:
(5)由元素周期律能得到
A.碱性:LiOH<NaOH B.与水反应的剧烈程度:Li<Na
C.溶解度:LiOH<NaOH D.密度:Li<Na
(6)NaN3可用于汽车安全气囊,冲撞时发生如下反应:□NaN3+□KNO3→□K2O+□Na2O+□N2↑,配平此反应的化学方程式,并标出电子转移的数目和方向。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。A元素原子中电子只有一种自旋取向;B元素原子最高能级的不同轨道都有电子,且自旋方向相同;C是地壳中含量最高的元素;D核外电子总数是最外层电子数的3倍;E元素只有一个不成对电子;F元素原子最外层只有一个电子,其次外层内的所有轨道的电子均成对。回答下列问题:
(1)六种元素中电负性最大的是______ (填元素符号),B、C、D三种元素的第一电离能由大到小的顺序是______ ,其中D基态原子的核外电子排布式为______ 。
(2)E的基态原子最外层轨道表示式为______ 。E单质与湿润的 反应可制备
反应可制备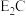 ,其化学方程式为
,其化学方程式为______ 。
(3)F元素有两种常见离子,化合价为+1和+2,从结构上分析F的基态离子中更稳定的是______ ,原因是______ 。
(1)六种元素中电负性最大的是
(2)E的基态原子最外层轨道表示式为
 反应可制备
反应可制备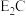 ,其化学方程式为
,其化学方程式为(3)F元素有两种常见离子,化合价为+1和+2,从结构上分析F的基态离子中更稳定的是
您最近一年使用:0次
【推荐1】光伏材料是指能将太阳能直接转换成电能的材料。光伏材料又称太阳能材料,只有半导体材料具有这种功能。可作太阳能电池材料的有单晶硅、多晶硅、非晶硅、 、
、 、
、 、
、 、
、 、
、 等。
等。
(1)指出31号元素镓 在元素周期表中的位置:第
在元素周期表中的位置:第___________ 周期第___________ 族。
(2) 、
、 、
、 电负性从大到小的顺序为
电负性从大到小的顺序为___________ 。
(3) 元素的第一电离能
元素的第一电离能___________ (填“大于”“小于”或“等于”) 元素的第一电离能,原因是
元素的第一电离能,原因是___________ 。
(4)写出原子序数最小的第Ⅷ族元素原子的核外电子排布式:___________ 。
(5)写出 轨道上只有2个未成对电子的元素的符号:
轨道上只有2个未成对电子的元素的符号:___________ 、___________ ;二者电负性:___________ >___________ 。
(6)太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:___________ 。
 、
、 、
、 、
、 、
、 、
、 等。
等。(1)指出31号元素镓
 在元素周期表中的位置:第
在元素周期表中的位置:第(2)
 、
、 、
、 电负性从大到小的顺序为
电负性从大到小的顺序为(3)
 元素的第一电离能
元素的第一电离能 元素的第一电离能,原因是
元素的第一电离能,原因是(4)写出原子序数最小的第Ⅷ族元素原子的核外电子排布式:
(5)写出
 轨道上只有2个未成对电子的元素的符号:
轨道上只有2个未成对电子的元素的符号:(6)太阳能电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】第四周期元素的单质及化合物在工农业生产中应用广泛。
(1)第四周期元素中,基态原子的最外层只有1个电子的元素共有__________ 种。
(2)铂丝蘸取氯化钙在酒精灯上灼烧,火焰呈现砖红色,显色原因是_______ (填序号)。
A.氯化钙受热挥发 B.氯化钙受热分解
C.钙离子中电子跃迁 D.氯离子中电子跃迁
(3)目前市售的发光二极管,其材质以砷化镓(GaAs)为主。镓的基态原子的电子排布式是______________________________________ 。
(4)稼氮砷合金材料的太阳能电池效率达40%,Ga、N、As电负性由大至小的顺序是________ 。As4O6的分子结构如下图所示,其中As原子的杂化方式为_______ 。
(5)已知:Fe(CO)5中Fe元素为0价,在一定条件下发生分解反应Fe(CO)5=Fe(s)+5CO,反应过程中,断裂的化学键只有配位键,形成的化学键是__________ 。
(1)第四周期元素中,基态原子的最外层只有1个电子的元素共有
(2)铂丝蘸取氯化钙在酒精灯上灼烧,火焰呈现砖红色,显色原因是
A.氯化钙受热挥发 B.氯化钙受热分解
C.钙离子中电子跃迁 D.氯离子中电子跃迁
(3)目前市售的发光二极管,其材质以砷化镓(GaAs)为主。镓的基态原子的电子排布式是
(4)稼氮砷合金材料的太阳能电池效率达40%,Ga、N、As电负性由大至小的顺序是

(5)已知:Fe(CO)5中Fe元素为0价,在一定条件下发生分解反应Fe(CO)5=Fe(s)+5CO,反应过程中,断裂的化学键只有配位键,形成的化学键是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Na、Mg、C、N、O、S、Cl等元素单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧产生的黄光是一种___________ 光谱(填“发射”或“吸收”)。
(2)基态碳原子核外电子排布式为___________ ,共有___________ 种能量不同的轨道,其原子核外未成对电子数为___________ 。
(3)N、O、Mg元素的前3级电离能如下表所示:
①、②、③中为氮元素的是___________ (填序号),判断理由是___________ 。
(4)用一个离子方程式说明氯元素和硫元素非金属性的相对强弱:___________ 。
(1)钠在火焰上灼烧产生的黄光是一种
(2)基态碳原子核外电子排布式为
(3)N、O、Mg元素的前3级电离能如下表所示:
| 元素 | 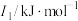 | 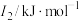 | 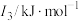 |
| ① | 737.7 | 1450.7 | 7732.7 |
| ② | 1313.9 | 3388.3 | 5300.5 |
| ③ | 1402.3 | 2856.0 | 4578.1 |
(4)用一个离子方程式说明氯元素和硫元素非金属性的相对强弱:
您最近一年使用:0次



