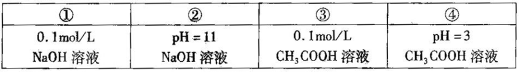
下列溶液中室温下酸性最强的是
A. | B. | C. | D. |
更新时间:2022-01-07 19:49:14
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A.100 mL 0.1 mol·L-1 K2SO4溶液中,含有氧原子数为0.04NA |
| B.1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,转移的电子数为NA |
| C.25 ℃时,1.0 L pH=13的Ba(OH)2溶液中,含有的OH-数目为0.2NA |
| D.100 g 17%的氨水中,含有氨分子数为NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】实验操作规范且能达到目的是
| 目的 | 操作 | |
| A | 取20.00mL盐酸 | 在50mL酸式滴定管中装入盐酸,调整初始读数为30.00mL后,将剩余盐酸放入锥形瓶 |
| B | 清洗碘升华实验所用试管 | 先用酒精清洗,再用水清洗 |
| C | 测定醋酸钠溶液的pH | 用玻璃棒蘸取溶液,点在湿润的pH试纸上 |
| D | 配制浓度为0.010mol·L-1的KMnO4溶液 | 称取KMnO4固体0.15g放入100mL容量瓶中,加水溶解并稀释至刻度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】用0.1000mol/LNaOH溶液滴定20.00mlH2A溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图所示。下列有关说法错误的是


| A.H2A的物质的量浓度为0.1000mol.L-1 |
| B.H2A是二元弱酸 |
| C.a-b段发生反应HA-+OH-=H2O+A2- |
| D.a点时HA-的水解程度大于电解程度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列叙述正确的是
| A.pH=7的溶液一定是中性溶液 |
| B.由水电离出来的H+的浓度为1.0×10-10mol/L,则原溶液的pH=4 |
| C.一定温度下,pH=a的氨水,稀释10倍后,其pH=b,则a=b+1 |
| D.升温纯水的电离程度增大,Kw增大,c(H+)增大,pH值减小,但仍呈中性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】水的离子积常数随着温度的变化关系如下表:
下列说法正确的是
| 温度/℃ | 25 | 50 | 75 | 100 |
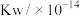 | 1.0 | 5.5 | 20.0 | 56.0 |
A.25℃时, 溶液中, 溶液中, |
B.水的电离度 |
C. 时某溶液的 时某溶液的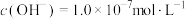 ,该溶液呈中性 ,该溶液呈中性 |
D.纯水中 的大小与温度无关 的大小与温度无关 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
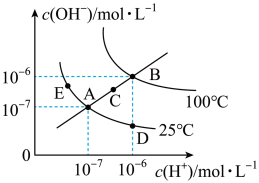
【推荐2】一定温度下,水溶液中 和
和 的物质的量浓度变化曲线如图所示,下列说法不正确的是
的物质的量浓度变化曲线如图所示,下列说法不正确的是
 和
和 的物质的量浓度变化曲线如图所示,下列说法不正确的是
的物质的量浓度变化曲线如图所示,下列说法不正确的是
A.图中五点对应的 间的关系: 间的关系: |
B.从A点到E点,可采用在水中加入少量NaOH或 的方法 的方法 |
C.从A点到D点,所得D点溶液中水电离产生的 的物质的量浓度不可能为 的物质的量浓度不可能为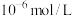 |
| D.若处在B点时,将pH=2的硫酸溶液与pH=10的KOH溶液等体积混合,所得溶液呈中性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知某温度下,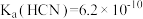 mol·L
mol·L ,
, mol·L
mol·L ,
,
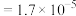 mol⋅L
mol⋅L ,
,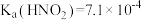 mol⋅L
mol⋅L 。物质的量浓度均为0.1mol⋅L
。物质的量浓度均为0.1mol⋅L 的下列溶液中,pH由大到小的顺序是
的下列溶液中,pH由大到小的顺序是
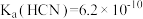 mol·L
mol·L ,
, mol·L
mol·L ,
,
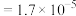 mol⋅L
mol⋅L ,
,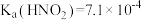 mol⋅L
mol⋅L 。物质的量浓度均为0.1mol⋅L
。物质的量浓度均为0.1mol⋅L 的下列溶液中,pH由大到小的顺序是
的下列溶液中,pH由大到小的顺序是A. |
B.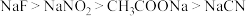 |
C.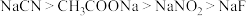 |
D.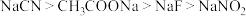 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列各溶液中一定能大量共存的微粒是( )
| A.在80℃pH=1O的溶液中:Na+、CH3CHO、Ag(NH3)2+、NO 3− |
| B.常温下c(H+)=10-14mol/L的溶液中:Na+、AlO 2−、SO 32−、S2- |
| C.加入NH4HCO3固体产生气泡的溶液中:Na+、Mg2+、ClO-、S2- |
| D.含有大量Fe3+的溶液中:Fe2+、Na+、SCN-、Br- |
您最近一年使用:0次

 )> c(
)> c( )> c(H+)
)> c(H+)