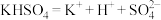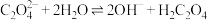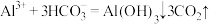用0.1000mol/LNaOH溶液滴定20.00mlH2A溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图所示。下列有关说法错误的是


| A.H2A的物质的量浓度为0.1000mol.L-1 |
| B.H2A是二元弱酸 |
| C.a-b段发生反应HA-+OH-=H2O+A2- |
| D.a点时HA-的水解程度大于电解程度 |
更新时间:2016-12-09 07:18:21
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】对于常温下pH为1的硝酸溶液,下列叙述正确的是
| A.该溶液lmL稀释至100mL后,pH等于3 | B.向pH为1的硝酸溶液中加入等体积、pH为13的氨水恰好完全中和 | C.该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为1×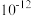 。 。 | D.该溶液中水电离出的c(H+)是pH为3的硝酸中水电离出的c(H+)的100倍 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某研究小组采用三种传感器分别测得氯水光照过程中pH、浓度、体积分数的变化,实验数据如图所示,下列叙述错误的是
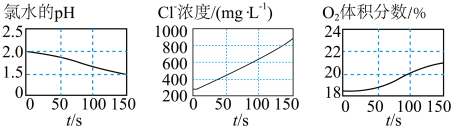

| A.从0s到150s,溶液pH降低的原因是HClO的电离程度增大 |
| B.从0s到150s,溶液中c(H+)增加到起始浓度的100.5倍 |
| C.从50s到150s,Cl-的平均生成速率约为5mg·(L·s)-1 |
| D.HClO光照分解的产物有HCl、O2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列叙述正确的是
| A.pH=7的溶液一定是中性溶液 |
| B.由水电离出来的H+的浓度为1.0×10-10mol/L,则原溶液的pH=4 |
| C.一定温度下,pH=a的氨水,稀释10倍后,其pH=b,则a=b+1 |
| D.升温纯水的电离程度增大,Kw增大,c(H+)增大,pH值减小,但仍呈中性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验方法不能达到相应实验目的的是
| 选项 | 实验目的 | 实验方法 |
| A | 验证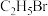 中卤素原子的种类 中卤素原子的种类 | 向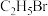 中加入过量的NaOH溶液,加热一段时间后静置,取少量上层清液于试管中,加入 中加入过量的NaOH溶液,加热一段时间后静置,取少量上层清液于试管中,加入 溶液,观察现象 溶液,观察现象 |
| B | 比较 和 和 的热稳定性 的热稳定性 | 分别加热 和 和 固体,将产生的气体通入澄清石灰水,观察现象 固体,将产生的气体通入澄清石灰水,观察现象 |
| C | 验证配位键影响物质的溶解性 | 向NaCl溶液中滴加少量 溶液,产生白色沉淀,继续滴加氨水直至过量,观察现象 溶液,产生白色沉淀,继续滴加氨水直至过量,观察现象 |
| D | 证明某酸 是二元酸 是二元酸 | 用NaOH标准液滴定 溶液,消耗NaOH的物质的量为 溶液,消耗NaOH的物质的量为 的2倍 的2倍 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】对含微量 的某样品进行
的某样品进行 化学定量测定,有以下两种途径,最后均是以淀粉作指示剂,用
化学定量测定,有以下两种途径,最后均是以淀粉作指示剂,用 标准溶液滴定以求得
标准溶液滴定以求得 的浓度。下列分析正确的是
的浓度。下列分析正确的是
已知: 过量
过量
方法一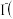 样品
样品

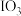 -
-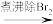
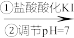

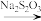

方法二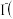 样品
样品
 I2
I2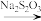

 的某样品进行
的某样品进行 化学定量测定,有以下两种途径,最后均是以淀粉作指示剂,用
化学定量测定,有以下两种途径,最后均是以淀粉作指示剂,用 标准溶液滴定以求得
标准溶液滴定以求得 的浓度。下列分析正确的是
的浓度。下列分析正确的是 已知:
 过量
过量
方法一
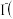 样品
样品

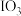 -
-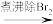
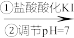

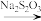

方法二
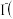 样品
样品
 I2
I2

| A.方法二对样品所做处理操作简便,用作微量的测定更准确 |
| B.当待测液由无色变为蓝色时即达到滴定终点 |
| C.方法一与方法二测量出的样品浓度比为6:l |
D.假设各步骤操作均得当,方法一所消耗 标准溶液的体积是方法二的6倍 标准溶液的体积是方法二的6倍 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】H2A为二元酸,其电离过程为:H2A H++HA-,HA-
H++HA-,HA- H++A2-。常温时,向20mL0.1mol/LH2A水溶液中逐滴滴加0.1mol/LNaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是
H++A2-。常温时,向20mL0.1mol/LH2A水溶液中逐滴滴加0.1mol/LNaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是

 H++HA-,HA-
H++HA-,HA- H++A2-。常温时,向20mL0.1mol/LH2A水溶液中逐滴滴加0.1mol/LNaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是
H++A2-。常温时,向20mL0.1mol/LH2A水溶液中逐滴滴加0.1mol/LNaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是
| A.H2A的Kal的数量级为10-1.2 |
| B.曲线Ⅱ表示A2- |
| C.当溶液中c(H2A)=c(A2-)时,pH=2.7 |
| D.向pH=4.2的溶液中继续滴加NaOH溶液,水的电离程度持续变大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.25℃时,已知Ka(CH3COOH)=1.7×10-5mol·L–1、Ka(C6H5OH)=1.0×10-10mol·L–1、Ka1(H2CO3)=4.2×10-7mol·L–1、Ka2(H2CO3)=5.6×10-11mol·L–1。pH相等的①CH3COONa、②C6H5ONa、③NaHCO3溶液中,c(Na+)大小关系:②<③<① |
| B.常温下,某溶液中由水电离出的c(H+)=1×10-amol·L–1,若a<7时,则该溶液可能为NaHSO4溶液 |
| C.常温下,中和同体积、同pH的硫酸、盐酸和醋酸所需相同浓度的NaOH溶液的体积关系:V(硫酸)>V(盐酸)=V(醋酸) |
| D.常温下,向饱和Na2CO3溶液中加入少量BaSO4粉末,过滤,向洗净的沉淀中加入稀盐酸有气泡产生,说明常温下Ksp(BaSO4)>Ksp(BaCO3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】取两份
 的
的 溶液,一份滴加
溶液,一份滴加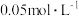 的盐酸,另一份滴加
的盐酸,另一份滴加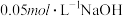 溶液,溶液的pH随加入酸(或碱)体积的变化如图。
溶液,溶液的pH随加入酸(或碱)体积的变化如图。
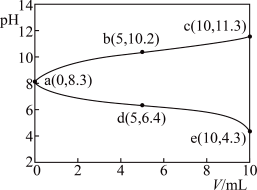
下列说法不正确 的是

 的
的 溶液,一份滴加
溶液,一份滴加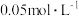 的盐酸,另一份滴加
的盐酸,另一份滴加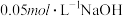 溶液,溶液的pH随加入酸(或碱)体积的变化如图。
溶液,溶液的pH随加入酸(或碱)体积的变化如图。
下列说法
A.由a点可知: 溶液中 溶液中 的水解程度大于电离程度 的水解程度大于电离程度 |
B.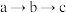 过程中: 过程中: 逐渐减小 逐渐减小 |
C. 过程中: 过程中: |
D.令c点的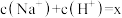 ,e点的 ,e点的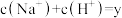 ,则 ,则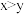 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】一定温度压强下,在容积可变的密闭容器中发生反应CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0,则下列说法不正确的是
CO2(g)+H2(g) ΔH<0,则下列说法不正确的是
 CO2(g)+H2(g) ΔH<0,则下列说法不正确的是
CO2(g)+H2(g) ΔH<0,则下列说法不正确的是| A.其他条件不变,加催化剂与不加催化剂其ΔH 相同 |
| B.当达到平衡,向体系中充入CO2其平衡向左移动 |
| C.理论上该反应可设计成燃料电池,H2O(g)在正极上发生还原反应 |
| D.平衡混合气体通入NaOH溶液恰好反应,升高温度溶液碱性增强,其pH一定增大 |
您最近一年使用:0次

 标准液滴定盐酸(滴加酚酞),滴定终点溶液由无色变为浅红色
标准液滴定盐酸(滴加酚酞),滴定终点溶液由无色变为浅红色 溶液中滴加几滴
溶液中滴加几滴 溶液,溶液由黄色变为血红色
溶液,溶液由黄色变为血红色 悬浊液中滴加适量
悬浊液中滴加适量 溶液,沉淀由黄色转化为黑色
溶液,沉淀由黄色转化为黑色 的
的 溶液中加入加入足量
溶液中加入加入足量 NH4++OH−
NH4++OH− 在熔融态的电离方程式为:
在熔融态的电离方程式为: