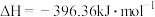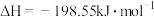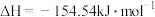制备环氧丙醇的反应如下:
①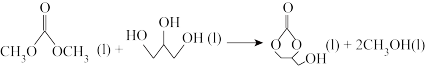

②

③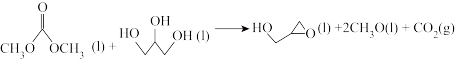
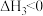
已知上述反应的焓变会随温度变化发生改变,焓变与温度的关系如图,下列说法不正确的是
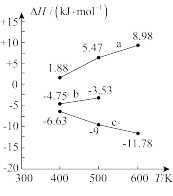
①
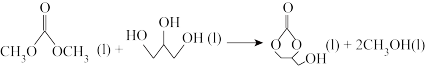

②


③
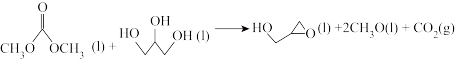
已知上述反应的焓变会随温度变化发生改变,焓变与温度的关系如图,下列说法不正确的是

| A.曲线a代表反应②的焓变 |
B.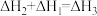 |
C.曲线b在600C对应的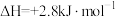 |
| D.曲线c代表反应①的焓变 |
更新时间:2022-03-13 09:55:52
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列六个说法中,正确的有
①已知2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1,则氢气的燃烧热为ΔH=-241.8 kJ·mol-1
②由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
③X(g)+Y(g) Z(g)+W(g) ΔH>0,恒温恒容条件下达到平衡后加入X,上述反应的ΔH增大
Z(g)+W(g) ΔH>0,恒温恒容条件下达到平衡后加入X,上述反应的ΔH增大
④已知:
根据上表数据可以计算出C6H6(g)+3H2(g)→C6H12(g)的焓变
⑤根据盖斯定律,推知在相同条件下,金刚石或石墨燃烧生成1 mol CO2固体时,放出的热量相等
⑥25 ℃、101 kPa时,1 mol碳完全燃烧生成CO2所放出的热量为碳的燃烧热
①已知2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1,则氢气的燃烧热为ΔH=-241.8 kJ·mol-1
②由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
③X(g)+Y(g)
 Z(g)+W(g) ΔH>0,恒温恒容条件下达到平衡后加入X,上述反应的ΔH增大
Z(g)+W(g) ΔH>0,恒温恒容条件下达到平衡后加入X,上述反应的ΔH增大④已知:
| 共价键 | C—C | C=C | C—H | H—H |
| 键能/(kJ·mol-1) | 348 | 610 | 413 | 436 |
⑤根据盖斯定律,推知在相同条件下,金刚石或石墨燃烧生成1 mol CO2固体时,放出的热量相等
⑥25 ℃、101 kPa时,1 mol碳完全燃烧生成CO2所放出的热量为碳的燃烧热
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
【推荐2】肼(H2N~NH2)是一种高能燃料,共价键的键能与热化学方程式信息如下表:
则关于反应 说法正确的是
说法正确的是
| 共价键 | N﹣H | N﹣N | O=O |  | O﹣H |
| 键能/(kJ·mol﹣1) | 391 | 161 | 498 | 946 | 463 |
 说法正确的是
说法正确的是| A.该反应是吸热反应 | B.N2H4(l)比N2H4(g)能量高 |
| C.反应物总能量大于生成物总能量 | D.气态H2O变液态H2O吸热 |
您最近一年使用:0次
【推荐1】已知反应:
(1)CH4(g)+2O2(g)=CO2(g)+2H2O(l) ∆H1=−akJ/mol
(2)CH4(g)+2O2(g)=CO2(g)+2H2O(g) ∆H2=−bkJ/mol。
其他数据如表:
下列说法正确的是
(1)CH4(g)+2O2(g)=CO2(g)+2H2O(l) ∆H1=−akJ/mol
(2)CH4(g)+2O2(g)=CO2(g)+2H2O(g) ∆H2=−bkJ/mol。
其他数据如表:
| 化学键 | C=O | O=O | C‒H | O‒H |
| 键能/(kJ•mol‒1) | 798 | x | 413 | 463 |
| A.∆H1>∆H2 | B.H2O(g)=H2O(l)的∆S<0,∆H=(b−a)kJ/mol |
| C.甲烷燃烧热为-akJ/mol | D.上表中x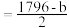 |
您最近一年使用:0次
【推荐2】一定条件下,相关有机物(均为气态)分别与氢气发生加成反应生成1mol气态环己烷的能量变化如图所示:

下列推理错误的是

下列推理错误的是
| A.碳碳双键加氢时放热,放出的热量与碳碳双键数目及相对位置有关 |
B.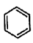 (g)+H2(g)→ (g)+H2(g)→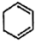 (g) △H=-21kJ·mol-1 (g) △H=-21kJ·mol-1 |
| C.∣△H2∣>∣△H3∣,说明单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定 |
| D.3∣△H1∣>∣△H4∣,说明苯分子中不存在三个完全独立的碳碳双键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知:2H2O(l)=2H2(g)+O2(g) ΔH=+571.0 kJ/mol。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的过程如下:
过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2 kJ/mol
过程Ⅱ:…
过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2 kJ/mol
过程Ⅱ:…
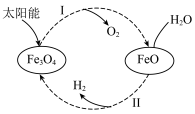
| A.过程Ⅰ中每消耗232 g Fe3O4转移2 mol电子 |
| B.过程Ⅱ的热化学方程式为3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+128.9 kJ/mol |
| C.过程Ⅰ、Ⅱ中能量转化的形式依次是太阳能→化学能→热能 |
| D.铁氧化合物循环制H2具有成本低、产物易分离等优点 |
您最近一年使用:0次
【推荐2】将1molN2O5充入10L恒容密闭容器中,在一定温度下发生下列反应:①2N2O5(g) 2N2O4(g)+O2(g) K1;②N2O4(g)
2N2O4(g)+O2(g) K1;②N2O4(g) 2NO2(g) K2(K1、K2为反应平衡常数)。10min末,该反应达到平衡,此时c(O2)=0.02mol•L-1,c(NO2)=0.06mol•L-1,下列说法正确的是
2NO2(g) K2(K1、K2为反应平衡常数)。10min末,该反应达到平衡,此时c(O2)=0.02mol•L-1,c(NO2)=0.06mol•L-1,下列说法正确的是
 2N2O4(g)+O2(g) K1;②N2O4(g)
2N2O4(g)+O2(g) K1;②N2O4(g) 2NO2(g) K2(K1、K2为反应平衡常数)。10min末,该反应达到平衡,此时c(O2)=0.02mol•L-1,c(NO2)=0.06mol•L-1,下列说法正确的是
2NO2(g) K2(K1、K2为反应平衡常数)。10min末,该反应达到平衡,此时c(O2)=0.02mol•L-1,c(NO2)=0.06mol•L-1,下列说法正确的是| A.N2O5的物质的量分数为20% |
B.若反应N2O5(g) 2NO2(g)+ 2NO2(g)+ O2(g) K3,则K3= O2(g) K3,则K3=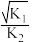 |
| C.v(O2)=0.02mol•L-1•min-1 |
| D.K1•K2=2×10-4 |
您最近一年使用:0次

 2CO
2CO CO+H2
CO+H2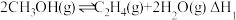
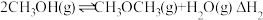
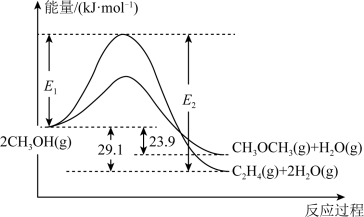
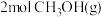 比
比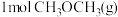 和
和 的总能量低
的总能量低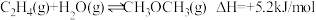
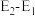 将变小
将变小 下,
下, 水蒸发为水蒸气需要吸热
水蒸发为水蒸气需要吸热
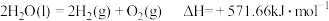
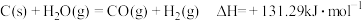
 的反应热为
的反应热为