A、B、C、D、E 代表前 4 周期的五种元素,原子序数依次增大。请填空:
(1)A 元素基态原子的最外层有 3 个未成对电子,次外层有 2 个电子,其电子轨道表示式为_______ 。其原子核外共有_______ 种不同运动状态的电子;其基态原子中最高能量能级轮廓图形状_______ ,其最高能量能级的电子云在空间有_______ 种伸展方向。
(2)B 元素的负一价离子的电子层结构与氩相同,B 离子的结构示意图为_______ 。
(3)C 元素的正三价离子的 3d 能级为半充满,C 的元素符号为_______ ,该元素在周期表中的位置为_______ 。
(4)D 元素基态原子的M 层全充满,N 层没有成对电子,只有一个未成对电子,D 的元素基态原子的电子排布式为_______ ,在元素周期表中的位置为_______ 。
(5)E 元素基态原子中没有未成对电子,E 的价层电子排布式是_______ 。
(1)A 元素基态原子的最外层有 3 个未成对电子,次外层有 2 个电子,其电子轨道表示式为
(2)B 元素的负一价离子的电子层结构与氩相同,B 离子的结构示意图为
(3)C 元素的正三价离子的 3d 能级为半充满,C 的元素符号为
(4)D 元素基态原子的M 层全充满,N 层没有成对电子,只有一个未成对电子,D 的元素基态原子的电子排布式为
(5)E 元素基态原子中没有未成对电子,E 的价层电子排布式是
更新时间:2022-02-21 10:36:05
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】四种短周期元素的性质或结构信息如表。请根据信息回答下列问题。
(1)写出A元素的原子结构示意图_______ ;B与C形成的化合物的电子式_______ (用元素符号表示,下同);D元素形成的单质的结构式_______ 。
(2)比较上述各元素形成的离子的半径大小_______ (用离子符号表示)。
(3)C的一种氧化物可做潜艇中的供氧剂,写出该氧化物与 反应的方程式
反应的方程式_______ 。
(4)A、C两元素金属性较强的是(写元素符号)_______ ,请设计一个实验,证明该结论_______ 。请从原子结构角度解释这两种元素金属性强弱关系_______ 。
(5)写出B的最高价氧化物对应的水化物与D的气态氢化物反应的离子反应方程式_______ 。
| 元素 | A | B | C | D |
| 性质结构信息 | 地壳中含量最多的金属元素;其氧化物具有两性。 | 淡黄色固体;一种单质相对分子质量为256,能溶于 。 。 | 原子半径是短周期主族元素中最大的。 | 其氧化物是汽车尾气的主要有害成分之一,也是空气质量预报的指标之一;该元素在三聚氰胺中含量较高。 |
(2)比较上述各元素形成的离子的半径大小
(3)C的一种氧化物可做潜艇中的供氧剂,写出该氧化物与
 反应的方程式
反应的方程式(4)A、C两元素金属性较强的是(写元素符号)
(5)写出B的最高价氧化物对应的水化物与D的气态氢化物反应的离子反应方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】W、X、Y、Z均为短周期主族元素,W的最外层电子数与核外电子总数之比为3:8;X的核外电子总数与Y的最外层电子数相等,X的原子序数是Z的原子序数的一半;W、Y、Z位于同一周期。
(1)W的单质是一种_______ 色晶体。
(2)W、Y、Z三种元素的气态氢化物稳定性由高到低的顺序是_______ (用化学式表示,Z的气态氢化物与其同主族元素气态氢化物化学式写法相似)。
(3)用化学方程式证明元素原子的得电子能力Y强于W_______
(4)Y的最高价氧化物为无色液体,0.25mol该物质与一定量水混合得到一种稀溶液,并放出QkJ的热量,写出该反应的热化学方程式_______ 。
(5)已知A.B.C.D四种物质存在如下反应关系:A+B C+D
C+D
①若A是Y和Z常见价态的化合物,B是X的氢化物,D是Y的氢化物,反应过程中没有化合价变化,该反应的化学方程式是_______ 。
②若A是Z的单质,B为红色固体,D为紫红色固体单质,高温下发生该反应,C的化学式是_______ 。D与X元素最高价氧化物对应水化物的浓溶液反应,生成的气体会对大气造成污染。用烧碱溶液吸收该气体生成两种盐,其中一种盐可用作防腐剂,烧碱溶液吸收气体的离子方程式是_______ 。
(1)W的单质是一种
(2)W、Y、Z三种元素的气态氢化物稳定性由高到低的顺序是
(3)用化学方程式证明元素原子的得电子能力Y强于W
(4)Y的最高价氧化物为无色液体,0.25mol该物质与一定量水混合得到一种稀溶液,并放出QkJ的热量,写出该反应的热化学方程式
(5)已知A.B.C.D四种物质存在如下反应关系:A+B
 C+D
C+D①若A是Y和Z常见价态的化合物,B是X的氢化物,D是Y的氢化物,反应过程中没有化合价变化,该反应的化学方程式是
②若A是Z的单质,B为红色固体,D为紫红色固体单质,高温下发生该反应,C的化学式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知A、B、C、D、E是五种短周期主族元素,C与E同主族,其原子半径与原子序数的关系如图,且A、B、C、D可形成化合物X。回答下列问题:
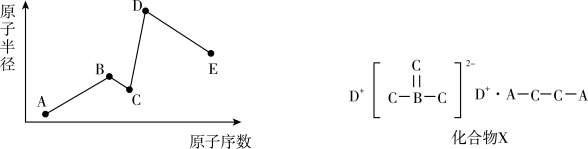
(1)元素E在周期表的位置为第_______ 周期_______ 族,A、B、C、D、E五种元素原子的最外层电子数之和为_______ 。
(2)B、C、E分别形成的最简单氢化物的沸点由高到低的顺序为_______ ;能比较得出B、E的最高价氧化物的水化物酸性强弱的化学反应离子方程式为_______ 。
(3)A、B、C、D、E五种元素中能形成的简单离子中,半径最大的是_______ (填离子符号,下同),半径最小的是_______ 。
(4)C、D形成的一种离子化合物M能与水反应生成C的单质和产物N。M的电子式为_______ ,N中所含有的化学键类型为_______ 。
(5)下列关于化合物X的说法正确的是_______。

(1)元素E在周期表的位置为第
(2)B、C、E分别形成的最简单氢化物的沸点由高到低的顺序为
(3)A、B、C、D、E五种元素中能形成的简单离子中,半径最大的是
(4)C、D形成的一种离子化合物M能与水反应生成C的单质和产物N。M的电子式为
(5)下列关于化合物X的说法正确的是_______。
| A.具有强氧化性 | B.溶于水呈碱性,能促进油污水解 |
C.能使酸性 溶液褪色 溶液褪色 | D.能用于净水,原理与明矾净水相同 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】根据题目要求,回答下列问题:
(1)下列现象和应用与电子跃迁无关的是___ 。
A.激光 B.焰色反应 C.燃烧放热 D.原子光谱
(2)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用__ 形象化描述。
(3)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)__ I1(Cu)(填“大于”或“小于”)。原因是__ 。
(4)ZnF2具有较高的熔点(872℃),其化学键类型是___ ;
(5)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为___ ,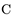 原子的杂化形式为
原子的杂化形式为__ 。
(6)与H2O分子互为等电子体的阴离子为__ 。
(7)[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为__ 。
(8)F2与其他卤素单质反应可以形成卤素互化物,例如ClF3、BrF3等。已知反应Cl2(g)+3F2(g)=2ClF3(g) ΔH=-313kJ/mol,F—F键的键能为159kJ/mol,Cl—Cl键的键能为242kJ/mol,则ClF3中Cl—F键的平均键能为__ kJ/mol。ClF3的熔、沸点比BrF3的__ (填“高”或“低”)。
(1)下列现象和应用与电子跃迁无关的是
A.激光 B.焰色反应 C.燃烧放热 D.原子光谱
(2)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
(3)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)
(4)ZnF2具有较高的熔点(872℃),其化学键类型是
(5)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为
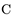 原子的杂化形式为
原子的杂化形式为(6)与H2O分子互为等电子体的阴离子为
(7)[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为
(8)F2与其他卤素单质反应可以形成卤素互化物,例如ClF3、BrF3等。已知反应Cl2(g)+3F2(g)=2ClF3(g) ΔH=-313kJ/mol,F—F键的键能为159kJ/mol,Cl—Cl键的键能为242kJ/mol,则ClF3中Cl—F键的平均键能为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】磷酸亚铁锂( )和锰酸锂(
)和锰酸锂( )均可用作锂离子电池正极材料。回答下列问题:
)均可用作锂离子电池正极材料。回答下列问题:
(1)在周期表中,与Li化学性质最相似的邻族元素是_______ ,画出基态O原子的价电子轨道表示式为_______ 。基态P原子电子占据最高能级的电子云轮廓图为_______ 形。
(2)原子核外电子有两种相反的自旋状态,分别用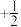 和
和 表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为_______ 。
(3)P的第一电离能与同周期相邻元素相比大小关系为_______ (用元素符号和“>”表示),原因是_______ 。
(4)Fe元素位于周期表的_______ 区。已知: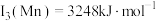 ,
,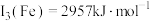 。第三电离能
。第三电离能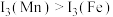 ,其主要原因是
,其主要原因是_______ 。
 )和锰酸锂(
)和锰酸锂( )均可用作锂离子电池正极材料。回答下列问题:
)均可用作锂离子电池正极材料。回答下列问题:(1)在周期表中,与Li化学性质最相似的邻族元素是
(2)原子核外电子有两种相反的自旋状态,分别用
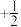 和
和 表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为(3)P的第一电离能与同周期相邻元素相比大小关系为
(4)Fe元素位于周期表的
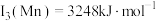 ,
,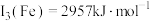 。第三电离能
。第三电离能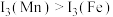 ,其主要原因是
,其主要原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G、H为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)写出BA3的电子式:_________ 。
(2)B元素基态原子中能量最高的电子,其电子云在空间有_____ 个取向,原子轨道呈___ 形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了_____ 。
(4)比较B和D的电负性_________ >_________ (填元素符号)。
(5)G的价电子轨道排布式为_________ 。
(6)H位于_________ 族,__________ 区,该元素的核外电子排布式为__________ 。
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能如下:I1=738kJ/mol、I2=1451kJ/mol、I3=7733kJ/mol、I4=10540kJ/mol |
| D原子价电子层的p轨道半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G是所在周期中未成对电子最多的元素 |
| H在周期表的第七列 |
(1)写出BA3的电子式:
(2)B元素基态原子中能量最高的电子,其电子云在空间有
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(4)比较B和D的电负性
(5)G的价电子轨道排布式为
(6)H位于
您最近一年使用:0次
【推荐1】13发展煤的液化技术被纳入 “十二五”规划,中科院山西煤化所有关煤液化技术的高效催化剂研发项目近日已获批复。已知:煤可以先转化为一氧化碳和氢气,再在催化剂作用下合成甲醇,从而实现液化。
(1)根据等电子原理,写出CO分子的结构式________________ 。
(2)煤炭液化所用的一种催化剂含有铜元素,写出基态铜原子的核外电子排布简式__________ 。
(3)右图是铜的某种氧化物的晶胞结构示意图(顶角和体心是氧),可确定该氧化物的化学式为_______ 。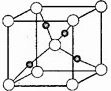
(4)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的结构类似,但NF3不易与Cu2+形成配离子,其主要原因是_____________ 。
(5)煤液化获得甲醇,再经催化氧化可得到重要工业原料甲醛,甲醇的沸点比甲醛的高,其主要原因是____________ ;甲醛分子中碳原子轨道的杂化类型为___________ ; 1mol甲醛分子中σ键的数目为______ 。
(1)根据等电子原理,写出CO分子的结构式
(2)煤炭液化所用的一种催化剂含有铜元素,写出基态铜原子的核外电子排布简式
(3)右图是铜的某种氧化物的晶胞结构示意图(顶角和体心是氧),可确定该氧化物的化学式为

(4)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的结构类似,但NF3不易与Cu2+形成配离子,其主要原因是
(5)煤液化获得甲醇,再经催化氧化可得到重要工业原料甲醛,甲醇的沸点比甲醛的高,其主要原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】钾、氟及锌的相关化合物用途非常广泛。回答下列问题:
(1)基态锌原子的价电子排布式为___________ ;K、F、Zn的电负性从大到小的顺序为___________ 。
(2)Zn与Ca位于同一周期且最外层电子数相等,钙的熔点与沸点均比锌高,其原因是_______________ 。
(3)OF2分子的几何构型为___________ (1分),中心原子的杂化类型为___________ 。
(4)KOH 与O3反应可得到KO3(臭氧化钾),KO3中除σ键外,还存在___________ 。
(5)K、F、Zn组成的一种晶体结构如图所示,其晶胞参数为a=0.4058 nm。
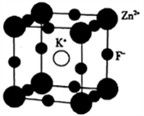
①晶胞中Zn2+的配位数为___________ 个。
②该晶体的密度为___________ (列出算式即可,用NA表示阿伏伽德罗常数的数值)g·cm-3。
(1)基态锌原子的价电子排布式为
(2)Zn与Ca位于同一周期且最外层电子数相等,钙的熔点与沸点均比锌高,其原因是
(3)OF2分子的几何构型为
(4)KOH 与O3反应可得到KO3(臭氧化钾),KO3中除σ键外,还存在
(5)K、F、Zn组成的一种晶体结构如图所示,其晶胞参数为a=0.4058 nm。

①晶胞中Zn2+的配位数为
②该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】亚微米级 复合物多相催化过一硫酸盐降解有机污染物的过程如图所示:
复合物多相催化过一硫酸盐降解有机污染物的过程如图所示:
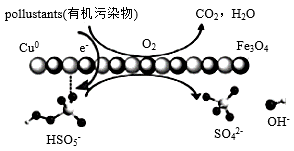
回答下列问题
(1)基态铜原子的M层电子排布式为_______ ,其位于元素周期表的_______ 区。
(2)C、S、H的电负性由大到小的顺序为_______ 。
(3) 中S的价层电子对数为
中S的价层电子对数为_______ ,其空间构型为_______ 。
(4)冰的结构如图所示,则1mol冰中含有_______ mol氢键

(5) 复合物也是有机反应中的催化剂,如
复合物也是有机反应中的催化剂,如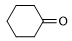


 ,
, 的键角
的键角_______ (填“大于”“小于”或“等于”) 的键角;理由是
的键角;理由是_______ 。
(6)铜的晶胞结构如图,铜原子的配位数为_______ ,若铜原子的半径为a ,则铜晶胞的密度为
,则铜晶胞的密度为_______  。
。

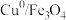 复合物多相催化过一硫酸盐降解有机污染物的过程如图所示:
复合物多相催化过一硫酸盐降解有机污染物的过程如图所示:
回答下列问题
(1)基态铜原子的M层电子排布式为
(2)C、S、H的电负性由大到小的顺序为
(3)
 中S的价层电子对数为
中S的价层电子对数为(4)冰的结构如图所示,则1mol冰中含有

(5)
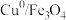 复合物也是有机反应中的催化剂,如
复合物也是有机反应中的催化剂,如


 ,
, 的键角
的键角 的键角;理由是
的键角;理由是(6)铜的晶胞结构如图,铜原子的配位数为
 ,则铜晶胞的密度为
,则铜晶胞的密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】据媒体报道,某公司日前研发出比当前广泛使用的锂电池成本更低、寿命更长、充电速度更快的钠离子电池。该电池的负极材料为Na2Co2TeO6(制备原料为Na2CO3、Co3O4和TeO2),电解液为NaClO4的碳酸丙烯酯溶液。回答下列问题:
(1)Co属于元素周期表中_______ 区元素,其基态原子的价电子排布图为_______ ,和Co同周期的元素中,基态原子具有1个未成对电子的元素有_______ 种。
(2)基态Na原子中,核外电子的空间运动状态有_______ 种,其占据的最高能级电子云轮廓图形状为_______ 。
(3)C、O、Cl的电负性由大到小的顺序为_______ (用“>”连接,下同)。用离子符号表示NaClO4中三种元素所对应的简单离子半径由大到小的顺序为_______ 。第一电离能介于B、N之间的第二周期元素有_______ 种。
(4)O的简单氢化物的沸点比下一周期同主族元素的简单氢化物沸点高,其原因是_______ 。
(5)等电子体是指价电子数和原子数相同的分子、离子或原子团。
①下列各组不互为等电子体的是_______ 。
A.PO 与ClO
与ClO B.CO
B.CO 与NO
与NO C.N2与CN-D.NO2与CS2
C.N2与CN-D.NO2与CS2
②互为等电子体的分子或离子具有相似的化学键特征,请写出CO的结构式_______ 。
(1)Co属于元素周期表中
(2)基态Na原子中,核外电子的空间运动状态有
(3)C、O、Cl的电负性由大到小的顺序为
(4)O的简单氢化物的沸点比下一周期同主族元素的简单氢化物沸点高,其原因是
(5)等电子体是指价电子数和原子数相同的分子、离子或原子团。
①下列各组不互为等电子体的是
A.PO
 与ClO
与ClO B.CO
B.CO 与NO
与NO C.N2与CN-D.NO2与CS2
C.N2与CN-D.NO2与CS2②互为等电子体的分子或离子具有相似的化学键特征,请写出CO的结构式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】镍、铬、铜及其化合物在工业上有广泛的应用,从电镀污泥[含有 、
、 、
、 、
、 和
和 等]中回收制备
等]中回收制备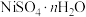 和其它金属及其化合物的工艺流程如图所示。
和其它金属及其化合物的工艺流程如图所示。
 (水相)+2RH(有机相)
(水相)+2RH(有机相)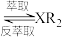 (有机相)
(有机相) (水相)
(水相)
回答下列问题:
(1)与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有________ (填元素符号)。原子核外运动的电子有两种相反的自旋状态,若一种自旋状态用“ ”表示,与之相反的用“
”表示,与之相反的用“ ”表示,“
”表示,“ ”即称为电子的自旋磁量子数。对于基态Ni原子,其价电子自旋磁量子数的代数和为
”即称为电子的自旋磁量子数。对于基态Ni原子,其价电子自旋磁量子数的代数和为________ 。
(2)已知NiO与MgO的晶体结构相同,其中 和
和 的离子半径分别为66pm和69pm。则熔点:NiO
的离子半径分别为66pm和69pm。则熔点:NiO________ MgO(填“>”“<”或“=”),理由是________ 。
(3)滤渣1的主要成分为________ (填化学式)。
(4)电解之后加入碳酸钠调节pH的目的是________ 。
(5)反萃取剂A为________ 。
(6)“反萃取”得到的 溶液,在碱性条件下可被NaClO氧化生成NiOOH沉淀,该反应的离子方程式为
溶液,在碱性条件下可被NaClO氧化生成NiOOH沉淀,该反应的离子方程式为________ 。
(7)资料显示,硫酸镍结晶水合物的形态与温度有如表关系:
由 溶液获得
溶液获得 晶体的操作依次是蒸发浓缩、
晶体的操作依次是蒸发浓缩、________ 、过滤、洗涤、干燥。
 、
、 、
、 、
、 和
和 等]中回收制备
等]中回收制备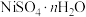 和其它金属及其化合物的工艺流程如图所示。
和其它金属及其化合物的工艺流程如图所示。
 (水相)+2RH(有机相)
(水相)+2RH(有机相)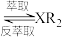 (有机相)
(有机相) (水相)
(水相)回答下列问题:
(1)与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有
 ”表示,与之相反的用“
”表示,与之相反的用“ ”表示,“
”表示,“ ”即称为电子的自旋磁量子数。对于基态Ni原子,其价电子自旋磁量子数的代数和为
”即称为电子的自旋磁量子数。对于基态Ni原子,其价电子自旋磁量子数的代数和为(2)已知NiO与MgO的晶体结构相同,其中
 和
和 的离子半径分别为66pm和69pm。则熔点:NiO
的离子半径分别为66pm和69pm。则熔点:NiO(3)滤渣1的主要成分为
(4)电解之后加入碳酸钠调节pH的目的是
(5)反萃取剂A为
(6)“反萃取”得到的
 溶液,在碱性条件下可被NaClO氧化生成NiOOH沉淀,该反应的离子方程式为
溶液,在碱性条件下可被NaClO氧化生成NiOOH沉淀,该反应的离子方程式为(7)资料显示,硫酸镍结晶水合物的形态与温度有如表关系:
温度 | 低于30.8℃ | 30.8℃~53.8℃ | 53.8℃~280℃ | 高于280℃ |
晶体形态 |
|
| 多种结晶水合物 |
|
 溶液获得
溶液获得 晶体的操作依次是蒸发浓缩、
晶体的操作依次是蒸发浓缩、
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
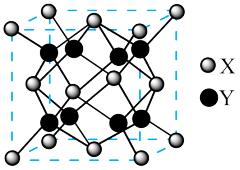
【推荐3】2022年北京冬奥会的“冰立方”是由2008年北京奥运会的“水立方”改造而来,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯 与四氟乙烯
与四氟乙烯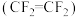 的共聚物
的共聚物 制成。回答下列问题:
制成。回答下列问题:
(1)基态F原子的价电子排布图为_______ 。
(2)固态氟化氢中存在 形式,画出
形式,画出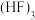 的链状结构
的链状结构_______ 。
(3) 属于
属于_______ (填“极性”或“非极性”)分子, 分子中C的杂化轨道类型为
分子中C的杂化轨道类型为_______ ;聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因:_______ 。
(4)萤石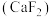 是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是
是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是_______ ;若该立方晶胞参数为 ,正负离子的核间距最小为
,正负离子的核间距最小为_______  。
。
 与四氟乙烯
与四氟乙烯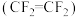 的共聚物
的共聚物 制成。回答下列问题:
制成。回答下列问题:(1)基态F原子的价电子排布图为
(2)固态氟化氢中存在
 形式,画出
形式,画出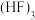 的链状结构
的链状结构(3)
 属于
属于 分子中C的杂化轨道类型为
分子中C的杂化轨道类型为(4)萤石
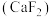 是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是
是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是 ,正负离子的核间距最小为
,正负离子的核间距最小为 。
。
您最近一年使用:0次




