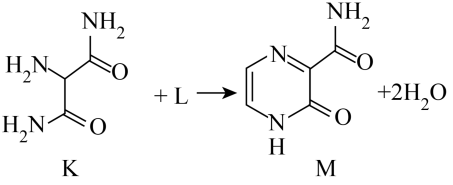
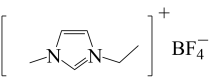
离子液体是在室温或接近室温时呈液态的盐类物质,应用广泛。1-乙基-3-甲基咪唑四氟硼酸盐离子液体结构如图所示,下列相关叙述错误的是

| A.该离子液体的熔沸点低于氯化钠晶体 |
| B.阴离子呈正四面体形,存在共价键和配位键 |
| C.阳离子中σ键数目是π键数目的10倍 |
| D.离子液体难挥发,可用作溶剂 |
更新时间:2022-03-17 21:06:51
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】共价化合物 中所有原子均满足8电子稳定结构,一定条件下可发生反应:
中所有原子均满足8电子稳定结构,一定条件下可发生反应: ,下列说法不正确的是
,下列说法不正确的是
 中所有原子均满足8电子稳定结构,一定条件下可发生反应:
中所有原子均满足8电子稳定结构,一定条件下可发生反应: ,下列说法不正确的是
,下列说法不正确的是A. 中 中 与 与 原子形成 原子形成 键 键 |
B. 中铝原子的杂化方式为 中铝原子的杂化方式为 杂化 杂化 |
C.该反应中 的配位能力大于氯 的配位能力大于氯 |
D. 的结构式为 的结构式为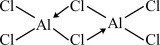 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】钯、铂形成一种化合物如图所示。下列叙述错误的是
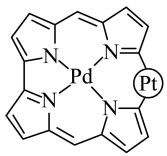

A.该化合物含 键和 键和 键 键 | B.该化合物只含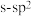 型 型 键 键 |
| C.该化合物含3种短周期元素 | D.电负性: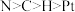 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E是原子序数依次增大的五种常见的短周期主族元素,其中A、B、C、D四种元素的原子序数之和为E元素原子序数的2倍。E是短周期中原子半径最大的元素。A、B、C、D四种元素形成的化合物[CA4]+[BD4]-有多种用途,可用来合成纳米管,还可作杀虫剂、催化剂、助熔剂、阻燃剂等,其结构如图所示。下列说法正确的是
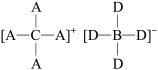
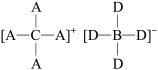
| A.1mol 该物质中存在1mol配位键 |
| B.元素A、C能形成含有非极性键的18电子化合物 |
| C.元素A、E形成的化合物不能与水发生氧化还原反应 |
| D.化合物[CA4]+[BD4]-中各原子均满足8电子稳定结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
A. 和NH3中的H—N—H键角相等 和NH3中的H—N—H键角相等 |
| B.AsH3和Ga(CH3)3晶体类型均为共价晶体 |
| C.NH3和N2H4都是由极性键构成的非极性分子 |
| D.基态砷原子(33As)核外价电子排布式为4s24p3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】由铁及其化合物可制得FeSO4·7H2O、FeCl3、K2FeO4等化工产品,它们在生产、生活中具有广泛应用。已知NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4。高炉炼铁的反应为 Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH=-23.5 kJ· mol-1。下列有关说法不正确的是
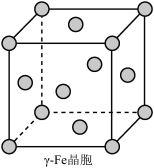

| A.如图所示γFe的晶胞中,铁原子的配位数为12 |
| B.配离子为[Fe(NO)(H2O)5]2+,配位数为6 |
| C.基态铁原子的核外电子排布式为1s22s22p63s23p63d74s1 |
| D.该配合物中阴离子空间结构为正四面体形 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】2023年春季甲流来势凶猛,甲流特效药磷酸奥司他韦结构如图,关于该物质的说法正确的是
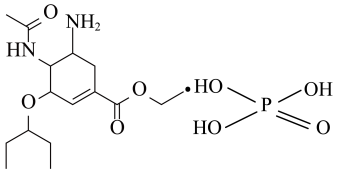

| A.分子中含3种官能团 |
| B.分子中的C=O键能小于C-O键能 |
C. 的空间结构与其VSEPR模型相同 的空间结构与其VSEPR模型相同 |
D.分子中C、N原子均采用 杂化 杂化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E、F为六种原子序数依次增大的短周期元素,A、B、D位于同一主族,且D的原子半径在短周期元素原子中最大,C是周期表中电负性最大的元素,基态E原子的核外电子有7种空间运动状态,基态F原子有3个未成对电子。下列说法正确的是
| A.C的最低价氢化物的沸点低于F的最低价氢化物 |
| B.A元素形成的离子半径小于B元素形成的离子半径 |
| C.A、B、E形成化合物中阴离子中心原子的杂化方式为sp2 |
| D.C、D、E形成的某种化合物能降低冶炼E单质的能耗 |
您最近一年使用:0次

 和
和 的空间结构不同,所以中心S原子杂化方式也不同
的空间结构不同,所以中心S原子杂化方式也不同 键或用来容纳未参与成键的孤电子对,未参与杂化的p轨道可用于形成
键或用来容纳未参与成键的孤电子对,未参与杂化的p轨道可用于形成