粉煤灰矿渣(主要含CaCO3、Al2O3、Fe2O3等)中的铝、铁回收工艺如图:

已知:表中是几种金属阳离子形成氢氧化物沉淀时所需要的pH:
下列说法不正确的是

已知:表中是几种金属阳离子形成氢氧化物沉淀时所需要的pH:
| 金属离子 | Fe3+ | Fe2+ | Al3+ |
| 开始沉淀所需pH最小值 | 2 | 7 | 3 |
| 完全沉淀所需pH最小值 | 3 | 9 | 5 |
| A.“酸浸”步骤中可搅拌以加快反应速率 |
| B.“还原”"步骤中可用SO2将Fe3+还原为Fe,以防止Fe元素在“沉铝”步骤中沉淀析出 |
| C.“沉铝”步骤中最合适的pH为3~5 |
| D.“再生”步骤中的氧化产物为CO2 |
更新时间:2022-03-22 10:44:21
|
相似题推荐
多选题
|
适中
(0.65)
解题方法
【推荐1】碳酸铈[ ]是一种优良的环保材料,可用作汽车尾气的净化催化剂。磷铈镧矿中铈(Ce)主要以
]是一种优良的环保材料,可用作汽车尾气的净化催化剂。磷铈镧矿中铈(Ce)主要以 形式存在,还含有
形式存在,还含有 、
、 、
、 、
、 等物质。以磷铈镧矿为原料制备
等物质。以磷铈镧矿为原料制备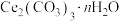 的工艺流程如下,下列说法正确的是
的工艺流程如下,下列说法正确的是

 ]是一种优良的环保材料,可用作汽车尾气的净化催化剂。磷铈镧矿中铈(Ce)主要以
]是一种优良的环保材料,可用作汽车尾气的净化催化剂。磷铈镧矿中铈(Ce)主要以 形式存在,还含有
形式存在,还含有 、
、 、
、 、
、 等物质。以磷铈镧矿为原料制备
等物质。以磷铈镧矿为原料制备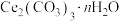 的工艺流程如下,下列说法正确的是
的工艺流程如下,下列说法正确的是
| A.“焙烧”时可使用陶瓷容器 |
| B.滤渣Ⅰ的成分只有2种 |
| C.“除铝”过程中的絮凝剂可以是硅酸胶体 |
D.“沉铈”过程离子方程式为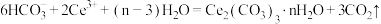 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】工业上以铬铁矿(主要成分为FeCr2O4,含有MgO、Al2O3等杂质)为主要原料制备K2Cr2O7的工艺流程如图(部分操作和条件略):

已知:
①100g水中溶解度数据如表所示。
②Cr2O +H2O
+H2O 2CrO
2CrO +2H+
+2H+
下列说法错误的是

已知:
①100g水中溶解度数据如表所示。
| 物质 | 20℃ | 40℃ | 50℃ | 80℃ | 100℃ |
| K2Cr2O7/g | 12.0 | 29.0 | 37.0 | 73.0 | 102.0 |
| Na2SO4/g | 19.5 | 48.8 | 46.2 | 43.7 | 42.5 |
 +H2O
+H2O 2CrO
2CrO +2H+
+2H+下列说法错误的是
| A.“高温煅烧”中Na2O2做氧化剂 |
| B.“调pH”时应加过量硫酸以保证除杂效果 |
| C.“沉铬”时应蒸发浓缩、冷却至40℃后过滤得K2Cr2O7晶体 |
| D.“沉铬”后滤液可回到“水浸”过程循环利用 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】Co3O4是制备石墨烯电池正极材料LiCoO2的原料。以钴矿石(主要成分为Co3S4,含有少量FeO、Fe2O3、Al2O3等杂质)为原料制取Co3O4的工艺流程如图:
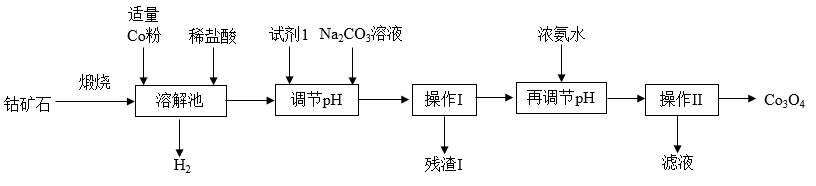
已知:Co与Fe为活泼金属,氧化性由强到弱的顺序为:Co3+>Fe3+>Co2+。
几种氢氧化物的溶度积如下表:
下列有关说法错误的是

已知:Co与Fe为活泼金属,氧化性由强到弱的顺序为:Co3+>Fe3+>Co2+。
几种氢氧化物的溶度积如下表:
| 氢氧化物 | Co(OH)2 | Fe(OH)2 | Co(OH)3 | Al(OH)3 | Fe(OH)3 |
| 溶度积(Ksp) | 2.0×10-15 | 8.0×10-16 | 2.0×10-44 | 1.3×10-33 | 4.0×10-39 |
| A.溶解池中生成H2的离子反应方程式为:Co+2H+=Co2++H2↑ |
| B.加入试剂1的目的是将Fe2+氧化为Fe3+,试剂1可选用双氧水或碘水 |
| C.残渣1的主要成分为Fe(OH)3 |
| D.操作Ⅱ包括过滤、洗涤、干燥和灼烧四个步骤 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】某矿石的主要成分为MgCO3,还含有CaO、SiO2、Fe3O4、Al2O3及少量其它杂质。某工厂采用该矿石为主要原料生产碱式碳酸镁,流程如下(已知:温度低于700℃时,SiO2不会与CaO等反应)。下列有关说法不正确的是
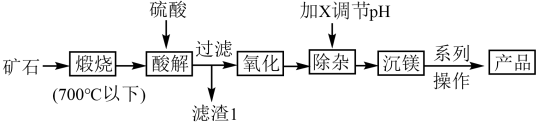

A.煅烧过程所发生的主要化学反应方程式为: |
| B.滤渣1的成分是SiO2 |
C.氧化步骤发生反应的离子方程式可以是: |
| D.加X调pH的X是氢氧化钠 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】废铁屑制取Fe2O3的流程如图:下列说法不正确的是


| A.热的纯碱液可以除去废铁屑表面的油污 |
| B.操作a是萃取 |
| C.冰水可以换为温水或热水 |
| D.Fe2O3可以用作红色颜料 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】硫化氢(H2S)是一种有毒、有害的不良气体。处理某废气中的 ,是将废气与空气混合通入
,是将废气与空气混合通入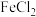 、
、 、
、 的混合液中,其转化的流程如图所示。下列说法正确的是
的混合液中,其转化的流程如图所示。下列说法正确的是

 ,是将废气与空气混合通入
,是将废气与空气混合通入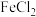 、
、 、
、 的混合液中,其转化的流程如图所示。下列说法正确的是
的混合液中,其转化的流程如图所示。下列说法正确的是
A.转化过程中参与循环的离子有 、 、 、 、 |
| B.转化过程有四种元素的化合价发生了变化 |
C.氧化性由强到弱的顺序: |
D.过程Ⅲ中发生的反应为 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】用FeCl3溶液刻蚀印刷电路板,发生反应: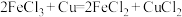 。分别取适量刻蚀后的溶液进行实验,下列实验结论一定正确的是
。分别取适量刻蚀后的溶液进行实验,下列实验结论一定正确的是
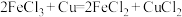 。分别取适量刻蚀后的溶液进行实验,下列实验结论一定正确的是
。分别取适量刻蚀后的溶液进行实验,下列实验结论一定正确的是| A.通入Cl2,再滴入KSCN溶液,溶液变红,说明所得溶液中不含Fe2+ |
| B.加入铁粉,充分反应,有固体剩余,说明所得溶液中不含Fe3+ |
C.滴加足量稀硝酸,充分反应,则所得溶液中 |
D.滴加足量NaOH溶液,充分反应[不考虑Fe(OH)2的氧化],则所得沉淀中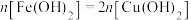 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
| 选项 | 实验 | 现象 | 结论 |
| A | 向稀硝酸中加入过量铁粉,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈血红色 | 稀硝酸将Fe氧化为Fe3+ |
| B | 向1.0 mol/L Fe2(SO4)3溶液中加入铜粉 | 溶液变蓝、有黑色固体出现 | 金属铁比铜活泼 |
| C | 用铂丝蘸取少量某溶液进行焰色反应 | 火焰呈黄色 | 该溶液含钠元素 |
| D | 蘸有浓氨水的玻璃棒靠近某溶液 | 有白烟产生 | 该溶液可能是浓盐酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】氧钒(Ⅳ)碱式碳酸铵晶体{ }难溶于水,可用于制备热敏材料
}难溶于水,可用于制备热敏材料 。已知+4价钒的化合物易被氧化,实验室以
。已知+4价钒的化合物易被氧化,实验室以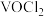 和
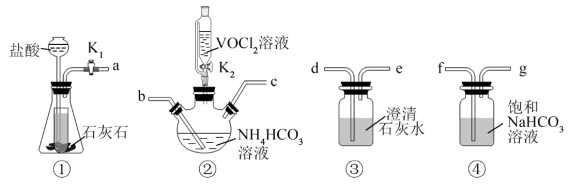
和 为原料制备氧钒(Ⅳ)碱式碳酸铵晶体的装置如图所示。下列说法正确的是
为原料制备氧钒(Ⅳ)碱式碳酸铵晶体的装置如图所示。下列说法正确的是
 }难溶于水,可用于制备热敏材料
}难溶于水,可用于制备热敏材料 。已知+4价钒的化合物易被氧化,实验室以
。已知+4价钒的化合物易被氧化,实验室以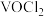 和
和 为原料制备氧钒(Ⅳ)碱式碳酸铵晶体的装置如图所示。下列说法正确的是
为原料制备氧钒(Ⅳ)碱式碳酸铵晶体的装置如图所示。下列说法正确的是
A.按气流方向从左往右,各装置接口为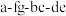 |
| B.装置①的优点是节约原料且能随开随用、随关随停 |
| C.实验时需先关闭K2,打开K1,待③中出现浑浊,再打开K2,关闭K1 |
D.装置②发生反应的离子方程式为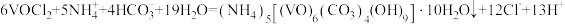 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:

下列说法中正确的是

下列说法中正确的是
| A.步骤①中可通过加入氯化铵溶液去除废铁屑表面的油污 |
| B.步骤②中可采取水浴加热方式 |
| C.步骤③中H2O2可替换为稀硝酸溶液 |
| D.步骤⑤的具体实验操作为蒸发浓缩、降温结晶、过滤、洗涤,干燥后得到硫酸铁铵晶体 |
您最近一年使用:0次

 、ZnS、CuS及少量的
、ZnS、CuS及少量的 。某实验小组以该废催化剂为原料,回收锌和铜,设计实验流程如图:
。某实验小组以该废催化剂为原料,回收锌和铜,设计实验流程如图:

 可以选用KSCN溶液
可以选用KSCN溶液 ,然后不断搅拌下缓慢加入
,然后不断搅拌下缓慢加入


 尽快干燥,防止被空气氧化
尽快干燥,防止被空气氧化

