某无色透明溶液中可能大量存在 、
、 、
、 、
、 、
、 中的几种。请回答下列问题:
中的几种。请回答下列问题:
(1)不做任何实验就可以肯定原溶液中不存在的离子是___________ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是___________ 。
(3)取(2)中的滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有___________ ,生成沉淀的离子方程式为___________ 。
(4)原溶液可能大量共存的阴离子是___________ (填字母)。
a. b.
b. c.
c. d.
d.
 、
、 、
、 、
、 、
、 中的几种。请回答下列问题:
中的几种。请回答下列问题:(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取(2)中的滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有
(4)原溶液可能大量共存的阴离子是
a.
 b.
b. c.
c. d.
d.
19-20高一·山东聊城·阶段练习 查看更多[29]
湖南省株洲市炎陵县第一中学等2校2022-2023学年高一下学期3月月考化学试题江西省南昌市知行中学2021-2022学年高一上学期期中化学试题重庆市青木关中学校2020-2021学年高一上学期12月月考化学试题陕西省咸阳市武功县2020-2021学年高一上学期期中质量检测化学试题重庆市万州第二高级中学2021-2022学年高一上学期期中考试化学试题黑龙江省肇东市第四中学2021-2022学年高一上学期期中考试化学试题海南省北京师范大学万宁附属中学2021-2022学年高一上学期第一次月考化学试题辽宁省朝阳市建平县实验中学2021-2022学年高一上学期第一次月考化学试题黑龙江省齐齐哈尔市第二十四中学2021-2022学年高一上学期第一次月考化学试题辽宁省清原满族自治县第二高级中学2020-2021学年高一上学期期中考试化学试题(已下线)3.2.5 离子反应的应用(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)黑龙江省齐齐哈尔市齐齐哈尔中学2020-2021学年高一上学期期中考试化学试卷河北省石家庄市第四中学2020-2021学年高一上学期期中考试化学试题湖南省湘潭市第一中学2020-2021学年高一上学期期中考试化学试题重庆市朝阳中学2020-2021学年高一上学期期中考试化学试题河南省开封市五县2020-2021学年高一上学期期中联考化学试题(已下线)【南昌新东方】13. 2020 高一上 莲塘二中 期中 程秀丽(已下线)【浙江新东方】hzomo化学001(已下线)【浙江新东方】17吉林省长春市长春外国语学校2020-2021学年高一上学期期中考试化学(文科)试题广东省肇庆市肇庆市实验中学2020-2021学年高一上学期开学考试化学试题湖北省黄石市育英高中2020-2021学年高一9月月考化学试题黑龙江省哈尔滨师范大学附属中学2020—2021学年高一上学期第一次月考化学试题江苏省南通市海安县2020-2021学年高一上学期第一次月考化学试题黑龙江省哈尔滨师范大学附属中学2020-2021学年高一10月月考化学试题(已下线)3.2.3 离子反应练习(1)——《高中新教材同步备课》(苏教版 必修第一册)步步为赢 高一化学寒假作业:作业五 离子反应湖南省张家界市慈利县2019-2020学年高一上学期期中考试化学试题山东省临清市第二中学2019-2020学年高一上学期10月月考化学试题
更新时间:2022-03-30 22:30:03
|
相似题推荐
【推荐1】Cr2O3(铬绿)是一种高级绿色颜料,工业上以铬铁矿(主要成分为Cr2O3、SiO2、Al2O3、Fe2O3)为原料制备Cr2O3的工艺流程如图所示:
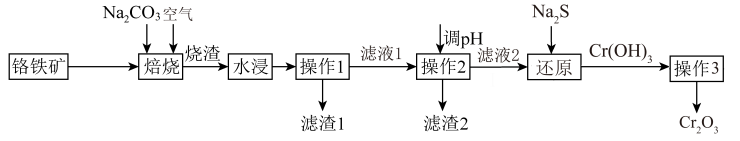
已知:焙烧可将Al、Si的氧化物转化为可溶性钠盐。
回答下列问题:
(1)为加快焙烧速率和提高原料的利用率,可采取的措施为_______ (写出一种即可)。
(2)“滤渣1”的主要成分是_______ 实验室中进行“操作3”时,下列仪器不需要用到的是_______ (填仪器名称)。
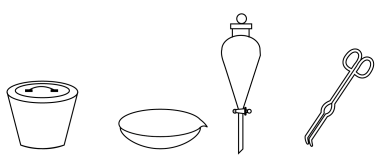
(3)已知“滤液1”中铬元素的存在形式为Na2CrO4,则Cr2O3 “焙烧”时反应的化学方程式为_______ 。
(4)常温下,溶液中部分离子的物质的量浓度的对数lgc与pH的关系如图所示。已知溶液中离子浓度 时认为沉淀完全。
时认为沉淀完全。
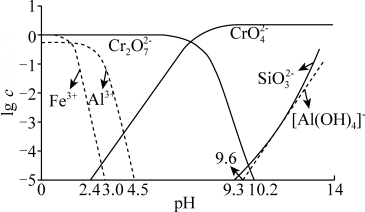
“滤液1”需加_______ (填酸试剂或碱试剂)“调pH”到最佳范围_______ 以除去杂质。“调pH”时铝元素转化的离子方程式为_______ 。
(5)如图以Na2CrO4溶液为原料,用电化学法制备重铬酸钠(已知离子交换膜只有Na+可以自由通过)。
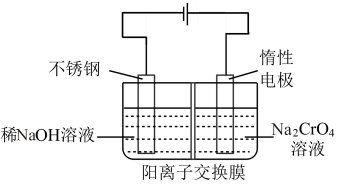
除电极反应外,阳极区发生反应的离子方程式为_______ ;电解一段时间后,若测得生成1 mol Na2Cr2O7,则理论上阴极区溶液质量的变化为_______ 。

已知:焙烧可将Al、Si的氧化物转化为可溶性钠盐。
回答下列问题:
(1)为加快焙烧速率和提高原料的利用率,可采取的措施为
(2)“滤渣1”的主要成分是

(3)已知“滤液1”中铬元素的存在形式为Na2CrO4,则Cr2O3 “焙烧”时反应的化学方程式为
(4)常温下,溶液中部分离子的物质的量浓度的对数lgc与pH的关系如图所示。已知溶液中离子浓度
 时认为沉淀完全。
时认为沉淀完全。
“滤液1”需加
(5)如图以Na2CrO4溶液为原料,用电化学法制备重铬酸钠(已知离子交换膜只有Na+可以自由通过)。

除电极反应外,阳极区发生反应的离子方程式为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】三氧化二砷(俗称砒霜,分子式As2O3)微溶于水。主要用于提炼单质砷及冶炼砷合金和制造半导体。从硫化神渣(含As2S3、CuS、Bi2S3)中回收As2O3的流程如下:
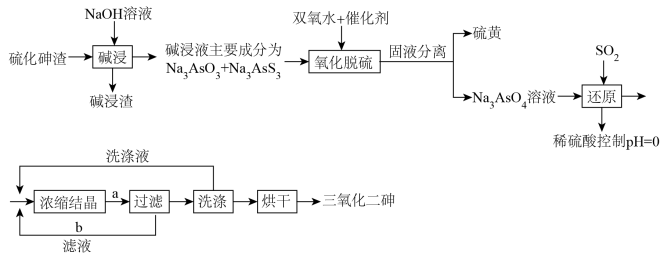
回答下列问题:
(1)“碱浸”时,As2S3反应生成Na3AsO3和Na3AsS3的离子方程式为___________ ,该工序需要将硫化砷渣粉碎,其目的是___________ ;碱浸渣的主要成分为___________ (写化学式)。
(2)“氧化脱硫”时,Na3AsS3反应的化学方程式为___________ 。
(3)下列有关硫黄的性质和用途的说法错误的是___________ (填字母)。
a.不溶于水,易溶于乙醇 b.可用于制造农药、火柴、火药
c.易溶于二硫化碳 d.硫黄在空气中燃烧时产生苍白色火焰
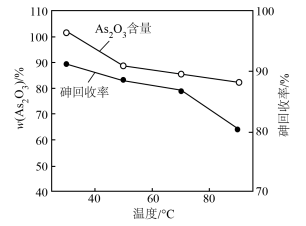
(4)“还原”时,反应的离子方程式为___________ ;该过程中,反应温度对产物中As2O3含量和砷的回收率的影响如图所示。随着温度升高,As2O3含量和砷的回收率逐渐降低的原因可能是___________ (写一点即可)。
(5)设计流程a、b的目的是___________ 。

回答下列问题:
(1)“碱浸”时,As2S3反应生成Na3AsO3和Na3AsS3的离子方程式为
(2)“氧化脱硫”时,Na3AsS3反应的化学方程式为
(3)下列有关硫黄的性质和用途的说法错误的是
a.不溶于水,易溶于乙醇 b.可用于制造农药、火柴、火药
c.易溶于二硫化碳 d.硫黄在空气中燃烧时产生苍白色火焰
(4)“还原”时,反应的离子方程式为

(5)设计流程a、b的目的是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】数形结合思想是化学学科的重要思维模式,请结合所学知识和图像作答:
I.完成下列问题:
(1)如图为含氯元素物质的“价类二维图”
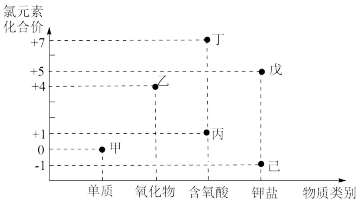
戊的化学式为______ 。
(2)将丁的水溶液滴入到碳酸氢钠溶液中的的离子方程式为______ 。
(3)下列说法正确的是______ 。
II.某实验小组向100mLFeI2溶液中通入Cl2,溶液中Fe3+、I2的物质的量随通入的Cl2的物质的量变化如图所示(不考虑与水的反应)。请回答下列问题:

(4)从开始通入Cl2到n(Cl2)=0.12mol时,溶液中: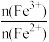 =
=_____ 。
(5)通入足量氯气反应的化学方程式为:______ 。
III.把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生1.16g白色沉淀,再向所得悬浊液中逐滴加入1.00mol/LHCl溶液,加入HCl溶液的体积与生成沉淀的关系如图。试回答:
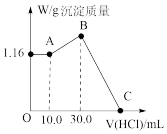
(6)A点的沉淀物的化学式为______ 。
(7)C点消耗HCl溶液的体积为______ mL。
I.完成下列问题:
(1)如图为含氯元素物质的“价类二维图”

戊的化学式为
(2)将丁的水溶液滴入到碳酸氢钠溶液中的的离子方程式为
(3)下列说法正确的是
| A.乙、丁均属于电解质 |
| B.丙的酸性强于碳酸 |
| C.乙是一种广谱型的消毒剂,可取代甲成为自来水的消毒剂 |
| D.戊→己必须加还原剂才能实现 |
II.某实验小组向100mLFeI2溶液中通入Cl2,溶液中Fe3+、I2的物质的量随通入的Cl2的物质的量变化如图所示(不考虑与水的反应)。请回答下列问题:

(4)从开始通入Cl2到n(Cl2)=0.12mol时,溶液中:
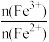 =
=(5)通入足量氯气反应的化学方程式为:
III.把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生1.16g白色沉淀,再向所得悬浊液中逐滴加入1.00mol/LHCl溶液,加入HCl溶液的体积与生成沉淀的关系如图。试回答:

(6)A点的沉淀物的化学式为
(7)C点消耗HCl溶液的体积为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】某溶液由K+、Cu2+、Ba2+、Fe3+、CO 、SO
、SO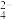 、Cl-中的若干种离子组成,取适量该溶液进行如下实验:
、Cl-中的若干种离子组成,取适量该溶液进行如下实验:
①向其中加入过量盐酸,有气体生成,并得到无色透明溶液;
②在①所得溶液中加入过量氢氧化钡溶液,产生白色沉淀,过滤;
③在②所得的滤液中加入过量稀硝酸,再加入硝酸银溶液,产生白色沉淀。
根据上述实验回答下列问题:
(1)原溶液中一定不存在的离子_______ ;
(2)原溶液中一定存在的离子是_______ ;
(3)原溶液中可能存在的离子是_______ 。
(4)请写出①中发生反应的离子方程式_______
 、SO
、SO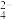 、Cl-中的若干种离子组成,取适量该溶液进行如下实验:
、Cl-中的若干种离子组成,取适量该溶液进行如下实验:①向其中加入过量盐酸,有气体生成,并得到无色透明溶液;
②在①所得溶液中加入过量氢氧化钡溶液,产生白色沉淀,过滤;
③在②所得的滤液中加入过量稀硝酸,再加入硝酸银溶液,产生白色沉淀。
根据上述实验回答下列问题:
(1)原溶液中一定不存在的离子
(2)原溶液中一定存在的离子是
(3)原溶液中可能存在的离子是
(4)请写出①中发生反应的离子方程式
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】现有五种物质A、B、C、D、E,其中有一种是碱,四种是盐。溶于水后电离可以产生下列离子:Na+、H+、Ba2+、OH-、CO32-、SO42-。为鉴别它们,分别完成以下实验,其结果如下:
① A溶液与B溶液反应可生成无色气体X,气体X可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应;
② B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请根据上述实验结果填空:
(1)写出下列物质的化学式:X__________ ,B __________ ,C __________
(2)写出A的稀溶液与X气体反应的离子方程式_____________________________________ 。
(3)向A溶液中逐滴加入B溶液至过量,写出该过程的离子方程式_________________ 。
① A溶液与B溶液反应可生成无色气体X,气体X可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应;
② B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请根据上述实验结果填空:
(1)写出下列物质的化学式:X
(2)写出A的稀溶液与X气体反应的离子方程式
(3)向A溶液中逐滴加入B溶液至过量,写出该过程的离子方程式
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某学习小组进行如下课外活动,邀请你参与:
(1)研究水溶液中复分解型离子反应的发生条件,设计如下方案:
①写出II实验中发生反应的离子方式___________ ;
②根据实验发现只要有___________ ,等物质生成,水溶液中复分解型离子反应就可以发生。
③经过小组同学积极思考、讨论交流发现在生成三类物质后,导致一个共同的结果,于是得出结论:溶液中复分解型的离子反应总是向着某些___________ 的方向进行(与溶液混合的瞬间相比)。
④小组同学进一步深入思考,发现上述问题其实质是化学反应进行的方向问题。请你结合化学反应原理的相关知识对③中的结论作出合理解释___________ ;
(2)如何研究H2SO4、KC1、NaHSO4、NaNO3、Na2CO3、NH4C1、NaOH的性质?设计方案为:将它们按照酸、碱、盐分类,然后分别溶于水得到溶液,进行实验,具体如下:
①根据方案进行分类时,经实验测得KC1、NaNO3,溶液的pH=7;
H2SO4、NaHSO4、NH4Cl溶液的pH<7;
Na2CO3、NaOH溶液的pH>7。
由此有的同学按分类法思想把H2SO4、NaHSO4、NH4Cl都划分为酸类,请你运用中学化学相关理论判断这样划分是否合理?并简要说明理由。___________ 、___________ ;
②向NaHSO4、NaNO3的混合溶液中,滴加Na2S溶液产生黄色沉淀和无色气体,写出反应的离子方程式:___________ ;反应中若生成标准状况下的无色气体1.12L,则被氧化的物质为___________ mol,转移电子的物质的量为___________ mol。
③某同学在用H2SO4鉴别NaNO3、Na2CO3、NaOH溶液时,Na2CO3很容易鉴别,但鉴别NaNO3和NaOH时却陷入了困境。限用上述另外六种物质,请你设计一个现象明显的实验方案帮忙解决这一难题___________ 。
(1)研究水溶液中复分解型离子反应的发生条件,设计如下方案:
| 实验设计及操作 | 离子方程式 |
| Ⅰ.向盛有2mlCuSO4溶液的试管里加入2mlNaOH溶液,观察现象 | Cu2++2OH-═Cu(OH)2↓ |
| Ⅱ.向盛有2mL pH=1的HCl溶液的试管里慢慢滴入18mL(已足量)CH3COONH4溶液(查资料知CH3COONH4,溶液呈中性 )振荡摇匀,测得pH≈3.7 | |
| Ⅲ向盛有2mLNaHCO3溶液的试管里加入2mL H2SO4溶液,观察现象 | HCO +H+═H2O+CO2↑ +H+═H2O+CO2↑ |
| Ⅳ向盛有2mL 稀Na2SO4溶液的试管里加入2mL稀KCl溶液,观察无明显现象 |  |
②根据实验发现只要有
③经过小组同学积极思考、讨论交流发现在生成三类物质后,导致一个共同的结果,于是得出结论:溶液中复分解型的离子反应总是向着某些
④小组同学进一步深入思考,发现上述问题其实质是化学反应进行的方向问题。请你结合化学反应原理的相关知识对③中的结论作出合理解释
(2)如何研究H2SO4、KC1、NaHSO4、NaNO3、Na2CO3、NH4C1、NaOH的性质?设计方案为:将它们按照酸、碱、盐分类,然后分别溶于水得到溶液,进行实验,具体如下:
①根据方案进行分类时,经实验测得KC1、NaNO3,溶液的pH=7;
H2SO4、NaHSO4、NH4Cl溶液的pH<7;
Na2CO3、NaOH溶液的pH>7。
由此有的同学按分类法思想把H2SO4、NaHSO4、NH4Cl都划分为酸类,请你运用中学化学相关理论判断这样划分是否合理?并简要说明理由。
②向NaHSO4、NaNO3的混合溶液中,滴加Na2S溶液产生黄色沉淀和无色气体,写出反应的离子方程式:
③某同学在用H2SO4鉴别NaNO3、Na2CO3、NaOH溶液时,Na2CO3很容易鉴别,但鉴别NaNO3和NaOH时却陷入了困境。限用上述另外六种物质,请你设计一个现象明显的实验方案帮忙解决这一难题
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】I.为探究某盐X ( 含五种元素)的组成和性质, 设计并完成如下实验:
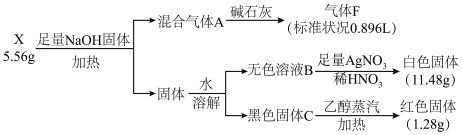
已知:气体F能使湿润的红色石蕊试纸变蓝。请回答:
(l)X含有的元素有 O、H、_____ ( 用元素符号表示), X 的化学式为_____ 。
(2)写出气体F 与黑色固体 C 在一定条件下发生的氧化还原反应, 产物中有一气体单质:______ 。
II.某学习小组设计制取 SO2并验证其部分性质的实验装置如图(夹持装置省略):

请回答:
(1)简述检查装置 A 气密性的方法:_________ 。
(2)写出C 中发生的离子反应方程式:_________ 。
(3)设计实验方案检验实验后 D 中的主要阴离子:________ .

已知:气体F能使湿润的红色石蕊试纸变蓝。请回答:
(l)X含有的元素有 O、H、
(2)写出气体F 与黑色固体 C 在一定条件下发生的氧化还原反应, 产物中有一气体单质:
II.某学习小组设计制取 SO2并验证其部分性质的实验装置如图(夹持装置省略):

请回答:
(1)简述检查装置 A 气密性的方法:
(2)写出C 中发生的离子反应方程式:
(3)设计实验方案检验实验后 D 中的主要阴离子:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】(1)某固体物质可能含有氯化钾、硫酸铜、氢氧化钠、硝酸镁,硫酸钠中的一种或几种,为鉴定它们,做如下实验:
①将该固体物质全部溶解于水中,得到无色溶液a。
②取少量a溶液于试管中,向其中滴加少量硫酸铁溶液,产生红褐色沉淀
③另取少量a溶液于试管中,向其中滴加少量的硝酸钡溶液,产生白色沉淀
步骤③中发生反应的化学方程式__________________________ 。据此推断,该固体物质中一定含有(以下写化学式,下同)______________ ,一定不含有________________ ,可能含有_____ 。
(2)下图是初中化学常见六种物质之间的关系图(物质是溶液的只考虑溶质)。图中用“—”表示两种物质之间能发生化学反应,用“→”表示一种物质可以转化为另一种物质(部分反应物或生成物及反应条件已略去)。

A是一种碱,其中阳离子是人体骨骼中的主要成分,B是胃酸的主要成分。C、D中所含元素种类相同。
①请分别写出A、B、C、D物质的化学式(或溶质的化学式):
A.___________ B.___________ C.___________ D.___________ ;
②写出Fe2O3反应生成C物质的化学方程式___________________________ (写一个);
③写出Fe2O3与足量B反应的实验现象_______________________________________ 。
①将该固体物质全部溶解于水中,得到无色溶液a。
②取少量a溶液于试管中,向其中滴加少量硫酸铁溶液,产生红褐色沉淀
③另取少量a溶液于试管中,向其中滴加少量的硝酸钡溶液,产生白色沉淀
步骤③中发生反应的化学方程式
(2)下图是初中化学常见六种物质之间的关系图(物质是溶液的只考虑溶质)。图中用“—”表示两种物质之间能发生化学反应,用“→”表示一种物质可以转化为另一种物质(部分反应物或生成物及反应条件已略去)。

A是一种碱,其中阳离子是人体骨骼中的主要成分,B是胃酸的主要成分。C、D中所含元素种类相同。
①请分别写出A、B、C、D物质的化学式(或溶质的化学式):
A.
②写出Fe2O3反应生成C物质的化学方程式
③写出Fe2O3与足量B反应的实验现象
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】氯化亚铁具有独有的脱色能力,适用于染料、染料中间体、印染、造纸行业的污水处理。某课题小组设计如下方案制备氯化亚铁并探究氯化亚铁(Fe2+)的还原性。
方案Ⅰ:甲同学设计如下装置制备氯化亚铁。
已知:实验室常用氯化钠固体与浓硫酸共热制备氯化氢;氯化亚铁能与水蒸气剧烈反应。

(1)写出A中反应的化学方程式:_______________ 。B中盛装的试剂为____________________ ,D装置中四氯化碳的作用是_____________ 。
(2)实验过程中,观察到D中现象是___________________________________________ 。
用物理方法检验氯化亚铁产品中是否混有铁粉:______________ 。
(3)上述方案有明显不足,请你提出改进上述方案的建议:______________________ 。方案Ⅱ:乙同学选择下列装置用氯化铁制备少量氯化亚铁(装置可以重复使用,氯化铁遇水剧烈水解)。查阅资料知,在加热条件下,氢气还原氯化铁生成氯化亚铁和氯化氢。
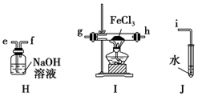
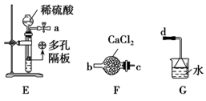
(4)气流从左至右,装置接口连接顺序是a______________________________________ 。
(5)设计简单实验证明氢气和氯化铁已发生反应:__________________________________ 。
(6)为了探究上述实验制备的氯化亚铁(Fe2+)具有还原性,设计如下方案:
a.取少量氯化亚铁样品溶于蒸馏水,滴加酸性高锰酸钾溶液,观察现象
b.取少量氯化亚铁样品溶于蒸馏水,滴加酸化的双氧水和KSCN溶液,观察现象
c.取少量氯化亚铁样品溶于蒸馏水,滴加铁氰化钾溶液,观察现象
d.取少量氯化亚铁样品溶于蒸馏水,先加KSCN溶液,后加氯水,观察现象
上述方案合理的是________ (填代号)。
方案Ⅰ:甲同学设计如下装置制备氯化亚铁。
已知:实验室常用氯化钠固体与浓硫酸共热制备氯化氢;氯化亚铁能与水蒸气剧烈反应。

(1)写出A中反应的化学方程式:
(2)实验过程中,观察到D中现象是
用物理方法检验氯化亚铁产品中是否混有铁粉:
(3)上述方案有明显不足,请你提出改进上述方案的建议:


(4)气流从左至右,装置接口连接顺序是a
(5)设计简单实验证明氢气和氯化铁已发生反应:
(6)为了探究上述实验制备的氯化亚铁(Fe2+)具有还原性,设计如下方案:
a.取少量氯化亚铁样品溶于蒸馏水,滴加酸性高锰酸钾溶液,观察现象
b.取少量氯化亚铁样品溶于蒸馏水,滴加酸化的双氧水和KSCN溶液,观察现象
c.取少量氯化亚铁样品溶于蒸馏水,滴加铁氰化钾溶液,观察现象
d.取少量氯化亚铁样品溶于蒸馏水,先加KSCN溶液,后加氯水,观察现象
上述方案合理的是
您最近半年使用:0次



