已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T 为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C、F是无色无味的气体,M为红褐色。
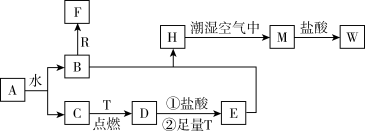
请回答下列问题:
(1)A的电子式是___________ ,R元素在元素周期表中位置为___________ ,D的俗称是___________ 。
(2)A与水反应的离子方程式为___________ 。
(3)检验W 溶液中金属阳离子的操作方法是___________ 。
(4)H转化为M的化学方程式为___________ 。
(5)B生成F反应的离子方程式为___________ 。
(6)向一定量T和D的混合物中加入200mL 1mol/L的盐酸,固体恰好完全溶解,且产生氢气448mL(标准状况下),所得溶液只有一种溶质,则混合物中两种物质的物质的量之比为___________ 。

请回答下列问题:
(1)A的电子式是
(2)A与水反应的离子方程式为
(3)检验W 溶液中金属阳离子的操作方法是
(4)H转化为M的化学方程式为
(5)B生成F反应的离子方程式为
(6)向一定量T和D的混合物中加入200mL 1mol/L的盐酸,固体恰好完全溶解,且产生氢气448mL(标准状况下),所得溶液只有一种溶质,则混合物中两种物质的物质的量之比为
更新时间:2022-04-04 19:57:49
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示 水及部分产物已略去
水及部分产物已略去 .
.
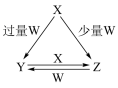
(1)若X为金属单质,W是某强酸的稀溶液,X与过量W反应生成Y的离子方程式为______ ;组成X的元素在周期表中的位置是 ______ 。
(2)若X为非金属单质,W是空气的主要成分之一,它们之间转化的能量变化如图A所示,则X+W→Z的热化学方程式为______ 。

(3)若X、Y为正盐,X的水溶液显酸性,W为一元强碱(化学式为MOH),则X与过量W反应生成Y的离子方程式为______ 。室温下,若用0.1mol/L的W溶液滴定V mL 0.1mol/L HA溶液,滴定曲线如图B所示,则a、b、c、d四点溶液中水的电离程度最大的是 ______ 点;a点溶液中离子浓度的大小顺序为 ______ .
(4)若X为强碱,常温下W为有刺激性气味的气态氧化物。常温时,将Z的水溶液露置于空气中,请在图C中画出其pH随时间(t)的变化趋势曲线图 不考虑水的挥发
不考虑水的挥发
______ 。
 水及部分产物已略去
水及部分产物已略去 .
.
(1)若X为金属单质,W是某强酸的稀溶液,X与过量W反应生成Y的离子方程式为
(2)若X为非金属单质,W是空气的主要成分之一,它们之间转化的能量变化如图A所示,则X+W→Z的热化学方程式为

(3)若X、Y为正盐,X的水溶液显酸性,W为一元强碱(化学式为MOH),则X与过量W反应生成Y的离子方程式为
(4)若X为强碱,常温下W为有刺激性气味的气态氧化物。常温时,将Z的水溶液露置于空气中,请在图C中画出其pH随时间(t)的变化趋势曲线图
 不考虑水的挥发
不考虑水的挥发
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z是中学化学常见的三种物质,它们之间的相互转化关系如下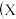 、Y、Z、E、F为英文字母,部分反应条件及产物略去
、Y、Z、E、F为英文字母,部分反应条件及产物略去
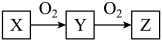
I.若Y是一种易溶于水,且能使品红溶液褪色的无色刺激性气味的气体。
(1)则Y和新制氯水主要成分反应生成两种强酸的化学方程式______________ 。
(2) Y气体的大量排放会形成酸雨,在工业上可以用足量氨水吸收,化学方程式为________________ 。
(3)Z的水溶液可以制得某种强酸E。实验室用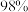 的浓
的浓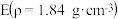 溶液配制
溶液配制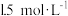 稀E溶液
稀E溶液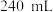 。
。
①制该稀E溶液需要使用的玻璃仪器有胶头滴管、量筒、烧杯、____ 和_____ ;
②算所需E浓溶液的体积为___ mL(保留1位小数)。
II.若Z是淡黄色固体粉末。在呼吸面具或潜水艇中由Z和CO2制备氧气的化学反应方程式为____ 。
III.若Z是红棕色气体。
(1)试写出Z与水反应制备另一种强酸F的化学方程式_______ 。
(2)2.0g铜镁合金完全溶解于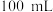 密度为
密度为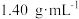 质量分数为
质量分数为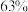 的浓F溶液中,得到Z和
的浓F溶液中,得到Z和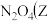 和
和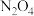 均为浓F溶液的还原产物
均为浓F溶液的还原产物 的混合气体
的混合气体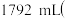 标准状况
标准状况 ,向反应后的溶液中加入
,向反应后的溶液中加入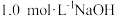 溶液,当金属离子全部沉淀,得到
溶液,当金属离子全部沉淀,得到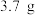 沉淀。则合金中铜与镁的物质的量之比为
沉淀。则合金中铜与镁的物质的量之比为_____ ,加入NaOH溶液的体积为_____ mL。
 、Y、Z、E、F为英文字母,部分反应条件及产物略去
、Y、Z、E、F为英文字母,部分反应条件及产物略去

I.若Y是一种易溶于水,且能使品红溶液褪色的无色刺激性气味的气体。
(1)则Y和新制氯水主要成分反应生成两种强酸的化学方程式
(2) Y气体的大量排放会形成酸雨,在工业上可以用足量氨水吸收,化学方程式为
(3)Z的水溶液可以制得某种强酸E。实验室用
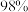 的浓
的浓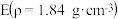 溶液配制
溶液配制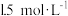 稀E溶液
稀E溶液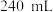 。
。①制该稀E溶液需要使用的玻璃仪器有胶头滴管、量筒、烧杯、
②算所需E浓溶液的体积为
II.若Z是淡黄色固体粉末。在呼吸面具或潜水艇中由Z和CO2制备氧气的化学反应方程式为
III.若Z是红棕色气体。
(1)试写出Z与水反应制备另一种强酸F的化学方程式
(2)2.0g铜镁合金完全溶解于
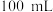 密度为
密度为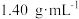 质量分数为
质量分数为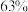 的浓F溶液中,得到Z和
的浓F溶液中,得到Z和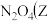 和
和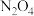 均为浓F溶液的还原产物
均为浓F溶液的还原产物 的混合气体
的混合气体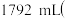 标准状况
标准状况 ,向反应后的溶液中加入
,向反应后的溶液中加入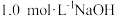 溶液,当金属离子全部沉淀,得到
溶液,当金属离子全部沉淀,得到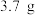 沉淀。则合金中铜与镁的物质的量之比为
沉淀。则合金中铜与镁的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】化合物A由四种常见元素组成。某同学为探究其组成进行了如图实验:
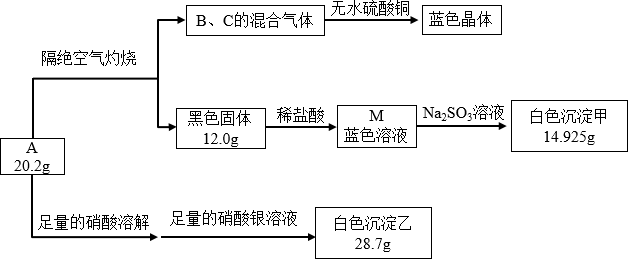
(1)已知A在隔绝空气灼烧时发生的是非氧化还原反应,黑色固体是______ (写化学式)。
(2)白色沉淀乙证明A中含______ 元素。(写元素符号)
(3)白色沉淀甲是一种氯化物,M溶液与Na2SO3溶液属于氧化还原反应,那么白色沉淀______ (写名称)。写出该反应的离子方程式______ ,得到白色沉淀的方法是______ 。检验硫酸根离子的操作______ 。
(4)A的化学式为______ 。

(1)已知A在隔绝空气灼烧时发生的是非氧化还原反应,黑色固体是
(2)白色沉淀乙证明A中含
(3)白色沉淀甲是一种氯化物,M溶液与Na2SO3溶液属于氧化还原反应,那么白色沉淀
(4)A的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,W溶液中加入KSCN出现血红色。
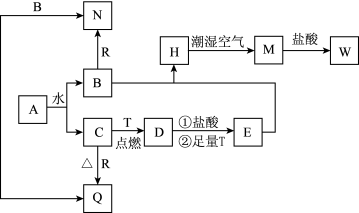
(1)写出下列物质的化学式:D_____ ,N_____ 。
(2)B与E混和得到H并在潮湿空气中变成M的过程中,可能观察到的现象:_____ ;H在潮湿空气中变成M的过程中发生的化学方程式为:______ 。
(3)按要求写方程式:B和R反应生成N的离子方程式:______ 。D→E的离子方程式:_____ 。

(1)写出下列物质的化学式:D
(2)B与E混和得到H并在潮湿空气中变成M的过程中,可能观察到的现象:
(3)按要求写方程式:B和R反应生成N的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】物质的转化关系如下图所示(有的反应可能在水溶液中进行)。其中A为气体化合物,甲可由两种单质直接化合得到,乙为金属单质,G为酸,乙在G的浓溶液中发生钝化。若甲为淡黄色固体,D和A的溶液均呈碱性,用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近,有大量白烟生成。

则(1)A的分子式是______________ ,甲的电子式是______________ 。
(2)D的溶液与乙反应的离子方程式是______________ 。

则(1)A的分子式是
(2)D的溶液与乙反应的离子方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】铝和铝合金是一类重要的金属材料。回答下列问题:
(1)除去镁粉中混有少量铝粉,应加入的试剂为_______ ,发生反应的离子方程式为_______ ,然后经过滤、洗涤、干燥。
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得H2在同温同压下的体积之比是_______ 。
(3)某同学在实验室用铝土矿(含有Al2O3和SiO2,不考虑其他杂质)制取金属铝的流程如下:
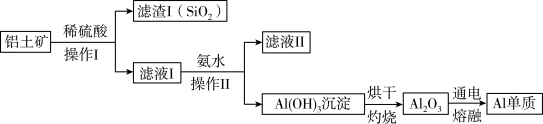
①Al2O3与稀硫酸反应的离子方程式为_______ 。
②滤液II中溶质的用途之一是_______ 。
③电解熔融的Al2O3除得到金属铝之外,还可得到的气体产物是_______ (填化学式)。工业上在电解熔融的Al2O3时,还加入了冰晶石(Na3AlF6)作熔剂,其作用是降低Al2O3的熔点。冰晶石在物质的分类中属于_______ (填字母)。
a.酸 b.碱 c.盐 d.氧化物
(1)除去镁粉中混有少量铝粉,应加入的试剂为
(2)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得H2在同温同压下的体积之比是
(3)某同学在实验室用铝土矿(含有Al2O3和SiO2,不考虑其他杂质)制取金属铝的流程如下:

①Al2O3与稀硫酸反应的离子方程式为
②滤液II中溶质的用途之一是
③电解熔融的Al2O3除得到金属铝之外,还可得到的气体产物是
a.酸 b.碱 c.盐 d.氧化物
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】元素化合物在日常生活、化工生产和环境科学中有着重要的用途。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的黑色固体Y,将Y溶于过量盐酸中,溶液中存在的阳离子有______________
(2)将题(1)中反应后生成的溶液分为a,b,c三份,a中加入适量的KNO3溶液,发生的离子反应为_________________ ,b中加入过量Na2O2,观察到的现象是_____________________ ,c中通入足量SO2,发生的离子反应为_____________
(3)取少量固体Y与金属铝在高温下反应方程式为_____________ ,若要提纯产物中的金属单质,应先加入足量的_________ 溶液再过滤,此时发生的反应方程式为________________
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的黑色固体Y,将Y溶于过量盐酸中,溶液中存在的阳离子有
(2)将题(1)中反应后生成的溶液分为a,b,c三份,a中加入适量的KNO3溶液,发生的离子反应为
(3)取少量固体Y与金属铝在高温下反应方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知A、D是两种金属单质,A燃烧时火焰呈黄色,A、B、C均含有同种元素,其中D是生活中应用最广泛的金属。请回答下列问题
A B
B C ; D
C ; D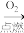 E
E  F
F
(1)根据上述反应推断B、E的化学式:B___________ ,E___________ 。
(2)金属单质A露置在空气中,最终形成___________ (填化学式)。
(3)写出B生成C的化学反应方程式:___________ 。
(4)请写出E与稀硫酸反应得到F溶液的离子方程式___________ 。
(5)请设计实验验证溶液F中所含的高价态金属阳离子:___________ 。
A
 B
B C ; D
C ; D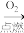 E
E  F
F(1)根据上述反应推断B、E的化学式:B
(2)金属单质A露置在空气中,最终形成
(3)写出B生成C的化学反应方程式:
(4)请写出E与稀硫酸反应得到F溶液的离子方程式
(5)请设计实验验证溶液F中所含的高价态金属阳离子:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】硫铁矿烧渣是一种重要的化学化工产业中间产物,主要成分是 、
、 、
、 和二氧化硅(二氧化硅难溶于水和酸)等。以硫铁矿烧渣制备高效净水剂聚合硫酸铁
和二氧化硅(二氧化硅难溶于水和酸)等。以硫铁矿烧渣制备高效净水剂聚合硫酸铁 (聚合硫酸铁中铁为+3价),流程图如下:
(聚合硫酸铁中铁为+3价),流程图如下:
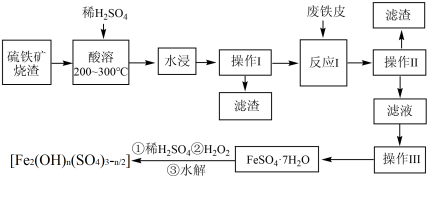
(1)实验室实现“操作Ⅰ”所用的玻璃仪器有________ 、玻璃棒和烧杯等。
(2)“酸溶”过程中 溶解的离子方程式:
溶解的离子方程式:________________________________________ 。
(3)硫铁矿烧渣在“酸溶”前要粉碎的主要目的是________________________________________ 。
(4)实验室检验“反应Ⅰ”已经完全的试剂是________ ,现象是________________________________ 。
(5)加入适量 的目的是
的目的是________ ,写出 发生反应的离子方程式:
发生反应的离子方程式:________________ 。
 、
、 、
、 和二氧化硅(二氧化硅难溶于水和酸)等。以硫铁矿烧渣制备高效净水剂聚合硫酸铁
和二氧化硅(二氧化硅难溶于水和酸)等。以硫铁矿烧渣制备高效净水剂聚合硫酸铁 (聚合硫酸铁中铁为+3价),流程图如下:
(聚合硫酸铁中铁为+3价),流程图如下:
(1)实验室实现“操作Ⅰ”所用的玻璃仪器有
(2)“酸溶”过程中
 溶解的离子方程式:
溶解的离子方程式:(3)硫铁矿烧渣在“酸溶”前要粉碎的主要目的是
(4)实验室检验“反应Ⅰ”已经完全的试剂是
(5)加入适量
 的目的是
的目的是 发生反应的离子方程式:
发生反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】有X、Y、Z、T、U五种短周期元素。X、Y、Z 三元素在周期表中的位置如图所示,三元素的原子序数之和是 41。X 和 T 的单质在不同条件下反应,可以生成T2X(白色固体)和T2X2(淡黄色固体)两种化合物。U 单质在 Z 单质中燃烧时产生苍白色火焰,生成物的水溶液能使石蕊试液变红。
(1)各元素的符号是 X______ ,Y______ ,Z______ 。
(2)Y 原子的结构示意图为_______ 。
(3)用电子式表示 Y 与 T 组成的化合物的形成过程:______ 。
(4)YX2 和 U2Y 反应的化学方程式为______ , 其中氧化剂是______ ,被氧化的元素是______ 。
| X | |
| Y | Z |
(1)各元素的符号是 X
(2)Y 原子的结构示意图为
(3)用电子式表示 Y 与 T 组成的化合物的形成过程:
(4)YX2 和 U2Y 反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】请回答下列问题。
(1)前20号X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子。若XY2为常见元素形成的离子化合物,则其电子式为_______ ;若XY2为共价化合物,则其结构式为_______ 。
(2)氯化铝的物理性质非常特殊,如氯化铝的熔点为190℃,但在180℃就开始升华。据此判断,氯化铝是_______ (填“共价化合物”或“离子化合物”),可以证明该判断正确的实验依据是_______ 。
(3)现有a~g七种短周期元素,它们在元素周期表中的位置如图所示,请据此回答下列问题:
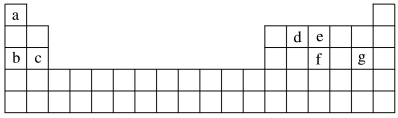
①.元素的原子间最容易形成离子键的是_______ (填字母,下同),容易形成共价键的是_______ 。
Ac和f B.b和g C.d和g D.b和e
②写出a~g七种元素形成的所有原子都满足最外层为8电子结构的任意一种分子的分子式:_______ 。
(1)前20号X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子。若XY2为常见元素形成的离子化合物,则其电子式为
(2)氯化铝的物理性质非常特殊,如氯化铝的熔点为190℃,但在180℃就开始升华。据此判断,氯化铝是
(3)现有a~g七种短周期元素,它们在元素周期表中的位置如图所示,请据此回答下列问题:

①.元素的原子间最容易形成离子键的是
Ac和f B.b和g C.d和g D.b和e
②写出a~g七种元素形成的所有原子都满足最外层为8电子结构的任意一种分子的分子式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】部分短周期元素原子半径与原子序数的关系如图所示。
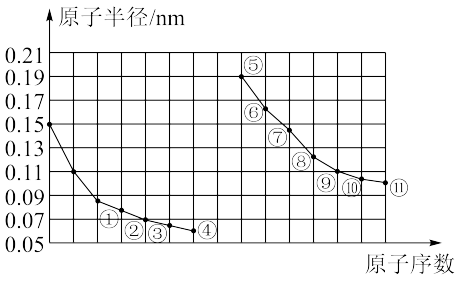
(1)元素①在周期表中的位置为_______ ;
(2)元素⑤、⑦的最高价氧化物对应的水化物中,碱性较强的是_______ (填化学式,下同);
(3)⑦、⑩、⑪三种元素常见离子的半径最大的是_______ ;
(4)元素③、⑩ 形成的简单氢化物中,熔沸点更高的是_______ ,原因是_______ ;
(5)元素③、④形成的简单氢化物中,稳定性较强的是_______ , 原因是_______ ;
(6)写出由H和③元素组成的含有极性键和非极性键的一种常见化合物的结构式:_______ ;
(7)用电子式表示⑤和⑩按2:1的原子个数比形成化合物的过程:_______ 。
(8)请设计实验比较C、N的非金属性强弱,选择的试剂有:稀硝酸、饱和NaHCO3溶液、澄清石灰水,化学仪器根据需要选择。

(1)元素①在周期表中的位置为
(2)元素⑤、⑦的最高价氧化物对应的水化物中,碱性较强的是
(3)⑦、⑩、⑪三种元素常见离子的半径最大的是
(4)元素③、⑩ 形成的简单氢化物中,熔沸点更高的是
(5)元素③、④形成的简单氢化物中,稳定性较强的是
(6)写出由H和③元素组成的含有极性键和非极性键的一种常见化合物的结构式:
(7)用电子式表示⑤和⑩按2:1的原子个数比形成化合物的过程:
(8)请设计实验比较C、N的非金属性强弱,选择的试剂有:稀硝酸、饱和NaHCO3溶液、澄清石灰水,化学仪器根据需要选择。
| 实验操作 | 实验现象 | 实验结论 |
您最近一年使用:0次



