生物浸出是指用细菌(微生物)从固体中浸出金属离子,有速率快、浸出率高等特点。
已知:①氧化亚铁硫杆菌是一类在酸性环境中加速 氧化的细菌,培养后能提供
氧化的细菌,培养后能提供 。
。
②控制适宜的温度和溶液酸碱度,可使氧化亚铁硫杆菌达到最大活性。
③氧化亚铁硫杆菌的生物浸矿机理如下图:

Ⅰ.用氧化亚铁硫杆菌生物浸出ZnS矿。
(1)反应1的离子方程式是_______ 。
(2)反应2中有S单质生成,离子方程式是_______ 。
(3)实验表明,温度较高或酸性过强时金属离子的浸出率均偏低,原因可能是_______ 。
Ⅱ.氧化亚铁硫杆菌生物浸出废旧锂离子电池中钻酸锂( )与上述浸出机理相似,发生的反应是:
)与上述浸出机理相似,发生的反应是:
ⅰ.上图中的反应1
ⅱ.反应3: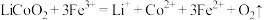
(4)已知 中Li为
中Li为 价,则Co(钴)元素的化合价是
价,则Co(钴)元素的化合价是_______ 。
(5)在酸性环境中, 浸出
浸出 的总反应的离子方程式是
的总反应的离子方程式是_______ 。
(6)研究表明氧化亚铁硫杆菌存在时, 对钴浸出率有影响,实验研究
对钴浸出率有影响,实验研究 的作用。取
的作用。取 粉末和氧化亚铁硫杆菌溶液于锥形瓶中,分别加入不同浓度
粉末和氧化亚铁硫杆菌溶液于锥形瓶中,分别加入不同浓度 时的溶液,钴浸出率随时间变化曲线如图:
时的溶液,钴浸出率随时间变化曲线如图:
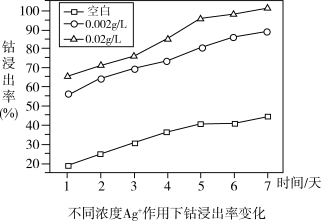
①由图和其他实验可知, 能催化浸出
能催化浸出 ,图1中的证据是
,图1中的证据是_______ 。
② 是反应3(
是反应3(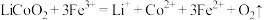 )的催化剂,催化过程可表示为:
)的催化剂,催化过程可表示为:
反应4: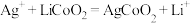 ;
;
反应5:……
反应5的离子方程式是_______ 。
已知:①氧化亚铁硫杆菌是一类在酸性环境中加速
 氧化的细菌,培养后能提供
氧化的细菌,培养后能提供 。
。②控制适宜的温度和溶液酸碱度,可使氧化亚铁硫杆菌达到最大活性。
③氧化亚铁硫杆菌的生物浸矿机理如下图:

Ⅰ.用氧化亚铁硫杆菌生物浸出ZnS矿。
(1)反应1的离子方程式是
(2)反应2中有S单质生成,离子方程式是
(3)实验表明,温度较高或酸性过强时金属离子的浸出率均偏低,原因可能是
Ⅱ.氧化亚铁硫杆菌生物浸出废旧锂离子电池中钻酸锂(
 )与上述浸出机理相似,发生的反应是:
)与上述浸出机理相似,发生的反应是:ⅰ.上图中的反应1
ⅱ.反应3:
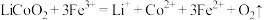
(4)已知
 中Li为
中Li为 价,则Co(钴)元素的化合价是
价,则Co(钴)元素的化合价是(5)在酸性环境中,
 浸出
浸出 的总反应的离子方程式是
的总反应的离子方程式是(6)研究表明氧化亚铁硫杆菌存在时,
 对钴浸出率有影响,实验研究
对钴浸出率有影响,实验研究 的作用。取
的作用。取 粉末和氧化亚铁硫杆菌溶液于锥形瓶中,分别加入不同浓度
粉末和氧化亚铁硫杆菌溶液于锥形瓶中,分别加入不同浓度 时的溶液,钴浸出率随时间变化曲线如图:
时的溶液,钴浸出率随时间变化曲线如图:
①由图和其他实验可知,
 能催化浸出
能催化浸出 ,图1中的证据是
,图1中的证据是②
 是反应3(
是反应3(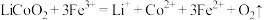 )的催化剂,催化过程可表示为:
)的催化剂,催化过程可表示为:反应4:
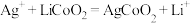 ;
;反应5:……
反应5的离子方程式是
更新时间:2022-04-04 08:57:08
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
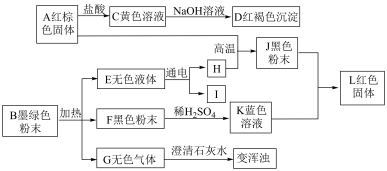
【推荐1】已知物质A~K之间有如下图所示转化关系。其中A是一种易溶于水的离子化合物,在空气中易潮解和变质,在水中可以电离出电子总数相等的两种离子;E为生活中常用消毒剂的有效成分,F是生活中不可缺少的调味剂,G为无色液体,B、C、D、K都是单质;反应②~⑤都是重要的工业反应。(部分反应需要在溶液中进行)
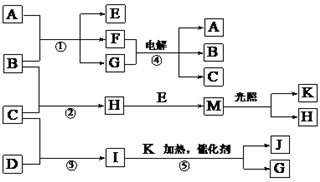
(1)物质D中所含元素在周期表中的位置为____________________________ ,
E中所含化学键类型有___________________________________________ ,
M的结构式为___________________________________________________ 。
(2)反应④的离子方程式为___________________________________________ 。
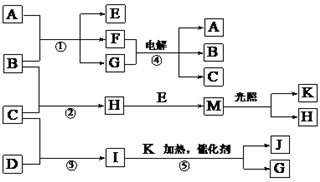
(1)物质D中所含元素在周期表中的位置为
E中所含化学键类型有
M的结构式为
(2)反应④的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】元素周期表的形式多种多样,下图是扇形元素周期表的一部分,对照中学化学常见的长式元素周期表(即鲁科版化学书附录中的元素周期表),回答下列问题:
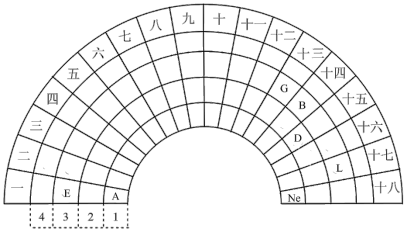
(1)元素B在长式元素周期表中的位置是_______ ,L元素的原子结构示意图为_______ 。
(2)保存E的最高价氧化物对应的水化物的溶液时,不能用磨口玻璃塞,请用化学方程式表示原因_______ 。
(3)G的最高价氧化物对应的水化物与L的最高价水化物对应的水化物反应的离子方程式为_______ 。
(4)写出A、D、L三种元素形成的常见的盐的电子式_______ 。

(1)元素B在长式元素周期表中的位置是
(2)保存E的最高价氧化物对应的水化物的溶液时,不能用磨口玻璃塞,请用化学方程式表示原因
(3)G的最高价氧化物对应的水化物与L的最高价水化物对应的水化物反应的离子方程式为
(4)写出A、D、L三种元素形成的常见的盐的电子式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】水泥是重要的建筑材料。水泥熟料的主要成分为CaO、 ,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:
,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:
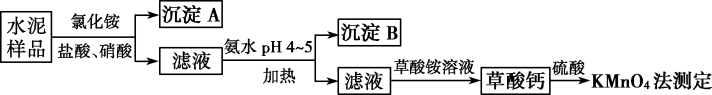
回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是_______ ,还可使用_______ 代替硝酸。
(2)沉淀A的主要成分是_______ ,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为_______ 。
(3)加氨水过程中加热的目的是_______ 。沉淀B的主要成分为 、
、_______ (填化学式)
(4)草酸钙沉淀经稀 处理后,用
处理后,用 标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为:
标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为: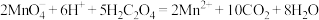 。实验中称取0.400g水泥样品,滴定时消耗了
。实验中称取0.400g水泥样品,滴定时消耗了 的
的 溶液36.00mL,则该水泥样品中钙的质量分数为
溶液36.00mL,则该水泥样品中钙的质量分数为_______ ,(相对原子质量Ca:40)
 ,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:
,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:
回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是
(2)沉淀A的主要成分是
(3)加氨水过程中加热的目的是
 、
、(4)草酸钙沉淀经稀
 处理后,用
处理后,用 标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为:
标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为: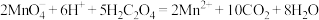 。实验中称取0.400g水泥样品,滴定时消耗了
。实验中称取0.400g水泥样品,滴定时消耗了 的
的 溶液36.00mL,则该水泥样品中钙的质量分数为
溶液36.00mL,则该水泥样品中钙的质量分数为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】(1)Ⅰ.太阳能、风能发电逐渐得到广泛应用,在发电系统中安装储能装置有助于持续稳定供电,其构造的简化图如下
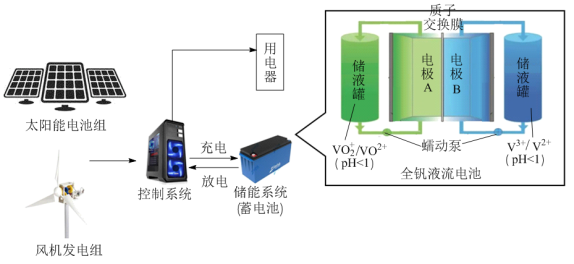
下列说法中,不正确的是________ (填字母序号)
a.太阳能、风能都是清洁能源
b.太阳能电池组实现了太阳能到电能的转化
c.控制系统能够控制储能系统是充电还是放电
d.阳光或风力充足时,储能系统实现由化学能到电能的转化
(2)全钒液流电池是具有发展前景的、用作储能系统的蓄电池。已知放电时V2+发生氧化反应,则放电时电极A的电极反应式为________ 。
(3)含钒废水会造成水体污染,对含钒废水(除VO2+外,还含有Al3+, Fe3+)等进行综合处理可实现钒资源的回收利用,流程如下:

已知溶液pH范围不同时,钒的存在形式如下表所示
①加入NaOH调节溶液pH至13时,沉淀1达最大量,并由灰白色转变为红褐色,用化学用语表示加入NaOH后涉及到氧化物还原反应的化学反应方程式为________ 。
②向碱性的滤液1(V的化合价为+4)中加入H2O2的作用是________ 。
(4)Ⅱ.氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:

Ⅰ中加入NaOH溶液,调pH=11并鼓入大量空气,用离子方程式表示加NaOH溶液的作用是________ ;鼓入大量空气的目的是________ 。
(5)Ⅱ中加入适量NaClO溶液,控制pH在6~7,将氨氮转化为无毒物质,过程Ⅱ发生3个反应:
ⅰ.ClO-+H+=HClO
ⅱ.NH4++HClO=NH2Cl+H++H2O(NH2Cl中Cl元素为+1价)
ⅲ. ……
已知:水体中以+1价形式存在的氯元素有消毒杀菌的作用,被称为“余氯”。下图为NaClO加入量与“余氯”含量的关系示意图。其中氨氮含量最低的点是c点。
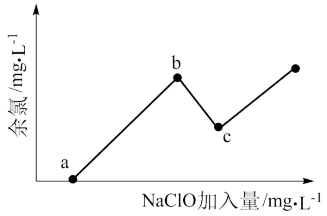
b点表示的溶液中氮元素的主要存在形式是(用化学式表示)________ ;反应ⅲ的化学方程式是________ 。
(6)Ⅲ中用Na2SO3溶液处理含余氯废水,要求达标废水中剩余Na2SO3的含量小于5mg·L-1。若含余氯废水中NaClO的含量是7.45mg·L-1,则处理10m3含余氯废水,至多添加10%Na2SO3溶液________ kg(溶液体积变化忽略不计)。

下列说法中,不正确的是
a.太阳能、风能都是清洁能源
b.太阳能电池组实现了太阳能到电能的转化
c.控制系统能够控制储能系统是充电还是放电
d.阳光或风力充足时,储能系统实现由化学能到电能的转化
(2)全钒液流电池是具有发展前景的、用作储能系统的蓄电池。已知放电时V2+发生氧化反应,则放电时电极A的电极反应式为
(3)含钒废水会造成水体污染,对含钒废水(除VO2+外,还含有Al3+, Fe3+)等进行综合处理可实现钒资源的回收利用,流程如下:

已知溶液pH范围不同时,钒的存在形式如下表所示
| 钒的化合价 | pH<2 | pH>11 |
| +4价 | VO2+, VO(OH)+ | VO(OH)3- |
| +5价 | VO2+ | VO43- |
①加入NaOH调节溶液pH至13时,沉淀1达最大量,并由灰白色转变为红褐色,用化学用语表示加入NaOH后涉及到氧化物还原反应的化学反应方程式为
②向碱性的滤液1(V的化合价为+4)中加入H2O2的作用是
(4)Ⅱ.氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:

Ⅰ中加入NaOH溶液,调pH=11并鼓入大量空气,用离子方程式表示加NaOH溶液的作用是
(5)Ⅱ中加入适量NaClO溶液,控制pH在6~7,将氨氮转化为无毒物质,过程Ⅱ发生3个反应:
ⅰ.ClO-+H+=HClO
ⅱ.NH4++HClO=NH2Cl+H++H2O(NH2Cl中Cl元素为+1价)
ⅲ. ……
已知:水体中以+1价形式存在的氯元素有消毒杀菌的作用,被称为“余氯”。下图为NaClO加入量与“余氯”含量的关系示意图。其中氨氮含量最低的点是c点。

b点表示的溶液中氮元素的主要存在形式是(用化学式表示)
(6)Ⅲ中用Na2SO3溶液处理含余氯废水,要求达标废水中剩余Na2SO3的含量小于5mg·L-1。若含余氯废水中NaClO的含量是7.45mg·L-1,则处理10m3含余氯废水,至多添加10%Na2SO3溶液
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】一个完整的氧化还原反应方程式可以拆开,写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”。如2Fe3++Cu=2Fe2++Cu2+,可拆写为氧化反应式:Cu-2e- =Cu2+,还原反应式:2Fe3++2e- =2Fe2+。据此,回答下列问题:
(1)将反应3NO2+H2O=2H++2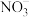 +NO拆写为两个“半反应式”:
+NO拆写为两个“半反应式”:
氧化反应式:_______ 。还原反应式:_______ 。
(2)某化学反应的反应物和产物如下:Al+NaNO3+H2O Al(OH)3+N2+NaAlO2
Al(OH)3+N2+NaAlO2
①该反应的氧化剂是_______ 。
②该反应的氧化产物是_______ 。
③配平该反应的化学方程式_______ 。
④反应过程中转移300个e-,生成_______ 个N2。
(1)将反应3NO2+H2O=2H++2
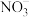 +NO拆写为两个“半反应式”:
+NO拆写为两个“半反应式”:氧化反应式:
(2)某化学反应的反应物和产物如下:Al+NaNO3+H2O
 Al(OH)3+N2+NaAlO2
Al(OH)3+N2+NaAlO2①该反应的氧化剂是
②该反应的氧化产物是
③配平该反应的化学方程式
Al+ NaNO3+ H2O Al(OH)3+ N2+ NaAlO2
Al(OH)3+ N2+ NaAlO2
④反应过程中转移300个e-,生成
您最近一年使用:0次
【推荐1】甲醇是重要的化工基础原料和清洁液体燃料,在CO2加氢合成CH3OH的体系中,同时发生下列竞争反应:
(ⅰ)CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-49.3 kJ/mol
CH3OH(g)+H2O(g) △H1=-49.3 kJ/mol
(ⅱ)CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41.1 kJ/mol
CO(g)+H2O(g) △H2=+41.1 kJ/mol
由CO也能直接加氢合成甲醇:(iii) 2H2(g)+CO(g) CH3OH(g) △H
CH3OH(g) △H
(1)△H =_______ kJ/mol。
(2)反应(ⅱ) CO2(g)+H2(g) CO(g)+H2O(g)的正、逆反应平衡常数随温度变化曲线如图所示。
CO(g)+H2O(g)的正、逆反应平衡常数随温度变化曲线如图所示。
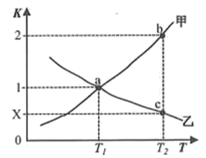
下列分析正确的是_______ 。
A.曲线甲为K(逆),曲线乙为K(正)
B.a点时,一定有v正=v逆
C.c点时,x=0.5
(3)催化剂M、N对CO2(g)+3H2(g) CH3OH(g)+H2O(g)反应进程的能量影响如下图(a)所示,两种催化剂对应的1nk~
CH3OH(g)+H2O(g)反应进程的能量影响如下图(a)所示,两种催化剂对应的1nk~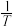 关系如下图(b)所示(已知;lnk=-
关系如下图(b)所示(已知;lnk=-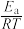 +C,其中Ea为活化能,k为速率常数,R和C为常数)。
+C,其中Ea为活化能,k为速率常数,R和C为常数)。
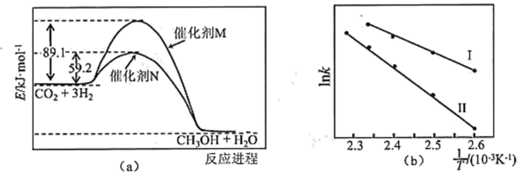
①使用催化剂M时,逆反应的活化能为_______ kJ/mol。
②催化剂N对应曲线是图(b)中的_______ (填“Ⅰ”或“Ⅱ”)
(4)为进一步研究CO2与H2反应制CH3OH的过程中原料气组成对反应速率的影响,分别向三个压强恒定为P的密闭容器(装有等量催化剂,且在实验温度范围内催化剂活性变化不大)中通入相同碳氢比的三种混合气,相同时间内,测得甲醇生成速率与温度的关系如图所示。
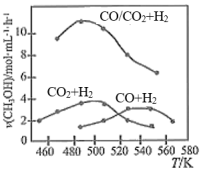
①三个容器中,甲醇的生成速率达峰值后均随温度升高而下降的原因是_______ 。
②结合研究目的,参照图中三条曲线,你可得出的结论是_______ (写一条)。
(5)恒温下,在压强恒定为P的装置中,按n(CO2):n(H2)=1:3加入反应物,发生反应(ⅰ)、(ⅱ)。达到平衡时,若CO2转化率为20%,甲醇的选择性为50%。列出反应(ⅰ)CO2(g)+3H2(g) CH3OH(g)+H2O(g)的平衡常数计算式:Kp=
CH3OH(g)+H2O(g)的平衡常数计算式:Kp=_______ (不必化简)。(已知: 的选择性x=
的选择性x=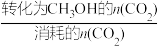 ×100%;Kp为用分压代替浓度的平衡常数。)
×100%;Kp为用分压代替浓度的平衡常数。)
(ⅰ)CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1=-49.3 kJ/mol
CH3OH(g)+H2O(g) △H1=-49.3 kJ/mol(ⅱ)CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41.1 kJ/mol
CO(g)+H2O(g) △H2=+41.1 kJ/mol由CO也能直接加氢合成甲醇:(iii) 2H2(g)+CO(g)
 CH3OH(g) △H
CH3OH(g) △H(1)△H =
(2)反应(ⅱ) CO2(g)+H2(g)
 CO(g)+H2O(g)的正、逆反应平衡常数随温度变化曲线如图所示。
CO(g)+H2O(g)的正、逆反应平衡常数随温度变化曲线如图所示。
下列分析正确的是
A.曲线甲为K(逆),曲线乙为K(正)
B.a点时,一定有v正=v逆
C.c点时,x=0.5
(3)催化剂M、N对CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)反应进程的能量影响如下图(a)所示,两种催化剂对应的1nk~
CH3OH(g)+H2O(g)反应进程的能量影响如下图(a)所示,两种催化剂对应的1nk~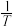 关系如下图(b)所示(已知;lnk=-
关系如下图(b)所示(已知;lnk=-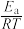 +C,其中Ea为活化能,k为速率常数,R和C为常数)。
+C,其中Ea为活化能,k为速率常数,R和C为常数)。
①使用催化剂M时,逆反应的活化能为
②催化剂N对应曲线是图(b)中的
(4)为进一步研究CO2与H2反应制CH3OH的过程中原料气组成对反应速率的影响,分别向三个压强恒定为P的密闭容器(装有等量催化剂,且在实验温度范围内催化剂活性变化不大)中通入相同碳氢比的三种混合气,相同时间内,测得甲醇生成速率与温度的关系如图所示。

①三个容器中,甲醇的生成速率达峰值后均随温度升高而下降的原因是
②结合研究目的,参照图中三条曲线,你可得出的结论是
(5)恒温下,在压强恒定为P的装置中,按n(CO2):n(H2)=1:3加入反应物,发生反应(ⅰ)、(ⅱ)。达到平衡时,若CO2转化率为20%,甲醇的选择性为50%。列出反应(ⅰ)CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)的平衡常数计算式:Kp=
CH3OH(g)+H2O(g)的平衡常数计算式:Kp= 的选择性x=
的选择性x=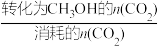 ×100%;Kp为用分压代替浓度的平衡常数。)
×100%;Kp为用分压代替浓度的平衡常数。)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】甲酸(HCOOH)常用于橡胶、医药等工业。铋基催化剂对CO2电化学还原制取HCOOH具有高效的选择性。其反应历程与能量变化如图所示。

(1)制取HCOOH催化效果较好的催化剂为___________ 。
(2)不同催化剂下,该历程的最大能垒(活化能)为___________ eV;由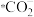 生成
生成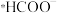 的反应为
的反应为___________ 。
(3)HCOOH燃料电池的工作原理如图所示。

①该离子交换膜为___________ (填“阳”或“阴”)离子交换膜。
②电池负极反应式为___________ 。
③当电路中转移0.2 mol电子时,理论上消耗标准状况下O2的体积为___________ L,需补充物质X的化学式为___________ 。

(1)制取HCOOH催化效果较好的催化剂为
(2)不同催化剂下,该历程的最大能垒(活化能)为
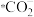 生成
生成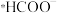 的反应为
的反应为(3)HCOOH燃料电池的工作原理如图所示。

①该离子交换膜为
②电池负极反应式为
③当电路中转移0.2 mol电子时,理论上消耗标准状况下O2的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol /L的溶液。在FeCl2溶 液中需加入少量铁屑,其目的是___________ 。
(2)甲组同学取2 mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为____________ 。
(3)乙组同学认为甲组的实验不够谨慎,该组同学在2 mL FeCl2溶液中先加入0.5 mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是__________ 。
(4)丙组同学取10 mL0.1mol/LKI溶液,加入6mL0.1 mol/LFeCl3溶液混合。 分别取2 mL此溶液于3支武管中进行如下实验:
①第一支试管中加入1 mL CCl4充分振荡、静置,CCl4层显紫色;
②第二支试管中加入1滴K3[Fe(CN)6]溶液,生成蓝色沉淀;
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是_______ (填离子符号);实验①和实验③说明:在I-过量的情况下, 溶液中仍含有_____ (填离子符号);由此可以证明该氧化还原反应为___________ 。
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为________ 。一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成,产生气泡的原因是__________ 。 生成沉淀的原因是______________ (用平衡移动原理解释)。
(6)某铁的氧化物(FexO) 1.52 g溶于足量盐酸中,向所得溶液通入标准状况下112 mL Cl2,恰好将Fe2+完全氧化,则x值为________ 。
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol /L的溶液。在FeCl2溶 液中需加入少量铁屑,其目的是
(2)甲组同学取2 mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为
(3)乙组同学认为甲组的实验不够谨慎,该组同学在2 mL FeCl2溶液中先加入0.5 mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是
(4)丙组同学取10 mL0.1mol/LKI溶液,加入6mL0.1 mol/LFeCl3溶液混合。 分别取2 mL此溶液于3支武管中进行如下实验:
①第一支试管中加入1 mL CCl4充分振荡、静置,CCl4层显紫色;
②第二支试管中加入1滴K3[Fe(CN)6]溶液,生成蓝色沉淀;
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为
(6)某铁的氧化物(FexO) 1.52 g溶于足量盐酸中,向所得溶液通入标准状况下112 mL Cl2,恰好将Fe2+完全氧化,则x值为
您最近一年使用:0次