非金属元素虽然种类不多,但是在自然界中的丰度却很大,请回答下列问题:
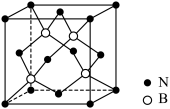
(1)BN(氮化硼,晶胞结构如图)和CO2中的化学键均为共价键,BN的熔点高且硬度大,CO2的晶体干冰却松软且极易升华。由此可以判断: BN可能是_______ 晶体,CO2可能是_______ 晶体,BN晶体中B原子的杂化轨道类型为_______ ,干冰中C原子的杂化轨道类型为_______ 。
(2)磷及其化合物在电池、催化等领域有重要应用。黑磷与石墨类似,也具有层状结构(如图甲)。为大幅度提高锂电池的充电速率,科学家最近研发了黑磷—石墨复合负极材料,其单层结构俯视图如图乙所示。

回答下列问题:
①根据图甲和图乙的信息,下列说法正确的有_______ (填序号)。
A.黑磷区中P-P键的键能不完全相同。
B.黑磷与石墨都属于混合型晶体
C.由石墨与黑磷制备该复合材料的过程,发生了物理反应
D.复合材料单层中,P原子与C原子之间的作用力属范德华力
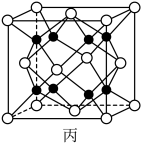
②贵金属磷化物Rh2P(化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图丙所示。已知晶胞参数为anm,晶体中与P距离最近的Rh的数目为_______ ,晶体的密度为_______ g·cm-3(列出计算式)。
(1)BN(氮化硼,晶胞结构如图)和CO2中的化学键均为共价键,BN的熔点高且硬度大,CO2的晶体干冰却松软且极易升华。由此可以判断: BN可能是

(2)磷及其化合物在电池、催化等领域有重要应用。黑磷与石墨类似,也具有层状结构(如图甲)。为大幅度提高锂电池的充电速率,科学家最近研发了黑磷—石墨复合负极材料,其单层结构俯视图如图乙所示。

回答下列问题:
①根据图甲和图乙的信息,下列说法正确的有
A.黑磷区中P-P键的键能不完全相同。
B.黑磷与石墨都属于混合型晶体
C.由石墨与黑磷制备该复合材料的过程,发生了物理反应
D.复合材料单层中,P原子与C原子之间的作用力属范德华力
②贵金属磷化物Rh2P(化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图丙所示。已知晶胞参数为anm,晶体中与P距离最近的Rh的数目为

更新时间:2022-04-14 20:03:24
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】氮化铜是一种在常温下处于亚稳态的半导体材料,由于氮化铜的可多种离子掺杂特性,有可能成为一种性能优异的锂电池负极材料。
(1)写出基态铜原子的外围电子排布式_______ 。
(2)氮元素及其同主族的非金属元素形成的最简单氢化物中,沸点最高的是_______ (填化学式),简述理由_______ 。
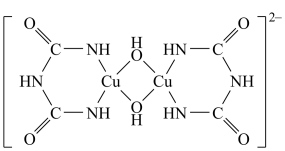
(3)在碱性溶液中缩二脲能与 反应得到特征的紫色配合物,其中的阴离子结构如图所示。该配离子中,配位原子是
反应得到特征的紫色配合物,其中的阴离子结构如图所示。该配离子中,配位原子是_______ 和_______ (填元素符号),它们的第一电离能较大的是_______ 。
(4)氮化铜的晶胞为立方晶胞,其晶胞结构如图所示。
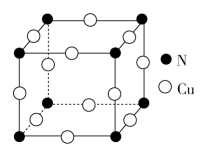
①根据晶胞结构,可判断氮化铜的化学式为_______ 。
②已知晶胞边长 ,则最近的两个Cu原子间的距离为
,则最近的两个Cu原子间的距离为_______ pm,列式并计算氮化铜晶体的密度
_______  。(保留小数点后两位)
。(保留小数点后两位)
(1)写出基态铜原子的外围电子排布式
(2)氮元素及其同主族的非金属元素形成的最简单氢化物中,沸点最高的是
(3)在碱性溶液中缩二脲能与
 反应得到特征的紫色配合物,其中的阴离子结构如图所示。该配离子中,配位原子是
反应得到特征的紫色配合物,其中的阴离子结构如图所示。该配离子中,配位原子是
(4)氮化铜的晶胞为立方晶胞,其晶胞结构如图所示。

①根据晶胞结构,可判断氮化铜的化学式为
②已知晶胞边长
 ,则最近的两个Cu原子间的距离为
,则最近的两个Cu原子间的距离为
 。(保留小数点后两位)
。(保留小数点后两位)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
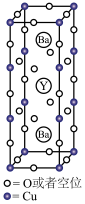
【推荐2】1911年,科学家发现汞在4.2K以下时电阻突然趋近于零——即低温超导性。1986年,科学家又发现了Nb3Ge在23K下具有超导性。1987年2月,赵忠贤及合作者独立发现了在液氮温区(沸点77 K)的高温超导体,其晶胞如图所示,元素组成为Ba-Y-Cu-O(临界温度93 K),推动了国际高温超导研究。赵忠贤院士获得2016年度国家最高科学技术奖。
回答下列问题:
(1)铌Nb位于第五周期,Nb的外围电子排布式为4d45s1,Nb位于_______ 族。
(2)下列关于Ge元素叙述正确的是______ (从下列选项中选择)。
A.Ge晶体属于准金属,且为原子晶体 B.Ge属于p区的过渡金属
C.Ge的第一电离能比As、Se均要小 D.Ge的电负性比C大
(3)Ge(CH3)2Cl2分子的中心原子Ge的杂化方式是______________ 。
(4)NH3也常作制冷剂,其键角_______ (填“大于”或“小于”)109°28′,主要原因是___________________________________________________________________________ 。
(5)图示材料的理想化学式(无空位时)为___________________ ,若Y(钇)元素的化合价为+3,则Cu的平均化合价为__________ 。

回答下列问题:
(1)铌Nb位于第五周期,Nb的外围电子排布式为4d45s1,Nb位于
(2)下列关于Ge元素叙述正确的是
A.Ge晶体属于准金属,且为原子晶体 B.Ge属于p区的过渡金属
C.Ge的第一电离能比As、Se均要小 D.Ge的电负性比C大
(3)Ge(CH3)2Cl2分子的中心原子Ge的杂化方式是
(4)NH3也常作制冷剂,其键角
(5)图示材料的理想化学式(无空位时)为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)①Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有___________ 个铜原子。
②Al单质为面心立方晶体,其晶胞参数a=0.405 nm,晶胞中铝原子的配位数为___________ 。列式表示Al单质的密度___________ g·cm-3(不必计算出结果)。
(2)前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子数相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2.A、B和D三种元素组成的一个化合物的晶胞如图所示。

①该化合物的化学式为___________ ;D的配位数为___________ ;
②列式计算该晶体的密度:___________ g·cm-3。
(3)立方ZnS晶体结构如图所示,其晶胞边长为540.0 pm,密度为___________ g·cm-3(列式并计算),a位置S2-与b位置Zn2+之间的距离为___________ pm(列式表示)。

(1)①Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有
②Al单质为面心立方晶体,其晶胞参数a=0.405 nm,晶胞中铝原子的配位数为
(2)前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子数相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2.A、B和D三种元素组成的一个化合物的晶胞如图所示。

①该化合物的化学式为
②列式计算该晶体的密度:
(3)立方ZnS晶体结构如图所示,其晶胞边长为540.0 pm,密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A、B属于同一短周期元素且相邻,A元素所形成的化合物种类最多,C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数相差为10,基态D、E原子的价电子层中未成对电子数分别为4、2,且原子序数相差为2。
(1)黄血盐是由A、B、C、D四种元素形成的配合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂)。请写出黄血盐的化学式___________ ,黄血盐晶体中各种微粒间的作用力不涉及___________ (填序号)。
a.金属键 b.共价键 c.配位键 d.离子键 e.氢键 f.分子间的作用力
(2)A的简单氢化物的键角比B的简单氢化物键角大,原因是___________ 。
(3)金属C、F晶体的晶胞如下图(金属C采取体心立方堆积),C、F两种晶体晶胞中金属原子的配位数之比为___________ 。金属F的晶胞中,若设其原子半径为r,晶胞的边长为a,根据硬球接触模型,则r = ___________ a,列式表示F原子在晶胞中的空间占有率___________ (不要求计算结果)。

(1)黄血盐是由A、B、C、D四种元素形成的配合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂)。请写出黄血盐的化学式
a.金属键 b.共价键 c.配位键 d.离子键 e.氢键 f.分子间的作用力
(2)A的简单氢化物的键角比B的简单氢化物键角大,原因是
(3)金属C、F晶体的晶胞如下图(金属C采取体心立方堆积),C、F两种晶体晶胞中金属原子的配位数之比为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)已知BA5为离子化合物,写出其电子式______
(2)B基态原子中能量最高的电子,其电子云在空间有______ 个方向,原子轨道呈______ 形
(3)某同学根据上述信息,推断C基态原子的核外电子排布为,
该同学所画的电子排布图违背了______
(4)G位于______ 族______ 区,价电子排布式为______
(5)DE3 中心原子的杂化方式为______ ,用价层电子对互斥理论推测其空间构型为______
(6)检验F元素的方法是______ ,请用原子结构的知识解释产生此现象的原因是______
(7)F元素的晶胞如下图所示,若设该晶胞的密度为a g/cm3,阿伏加德罗常数为NA,F原子的摩尔质量为M,则F原子的半径为______ cm
| A元素的核外电子数和电子层数相等,也是原子半径最小的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是:I1=738kJ/mol I2 = 1451 kJ/mol I3 = 7733kJ/mol I4 = 10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(2)B基态原子中能量最高的电子,其电子云在空间有
(3)某同学根据上述信息,推断C基态原子的核外电子排布为,
该同学所画的电子排布图违背了
(4)G位于
(5)DE3 中心原子的杂化方式为
(6)检验F元素的方法是
(7)F元素的晶胞如下图所示,若设该晶胞的密度为a g/cm3,阿伏加德罗常数为NA,F原子的摩尔质量为M,则F原子的半径为

您最近一年使用:0次
【推荐3】钯(Pd)、锌及其化合物在合成酮类物质中有极其重要的作用,如图为合成 的反应过程:
的反应过程:

回答下列问题:
(1)I原子价电子排布式为_________ ,其能量最高的能层是______ (填能层符号)。
(2)H、C、O三种元素的电负性由大到小的顺序为__________ 。
(3) 中碳原子的杂化方式为
中碳原子的杂化方式为__________ 。
(4)ZnCl2溶液中加入足量氨水,发生的反应为ZnCl2+4NH3·H2O=[Zn(NH3)4]Cl2+4H2O
①上述反应涉及的物质中,固态时属于分子晶体的是________ 。
②NH3的空间构型为_____________ 。
③1 mol[Zn(NH3)4]Cl2中含有______ mol σ键。
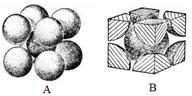
(5)金属钯的堆积方式如图所示:

①该晶胞中原子的空间利用率为_________ (用含π的式子表示)。
②若该晶胞参数a=658 pm,则该晶胞密度为______ (列出计算表达式)g/cm3。
 的反应过程:
的反应过程:
回答下列问题:
(1)I原子价电子排布式为
(2)H、C、O三种元素的电负性由大到小的顺序为
(3)
 中碳原子的杂化方式为
中碳原子的杂化方式为(4)ZnCl2溶液中加入足量氨水,发生的反应为ZnCl2+4NH3·H2O=[Zn(NH3)4]Cl2+4H2O
①上述反应涉及的物质中,固态时属于分子晶体的是
②NH3的空间构型为
③1 mol[Zn(NH3)4]Cl2中含有
(5)金属钯的堆积方式如图所示:

①该晶胞中原子的空间利用率为
②若该晶胞参数a=658 pm,则该晶胞密度为
您最近一年使用:0次



