将3.84g铜与200mL一定浓度的稀硝酸反应,5min时铜恰好完全溶解,产生无色气体NO。待产生的气体全部释放后,向溶液中加入
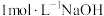 溶液,恰好使溶液中
溶液,恰好使溶液中 全部转化为沉淀。假设溶液体积不变,请计算:
全部转化为沉淀。假设溶液体积不变,请计算:
(1)Cu与稀硝酸反应时,参加反应的硝酸与被还原的硝酸物质的量之比是_______ 。
(2)用硝酸表示前5min内反应的平均速率为_______ 。
(3)原稀硝酸的物质的量浓度是_______  。
。

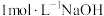 溶液,恰好使溶液中
溶液,恰好使溶液中 全部转化为沉淀。假设溶液体积不变,请计算:
全部转化为沉淀。假设溶液体积不变,请计算:(1)Cu与稀硝酸反应时,参加反应的硝酸与被还原的硝酸物质的量之比是
(2)用硝酸表示前5min内反应的平均速率为
(3)原稀硝酸的物质的量浓度是
 。
。
更新时间:2022-04-23 22:08:50
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】硫有多种含氧酸,如亚硫酸(H2SO3)、硫酸(H2SO4)、焦硫酸、硫代硫酸(H2S2O3)等,其中硫酸最为重要,在工业上有广泛的应用。完成下列计算:
(1)浓硫酸与铜在加热时发生反应,生成二氧化硫气体的体积为4.48 L(标准状况),若将反应后的溶液稀释至500 mL,该溶液中硫酸铜的物质的量浓度为__________ mol·L-1。
(2)焦硫酸(H2SO4·SO3)溶于水,其中的SO3都转化为硫酸,若将445 g焦硫酸溶于水配成4.00 L硫酸,该硫酸的物质的量浓度为____________ mol·L-1。
(1)浓硫酸与铜在加热时发生反应,生成二氧化硫气体的体积为4.48 L(标准状况),若将反应后的溶液稀释至500 mL,该溶液中硫酸铜的物质的量浓度为
(2)焦硫酸(H2SO4·SO3)溶于水,其中的SO3都转化为硫酸,若将445 g焦硫酸溶于水配成4.00 L硫酸,该硫酸的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】将6.5g锌放入足量的稀硫酸中充分反应,得到80mL密度为1.25g/mL的溶液。试计算所得溶液中硫酸锌的物质的量浓度和质量分数各是多少?
______________
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】如图是某学校实验室从化学试剂商店买回来的氢氧化钠试剂标签上的部分内容。某同学从该试剂瓶中取出24.0 g固体,配成1 L溶液,请计算:
氢氧化钠 化学纯(CP)
500 g
品名:氢氧化钠
化学式:NaOH
相对分子质量:40
(1)所得氢氧化钠溶液中溶质的物质的量浓度。_______________________
(2)从所得氢氧化钠溶液中取出200 mL倒入一烧杯中,投入足量的金属铝,完全反应后,产生的气体在标准状况下的体积。__________________________
氢氧化钠 化学纯(CP)
500 g
品名:氢氧化钠
化学式:NaOH
相对分子质量:40
(1)所得氢氧化钠溶液中溶质的物质的量浓度。
(2)从所得氢氧化钠溶液中取出200 mL倒入一烧杯中,投入足量的金属铝,完全反应后,产生的气体在标准状况下的体积。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】氧化还原反应是一类重要的反应,在工农业生产、日常生活中都有广泛的用途。回答下列有关氧化还原的问题。
Ⅰ.氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3-+4H++3e-→NO+2H2O。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)物质(甲)为_________ 。(填化学式)
(2)反应中若产生标况下4.48LNO气体,则转移电子的数目是____________ 。
Ⅱ.亚硝酸钠(NaNO2)像食盐一样有咸味,但有很强的毒性,误食NaNO2会使人中毒。已知亚硝酸钠能发生如下反应:2NaNO2 + 4HI ═ 2NO↑ + 2NaI + I2 + 2H2O
(1)用双线桥标出该反应的电子转移方向及数目:_______ 。氧化剂与还原剂的物质的量之比为______ 。
(2)测定NaNO2的质量分数的过程如下:称取NaNO2粗品0.6 g于锥形瓶中,先加水溶解,再向其中滴加0.1 mol·L-1酸性KMnO4溶液,恰好完全反应时,消耗酸性KMnO4溶液24mL。计算装置C中所得固体中NaNO2的质量分数___________ 。【已知测定过程中发生反应的方程式为MnO4-+NO2-+H+—Mn2++NO3-+H2O(未配平),且杂质不与KMnO4反应】
(3)自来水中的NO3-对人类健康产生危害。为了降低自来水中NO3-的浓度,某研究人员提出两种方案。
①方案a:微碱性条件下用Fe(OH)2还原NO3-,产物为NH3。生成3.4g NH3同时会生成_____ molFe(OH)3。
②方案b:碱性条件下用Al粉还原NO3-,产物是N2。发生的反应可表示如下,完成方程式并配平。
____ Al+____ NO3-+____ ( ) —____ AlO2-+______ N2↑+____ ( )
Ⅰ.氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3-+4H++3e-→NO+2H2O。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)物质(甲)为
(2)反应中若产生标况下4.48LNO气体,则转移电子的数目是
Ⅱ.亚硝酸钠(NaNO2)像食盐一样有咸味,但有很强的毒性,误食NaNO2会使人中毒。已知亚硝酸钠能发生如下反应:2NaNO2 + 4HI ═ 2NO↑ + 2NaI + I2 + 2H2O
(1)用双线桥标出该反应的电子转移方向及数目:
(2)测定NaNO2的质量分数的过程如下:称取NaNO2粗品0.6 g于锥形瓶中,先加水溶解,再向其中滴加0.1 mol·L-1酸性KMnO4溶液,恰好完全反应时,消耗酸性KMnO4溶液24mL。计算装置C中所得固体中NaNO2的质量分数
(3)自来水中的NO3-对人类健康产生危害。为了降低自来水中NO3-的浓度,某研究人员提出两种方案。
①方案a:微碱性条件下用Fe(OH)2还原NO3-,产物为NH3。生成3.4g NH3同时会生成
②方案b:碱性条件下用Al粉还原NO3-,产物是N2。发生的反应可表示如下,完成方程式并配平。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】硫代硫酸钠(Na2S2O3)俗称海波、大苏打,无色透明晶体,易溶于水,遇强酸反应产生硫单质和二氧化硫气体;具有强还原性,与强氧化剂反应产物为SO42-;
(1)Na2S2O3中S元素的化合价为_________ 。
(2)向Na2S2O3溶液中滴加稀硫酸,其反应的离子方程式为____________________________ 。
(3)Na2S2O3溶液与Cl2反应,可作为绵织物漂白后的脱氧剂。该反应的离子方程式为_______ ,要脱去22.4 L Cl2(标准状况下),需要Na2S2O3________ mol。
(4)工业上常用硫化碱法制备海波。其原理是向碳酸钠和硫化钠物质的量之比为1:2的混合液中通入过量的二氧化硫,经蒸发、结晶,即得硫代硫酸钠。其反应的化学方程式为_____ ,其氧化剂为_____________ 。
(1)Na2S2O3中S元素的化合价为
(2)向Na2S2O3溶液中滴加稀硫酸,其反应的离子方程式为
(3)Na2S2O3溶液与Cl2反应,可作为绵织物漂白后的脱氧剂。该反应的离子方程式为
(4)工业上常用硫化碱法制备海波。其原理是向碳酸钠和硫化钠物质的量之比为1:2的混合液中通入过量的二氧化硫,经蒸发、结晶,即得硫代硫酸钠。其反应的化学方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】50 mL浓H2SO4溶液(足量)中加入3.2 g Cu,在加热条件下充分反应:
(1)将题干中反应后的溶液稀释到500 mL,取出50 mL,并向取出液中加入足量的BaCl2溶液,得到沉淀19.81 g,则原浓硫酸的物质的量浓度为____ 。
(2)若题干中浓硫酸的物质的量浓度为a mol/L,投入足量的铜片加热,充分反应后,被还原的硫酸的物质的量n(H2SO4)___ 0.025a mol(填“等于”、“大于”或“小于”)。
(3)反应消耗的H2SO4的物质的量是____ ,生成SO2的体积为(标准状况下)_____ mL。
(1)将题干中反应后的溶液稀释到500 mL,取出50 mL,并向取出液中加入足量的BaCl2溶液,得到沉淀19.81 g,则原浓硫酸的物质的量浓度为
(2)若题干中浓硫酸的物质的量浓度为a mol/L,投入足量的铜片加热,充分反应后,被还原的硫酸的物质的量n(H2SO4)
(3)反应消耗的H2SO4的物质的量是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】钢铁是最重要、用量最大的金属材料之一。完成下列计算:
51.生产1吨含铁96%的生铁,至少需要氧化铁含量70%的赤铁矿(杂质不含铁)_____ 吨。(计算结果保留2位小数)
52.工业炼铁用一氧化碳还原氧化铁时会发生如下一系列反应:
3Fe2O3+CO=2Fe3O4+CO2
Fe3O4+CO=3FeO+CO2
FeO+CO=Fe+CO2
某次实验中,用CO还原4.80 g氧化铁,当固体质量变成4.56 g时,测得此固体中只存在2种氧化物。通过计算确定此固体可能的成分和它们的物质的量之比_____ 。
53.为了测定某碳素钢(假设只含铁和碳)的含碳量,将10.000 g钢样完全溶解于过量的热浓硝酸中,产生了0.300 mol气体(假设气体全部逸出,N2O4已折算为NO2)。气体用50.00 mL 12.00 mol/L的NaOH溶液完全吸收后,只生成两种盐,溶液蒸干后得到不含结晶水的固体32.664 g。计算:
(1)钢样的含碳量_____ 。
(2)参加反应的硝酸的物质的量_____ 。
51.生产1吨含铁96%的生铁,至少需要氧化铁含量70%的赤铁矿(杂质不含铁)
52.工业炼铁用一氧化碳还原氧化铁时会发生如下一系列反应:
3Fe2O3+CO=2Fe3O4+CO2
Fe3O4+CO=3FeO+CO2
FeO+CO=Fe+CO2
某次实验中,用CO还原4.80 g氧化铁,当固体质量变成4.56 g时,测得此固体中只存在2种氧化物。通过计算确定此固体可能的成分和它们的物质的量之比
53.为了测定某碳素钢(假设只含铁和碳)的含碳量,将10.000 g钢样完全溶解于过量的热浓硝酸中,产生了0.300 mol气体(假设气体全部逸出,N2O4已折算为NO2)。气体用50.00 mL 12.00 mol/L的NaOH溶液完全吸收后,只生成两种盐,溶液蒸干后得到不含结晶水的固体32.664 g。计算:
(1)钢样的含碳量
(2)参加反应的硝酸的物质的量
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】实验室里常用铜与稀硝酸制取NO 气体,将一定量铜加入200mL 的稀硝酸中恰好完全反应,生成4.48L (STP) NO,完成下列问题:
(1)反应的离子方程式_______________ 。
(2)稀硝酸的物质的量浓度为多少?___________
(3) 被还原的HNO3的物质的量为多少?________________
(1)反应的离子方程式
(2)稀硝酸的物质的量浓度为多少?
(3) 被还原的HNO3的物质的量为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
名校
【推荐3】氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3-+4H++3e→NO+2H2O ;KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:_______________________________
(2)反应中硝酸体现了_________ 、_________ 性质。
(3)反应中若产生0.2mol气体,则转移电子的物质的量是________ mol。
(4)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是:___________________________________ 。
(1)写出并配平该氧化还原反应的方程式:
(2)反应中硝酸体现了
(3)反应中若产生0.2mol气体,则转移电子的物质的量是
(4)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是:
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】在温度为373K时,将0.100mol无色的N2O4气体放入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4 2NO2的平衡.下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
2NO2的平衡.下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
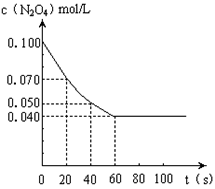
(1)计算在20至40秒时间内,NO2的平均生成速率为____________ mol•L-1•S-1
(2)①该反应的化学平衡常数表达式为__________ ,
(3)求达到平衡状态时N2O4的转化率____________
(4)求平衡时容器内气体压强与反应前的压强之比为__________ (最简整数比)
 2NO2的平衡.下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
2NO2的平衡.下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
(1)计算在20至40秒时间内,NO2的平均生成速率为
(2)①该反应的化学平衡常数表达式为
②求该温度下平衡常数的值
(3)求达到平衡状态时N2O4的转化率
(4)求平衡时容器内气体压强与反应前的压强之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)氢气可由天然气和水反应制备,其主要反应为:
CH4(g)+ 2H2O(g) CO2(g)+4H2(g)
CO2(g)+4H2(g)
反应过程中能量变化如图所示:
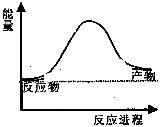
则该反应为_____ 反应(填“吸热”或“放热”)。若已知,破坏1mol化学键需要吸收的热量如下代数式表示:
则根据该反应制取1mol H2要吸收或放出热量为_____________ kJ(用含a b c d字母表示)。
(2)某温度下,10L密闭容器中充入1.8mol CH4和3mol H2O(g),发生CH4+2H2O(g) CO2+4H2反应,反应进行到8s时CO2的浓度为0.08mol/L,则:
CO2+4H2反应,反应进行到8s时CO2的浓度为0.08mol/L,则:
①前8s以H2O(g)表示的平均反应速率为__________ ;
②8s时,混合气体中H2的体积分数为__________ ;
CH4(g)+ 2H2O(g)
 CO2(g)+4H2(g)
CO2(g)+4H2(g)反应过程中能量变化如图所示:

则该反应为
| 化学键 | C—H | O—H | C=O | H—H |
| 吸收热量(kJ/mol) | a | b | c | d |
则根据该反应制取1mol H2要吸收或放出热量为
(2)某温度下,10L密闭容器中充入1.8mol CH4和3mol H2O(g),发生CH4+2H2O(g)
 CO2+4H2反应,反应进行到8s时CO2的浓度为0.08mol/L,则:
CO2+4H2反应,反应进行到8s时CO2的浓度为0.08mol/L,则:①前8s以H2O(g)表示的平均反应速率为
②8s时,混合气体中H2的体积分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】减弱温室效应的方法之一是将CO2回收利用,科学家研究利用回收的CO2制取甲醛,反应的热化学方程式为CO2(g)+2H2(g HCHO(g)+H2O(g) ΔH。实验室在2L密闭容器中进行模拟上述合成HCHO的实验。T1℃时,将体积比为1∶2的CO2和H2混合气体充入容器中,每隔一定时间测得容器内气体压强如表所示:
HCHO(g)+H2O(g) ΔH。实验室在2L密闭容器中进行模拟上述合成HCHO的实验。T1℃时,将体积比为1∶2的CO2和H2混合气体充入容器中,每隔一定时间测得容器内气体压强如表所示:
已知:v(B)=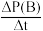 ,则反应开始10min内,用H2的压强变化表示该反应的平均反应速率为
,则反应开始10min内,用H2的压强变化表示该反应的平均反应速率为_____ kPa•min-1。
 HCHO(g)+H2O(g) ΔH。实验室在2L密闭容器中进行模拟上述合成HCHO的实验。T1℃时,将体积比为1∶2的CO2和H2混合气体充入容器中,每隔一定时间测得容器内气体压强如表所示:
HCHO(g)+H2O(g) ΔH。实验室在2L密闭容器中进行模拟上述合成HCHO的实验。T1℃时,将体积比为1∶2的CO2和H2混合气体充入容器中,每隔一定时间测得容器内气体压强如表所示:| 时间/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 压强/kPa | 1.08 | 0.96 | 0.88 | 0.82 | 0.80 | 0.80 | 0.80 |
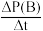 ,则反应开始10min内,用H2的压强变化表示该反应的平均反应速率为
,则反应开始10min内,用H2的压强变化表示该反应的平均反应速率为
您最近一年使用:0次



