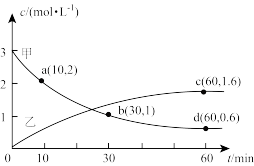
在恒温恒容条件下,发生反应2A(g)+xB(g) 2C(g),反应体系中某物质的浓度c随时间的变化如图中曲线甲、乙所示,已知x为整数。下列说法正确的是
2C(g),反应体系中某物质的浓度c随时间的变化如图中曲线甲、乙所示,已知x为整数。下列说法正确的是
 2C(g),反应体系中某物质的浓度c随时间的变化如图中曲线甲、乙所示,已知x为整数。下列说法正确的是
2C(g),反应体系中某物质的浓度c随时间的变化如图中曲线甲、乙所示,已知x为整数。下列说法正确的是
| A.x=3 |
| B.曲线乙表示的是物质A在反应进程中的浓度变化 |
| C.10~30min内v(C)=0.05mol·L-1·min-1 |
| D.c点对应物质的浓度与d点对应物质的浓度相等 |
21-22高一下·河南·期中 查看更多[4]
河南省名校联盟2021-2022学年高一下学期期中考试化学试题河南省顶级名校2021-2022学年高一下学期5月月考化学试题(已下线)第16练 化学反应的速率与限度-2023年高考化学一轮复习小题多维练(全国通用)湖北省武汉市部分示范学校2022-2023学年高一下学期5月联考化学试题
更新时间:2022-04-29 20:08:11
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】向2L恒容密闭容器中充入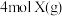 和
和 ,在一定温度下发生反应:
,在一定温度下发生反应: 。2min末测得容器中有1.8molY。下列结论正确的是
。2min末测得容器中有1.8molY。下列结论正确的是
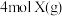 和
和 ,在一定温度下发生反应:
,在一定温度下发生反应: 。2min末测得容器中有1.8molY。下列结论正确的是
。2min末测得容器中有1.8molY。下列结论正确的是A.2min内X的平均反应速率为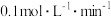 |
| B.容器内压强不变时,反应达到平衡状态 |
C.只有反应达到平衡时,才有 |
D.由于 ,给予足够的时间,X的转化率可达到100% ,给予足够的时间,X的转化率可达到100% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知反应4A(s)+3B(g)⇌2C(g)+D(g)ΔH=-akJ·mol-1(a>0)。恒温下,向2L的恒容密闭容器中加入足量的A和3molB,经2min反应达到平衡,B的体积分数为60%。下列有关说法正确的是
| A.其他条件不变,将容器的体积缩小到1L,v正增大,v逆减小 |
| B.0~2min内用D表示的平均反应速率为0.3mol·L-1·min-1 |
| C.相同条件下,若起始时加入1molC和0.5molD,则达到平衡时,吸收的热量为0.4akJ |
| D.混合气体的密度不再变化,说明可逆反应达到平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】利用CH4可消除NO2的污染,反应原理为:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g),在10L密闭容器中分别加入0.50molCH4和1.2molNO2,测得不同温度下n(CH4)随时间变化的有关实验数据如表所示:下列说法正确的是
N2(g)+CO2(g)+2H2O(g),在10L密闭容器中分别加入0.50molCH4和1.2molNO2,测得不同温度下n(CH4)随时间变化的有关实验数据如表所示:下列说法正确的是
 N2(g)+CO2(g)+2H2O(g),在10L密闭容器中分别加入0.50molCH4和1.2molNO2,测得不同温度下n(CH4)随时间变化的有关实验数据如表所示:下列说法正确的是
N2(g)+CO2(g)+2H2O(g),在10L密闭容器中分别加入0.50molCH4和1.2molNO2,测得不同温度下n(CH4)随时间变化的有关实验数据如表所示:下列说法正确的是| 组别 | 温度/K | 时间/min 物质的量/mol | 0 | 10 | 20 | 40 | 50 |
| ① | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| ② | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | M | 0.15 |
| A.组别①中0~20min内,NO2降解速率为0.25mol·L-1·min-l |
| B.由实验数据可知温度T1>T2 |
| C.40min时,表格中M对应的数据为0.15 |
| D.组别②中,20min时,CO2的浓度为0.32mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在t ℃时,10 L 0.4 mol·L-1 H2O2溶液发生催化分解:2H2O2===2H2O+O2↑,不同时刻测得生成O2的体积如下表,已知反应至6 min时,H2O2分解了50%(已折算为标准状况)
下列叙述正确的是(溶液体积变化忽略不计)( )
| t/min | 0 | 2 | 4 | 6 |
| V(O2)/L | 0.0 | 9.9 | 17.2 | V=? |
| A.0~2 min H2O2平均反应速率比4~6 min慢 |
| B.反应至6 min时,共产生O2 44.8 L |
| C.0~6 min的平均反应速率v(H2O2)≈3.3×10-2 mol·L-1·min-1 |
| D.反应至6 min时,c(H2O2)=0.3 mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】反应A(g)+3B(g) 2C(g)+2D(g)在四种不同情况下的反应速率分别如下,其中反应速率最大的是
2C(g)+2D(g)在四种不同情况下的反应速率分别如下,其中反应速率最大的是
 2C(g)+2D(g)在四种不同情况下的反应速率分别如下,其中反应速率最大的是
2C(g)+2D(g)在四种不同情况下的反应速率分别如下,其中反应速率最大的是| A.vA=0.15 mol·L-1·min-1 | B.vB=0.6 mol·L-1·min-1 |
| C.vC=0.4 mol·L-1·min-1 | D.vD=0.01 mol·L-1·s-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】H2O2分解速率受多种因素影响。实验测得 70 ℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法不正确的是
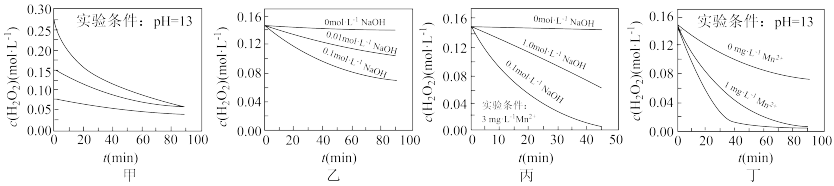

| A.图甲表明,其他条件相同时,H2O2浓度越大,其分解速率越快 |
| B.图乙表明,其他条件相同时,NaOH溶液浓度越小,H2O2分解速率越慢 |
| C.图丙表明,少量Mn2+存在时,溶液碱性越强,H2O2分解速率越快 |
| D.图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】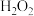 分解速率受多种因素影响。实验测得
分解速率受多种因素影响。实验测得 时不同条件下
时不同条件下 浓度随时间的变化如图所示
浓度随时间的变化如图所示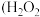 起始浓度均为
起始浓度均为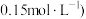 。下列说法正确的是
。下列说法正确的是
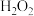 分解速率受多种因素影响。实验测得
分解速率受多种因素影响。实验测得 时不同条件下
时不同条件下 浓度随时间的变化如图所示
浓度随时间的变化如图所示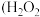 起始浓度均为
起始浓度均为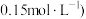 。下列说法正确的是
。下列说法正确的是 | 实验条件 | 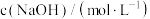 |  浓度 浓度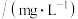 |  |
| ① | 0 | 0 | |
| ② |  | 0 | |
| ③ |  | 3 | |
| ④ |  | 3 |
A. 内,④条件下 内,④条件下 的平均反应速率为 的平均反应速率为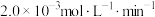 |
B.分析②③条件可知, 浓度越大, 浓度越大, 分解速率越慢 分解速率越慢 |
C.少量 存在时,溶液碱性越强, 存在时,溶液碱性越强, 分解速率越快 分解速率越快 |
D.分析①②条件可知,无 时,碱性条件有利于双氧水的分解 时,碱性条件有利于双氧水的分解 |
您最近一年使用:0次

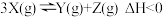 ,反应一段时间后改变某一个外界条件,反应中各时刻X物质的浓度如下表所示。下列说法不正确的是
,反应一段时间后改变某一个外界条件,反应中各时刻X物质的浓度如下表所示。下列说法不正确的是
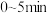 时,该反应的速率为
时,该反应的速率为



