请按要求回答下列问题:
(1)Al2O3能溶于强酸或强碱溶液生成盐和水,则Al2O3是一种_______ (填“酸性”、“碱性”或“两性”) 氧化物。
(2)氨气极易溶于水,其水溶液显_______ (填“酸”、“碱”或“中”)性。
(3)在常温下,将Cl2通入NaOH溶液中,可以得到漂白液。请写出该反应的离子方程式_______ 。
(4)高锰酸钾与浓盐酸在常温下能反应生成氯气,请写出反应的化学方程式_______ 。
(5)等质量的下列气体HCl、NH3、CO2、O2四种气体中,在相同温度和相同压强条件下,体积最大的是_______ 。
(6)设NA为阿伏加德罗常数的数值,如果ag某未知气体中含有的分子数为b,则cg该气体在标准状况下的体积约是_______ L (用NA的式子表示)。
(1)Al2O3能溶于强酸或强碱溶液生成盐和水,则Al2O3是一种
(2)氨气极易溶于水,其水溶液显
(3)在常温下,将Cl2通入NaOH溶液中,可以得到漂白液。请写出该反应的离子方程式
(4)高锰酸钾与浓盐酸在常温下能反应生成氯气,请写出反应的化学方程式
(5)等质量的下列气体HCl、NH3、CO2、O2四种气体中,在相同温度和相同压强条件下,体积最大的是
(6)设NA为阿伏加德罗常数的数值,如果ag某未知气体中含有的分子数为b,则cg该气体在标准状况下的体积约是
21-22高一上·甘肃金昌·期末 查看更多[2]
更新时间:2022-05-13 19:14:54
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某容积固定的密闭容器由可移动的活塞隔成A、B 两室,向B 室充入 1 molN2,A 室加入一定量的X 固体,加热,发生化学反应X 2Y↑+CO2↑+H2O↑,反应结束后活塞的位置如图所示。
2Y↑+CO2↑+H2O↑,反应结束后活塞的位置如图所示。

(1) A 室混合气体的物质的量为______________ ,生成的 CO2在标况下的体积为_____________ 。
(2)Y 是一种极易溶于水的有刺激性气味气体,实验室需要进行尾气处理,下列装置可用于作为Y 气体的尾气处理装置的是________________ 。

(3)实验测得反应后A 室混合气体的质量为 48g,则该混合气体的密度是同温同压条件下氢气密度的_______ 倍,X 的摩尔质量为____________ 。
(4)若在 A 室加入足量碱石灰(碱石灰可吸收 CO2和 H2O,忽略固体所占体积),保持温度不变,最终活塞停留的位置在___________ 刻度,此时容器内气体压强与加碱石灰前气体压强之比为_______________ 。
 2Y↑+CO2↑+H2O↑,反应结束后活塞的位置如图所示。
2Y↑+CO2↑+H2O↑,反应结束后活塞的位置如图所示。
(1) A 室混合气体的物质的量为
(2)Y 是一种极易溶于水的有刺激性气味气体,实验室需要进行尾气处理,下列装置可用于作为Y 气体的尾气处理装置的是

(3)实验测得反应后A 室混合气体的质量为 48g,则该混合气体的密度是同温同压条件下氢气密度的
(4)若在 A 室加入足量碱石灰(碱石灰可吸收 CO2和 H2O,忽略固体所占体积),保持温度不变,最终活塞停留的位置在
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)16 g O2所含原子总数为______ ;与16 g O2物质的量相同的NH3在标准状况下的体积是_______ L;
(2)常温常压下,6.0g SiO2中含有Si-O键的数目为_____ 。
(3)同温同压下,同体积的NH3和H2S气体的质量比为___________ ;同质量的NH3和H2S气体的体积比为___________ 。
(4)在标准状况下,用惰性电极电解饱和食盐水,若阴极上产生44.8L气体,则线路中通过电子的物质的量为___________ 。
(1)16 g O2所含原子总数为
(2)常温常压下,6.0g SiO2中含有Si-O键的数目为
(3)同温同压下,同体积的NH3和H2S气体的质量比为
(4)在标准状况下,用惰性电极电解饱和食盐水,若阴极上产生44.8L气体,则线路中通过电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入 、
、 的混合气体和2mol空气,此时活塞的位置如图所示。
的混合气体和2mol空气,此时活塞的位置如图所示。

(1)A室混合气体所含分子总数为___________ 。(用NA表示阿伏加德罗常数的数值)
(2)实验测得A室混合气体的质量为68g,则该混合气体的密度是同温同压条件下 密度的
密度的___________ 倍。
(3)若将A室 、
、 的混合气体点燃引爆,恢复原温度后,最终活塞停留的位置在
的混合气体点燃引爆,恢复原温度后,最终活塞停留的位置在___________ 刻度,此时容器内气体压强与反应前气体压强之比为___________ 。
 、
、 的混合气体和2mol空气,此时活塞的位置如图所示。
的混合气体和2mol空气,此时活塞的位置如图所示。
(1)A室混合气体所含分子总数为
(2)实验测得A室混合气体的质量为68g,则该混合气体的密度是同温同压条件下
 密度的
密度的(3)若将A室
 、
、 的混合气体点燃引爆,恢复原温度后,最终活塞停留的位置在
的混合气体点燃引爆,恢复原温度后,最终活塞停留的位置在
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】对一定量气体体积的探究。已知1mol不同气体在不同条件下的体积:
回答下列问题:
(1)从表中数据分析得出的结论:
① 任何气体,在标准状况下的体积都约为
任何气体,在标准状况下的体积都约为_______ 。
② 不同的气体,在不同的条件下,体积
不同的气体,在不同的条件下,体积_______ (填“一定”“一定不”或“不一定”)相等。
(2)理论依据:相同条件下,1mol任何气体的体积几乎相等的原因是:①_______ ;②________ 。
(3)应用:在标准状况下,32gO2的体积为_______ 。
(4)等温、等压下,等体积的O2和O3所含分子个数比为_______ ,质量比为_______ 。
| 化学式 | 条件 | 1mol气体体积/L |
| H2 | 0℃,101kPa | 22.4 |
| O2 | 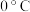 ,101kPa ,101kPa | 22.4 |
| CO | 0℃,101kPa | 22.4 |
| H2 | 0℃,202kPa | 11.2 |
| CO2 | 0℃,202kPa | 11.2 |
| N2 | 273℃,202kPa | 22.4 |
| NH3 | 273℃,202kPa | 22.4 |
(1)从表中数据分析得出的结论:
①
 任何气体,在标准状况下的体积都约为
任何气体,在标准状况下的体积都约为②
 不同的气体,在不同的条件下,体积
不同的气体,在不同的条件下,体积(2)理论依据:相同条件下,1mol任何气体的体积几乎相等的原因是:①
(3)应用:在标准状况下,32gO2的体积为
(4)等温、等压下,等体积的O2和O3所含分子个数比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有下列物质:①NaOH、②氨水、③蔗糖、④氯化铁、⑤氯气、⑥SO2、⑦硫酸铜溶液、⑧氢氧化铝胶体。
(1)属于强电解质的是___________ (填序号,下同);属于非电解质的是___________ 。
(2)区分⑦与⑧的实验方法是___________ (填方法名称)。
(3)写出氯化铁溶于水的电离方程式:___________ 。
(4)现有m g某气体,它由双原子分子构成,它的摩尔质量为Mg▪mol﹣1。若阿伏加德罗常数用NA表示,则:
a.该气体所含原子总数为___________ 个。
b.该气体在标准状况下的体积为___________ L。
(5)在标准状况下,CO和CO2的混合气体质量为36 g,体积为22.4 L,则CO和CO2的体积比是___________ ,CO2质量是___________ g。
(1)属于强电解质的是
(2)区分⑦与⑧的实验方法是
(3)写出氯化铁溶于水的电离方程式:
(4)现有m g某气体,它由双原子分子构成,它的摩尔质量为Mg▪mol﹣1。若阿伏加德罗常数用NA表示,则:
a.该气体所含原子总数为
b.该气体在标准状况下的体积为
(5)在标准状况下,CO和CO2的混合气体质量为36 g,体积为22.4 L,则CO和CO2的体积比是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】高铁酸钠 是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为:
是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为: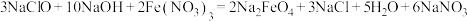 。回答下列问题:
。回答下列问题:
(1)用氯气制备 的反应原理为
的反应原理为___________ (化学方程式)
(2)制备高铁酸钠的反应中 体现了
体现了___________ (填“还原性”、“氧化性”或“氧化性和还原性”)
(3)该反应的离子方程式为___________ 。
(4) 中Fe的价态为
中Fe的价态为___________ 价, 可用于自来水杀菌消毒的原因是
可用于自来水杀菌消毒的原因是___________ 。
(5)该反应中,每消耗 ,生成
,生成 的物质的量
的物质的量___________ mol,转移的电子数目为___________ (用 表示阿伏伽德罗常数的值)
表示阿伏伽德罗常数的值)
 是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为:
是一种新型绿色消毒剂,主要用于饮用水处理。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理为: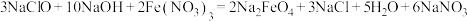 。回答下列问题:
。回答下列问题:(1)用氯气制备
 的反应原理为
的反应原理为(2)制备高铁酸钠的反应中
 体现了
体现了(3)该反应的离子方程式为
(4)
 中Fe的价态为
中Fe的价态为 可用于自来水杀菌消毒的原因是
可用于自来水杀菌消毒的原因是(5)该反应中,每消耗
 ,生成
,生成 的物质的量
的物质的量 表示阿伏伽德罗常数的值)
表示阿伏伽德罗常数的值)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)根据分类的方法可以预测物质的性质及可能发生的变化。SiO2是普通玻璃的主要成分,与CO2一样是酸性氧化物,写出SiO2溶于NaOH溶液的化学方程式:___________ 。
(2)根据所学,写出一个H2O既做氧化剂,又做还原剂的化学反应方程式___________ 。
(3)将Cl2通入NaOH溶液,充分反应后测得溶液中ClO-与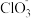 个数比为3:1,则被氧化与被还原的氯元素质量比为
个数比为3:1,则被氧化与被还原的氯元素质量比为___________ ;离子方程式为___________ 。
(4)H2与Cl2混合点燃,充分反应后,将气体通入含有40 g NaOH的溶液中恰好完全反应,则混合气体中Cl2质量为___________ 。
(5)向FeBr2溶液中通入一定量的Cl2,充分反应后,测得游离态的溴元素和化合态的溴元素质量比为1:1,写出反应的离子方程式___________ 。
(6)将醋酸(CH3COOH)溶液滴入到Na2CO3溶液中,开始时发生的离子方程式是___________ 。将Na2CO3溶液滴入到醋酸(CH3COOH)溶液中,开始时发生的离子方程式是___________ 。
(7)在碱性条件下,Cl2可将废水中的CN-氧化为无毒的N2和 ,该过程反应的离子方程式为
,该过程反应的离子方程式为___________ 。
(8)在一定条件下,实验室分别以过氧化氢、高锰酸钾、氯酸钾、过氧化钠为原料制取氧气,当制得相同质量的氧气时,四个反应中转移的电子数之比为___________ 。
(1)根据分类的方法可以预测物质的性质及可能发生的变化。SiO2是普通玻璃的主要成分,与CO2一样是酸性氧化物,写出SiO2溶于NaOH溶液的化学方程式:
(2)根据所学,写出一个H2O既做氧化剂,又做还原剂的化学反应方程式
(3)将Cl2通入NaOH溶液,充分反应后测得溶液中ClO-与
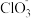 个数比为3:1,则被氧化与被还原的氯元素质量比为
个数比为3:1,则被氧化与被还原的氯元素质量比为(4)H2与Cl2混合点燃,充分反应后,将气体通入含有40 g NaOH的溶液中恰好完全反应,则混合气体中Cl2质量为
(5)向FeBr2溶液中通入一定量的Cl2,充分反应后,测得游离态的溴元素和化合态的溴元素质量比为1:1,写出反应的离子方程式
(6)将醋酸(CH3COOH)溶液滴入到Na2CO3溶液中,开始时发生的离子方程式是
(7)在碱性条件下,Cl2可将废水中的CN-氧化为无毒的N2和
 ,该过程反应的离子方程式为
,该过程反应的离子方程式为(8)在一定条件下,实验室分别以过氧化氢、高锰酸钾、氯酸钾、过氧化钠为原料制取氧气,当制得相同质量的氧气时,四个反应中转移的电子数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)实验室少量的金属钠保存在___________ 中,取用时用到的仪器和用品有小刀、玻璃片、滤纸和____________ , 剩余的钠应_______________ ;将一小块钠投入到硫酸铜溶液中,反应的离子方程式为______________________________________ ,观察到的现象为_____________ (填写标号)。
(2)实验室制氯气的化学反应方程式为_________________________________ ;氯气为有毒气体,需用氢氧化钠溶液进行尾气处理,请完成该离子方程式____________ , 该原理还可用于工业制______________ 。
(3)下列物质既能与盐酸反应,又能与烧碱溶液反应的是________________________________
a.钠浮在液面上四处游动 b.钠融成了一个闪亮的小球
c.溶液中有蓝色沉淀生成 d.溶液中有红色固体析出
(2)实验室制氯气的化学反应方程式为
(3)下列物质既能与盐酸反应,又能与烧碱溶液反应的是
a. Al b. Mg c. CH3COONH4 d. NaHCO3 e. Al2O3
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有下列4种物质:①Cl2、② NH3.③浓H2SO4、④A12O3。其中,能与水反应生成两种酸的是__ (填序号,下同);与强酸、强碱溶液均可反应生成盐的是______ ;能使湿润的红色石蕊试纸变蓝的是___ ;能使蔗糖变黑并有气体生成的是_____ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】葡萄酒的酿造:葡萄酒是由葡萄汁发酵而成的。在酿造葡萄酒的过程中面临两大问题:一是在葡萄汁发酵过程中产生的杂菌会影响葡萄酒的酿造和保存;二是葡萄酒中所含的还原性物质一旦被氧化,葡萄酒的果香味就会消失,影响口感。在酿酒实践中,人们发现二氧化硫可以解决这两大问题。某同学拟设计实验探究SO2能解决以上问题的原因。
(1)“封管实验”具有简易、方便、节约、绿色等优点,下列关于三个“封管实验”(夹持装置未画出)的说法错误的是

(2)将 SO2气体通入 BaCl2溶液中,没有看到明显现象,再通入一种气体(或加入一种物质)后,可产生一种沉淀,该气体(或物质)不可能是
(3)实验室一般用亚硫酸钠固体和质量分数为 70%左右的浓硫酸反应,反应的化学方程式为_______ ,不选择稀硫酸的原因是_______ 。
(4)二氧化硫的水溶液能导电,有同学据此认为SO2是电解质,谈谈你的看法_____ ;该水溶液放置一段时间后,pH减小,此过程发生反应的离子方程式为____ 。
(5)中华人民共和国国家标准(G2762022)规定葡萄酒中 SO2最大使用量为 0.25g·L−1, 取 300.00mL 葡萄酒,通过适当的方法使所含 SO2全部逸出并用 H2O2将其全部氧化为 H2SO4, 消耗浓度为 0.0900mol·L-1NaOH 标准溶液 25mL,该葡萄酒中 SO2含量为_______ g·L−1。
(1)“封管实验”具有简易、方便、节约、绿色等优点,下列关于三个“封管实验”(夹持装置未画出)的说法错误的是

| A.加热时,①中白色固体从下部转移到上部 |
| B.加热时,②中溶液从红色变浅至几乎无色,冷却后又恢复红色 |
| C.加热时,③中溶液变红,冷却后溶液红色褪去 |
| D.三个“封管实验”中所发生的化学反应都是可逆反应 |
| A.Cl2 | B.NH3 | C.CO2 | D.H2S |
(4)二氧化硫的水溶液能导电,有同学据此认为SO2是电解质,谈谈你的看法
(5)中华人民共和国国家标准(G2762022)规定葡萄酒中 SO2最大使用量为 0.25g·L−1, 取 300.00mL 葡萄酒,通过适当的方法使所含 SO2全部逸出并用 H2O2将其全部氧化为 H2SO4, 消耗浓度为 0.0900mol·L-1NaOH 标准溶液 25mL,该葡萄酒中 SO2含量为
您最近一年使用:0次




