(1)实验室少量的金属钠保存在___________ 中,取用时用到的仪器和用品有小刀、玻璃片、滤纸和____________ , 剩余的钠应_______________ ;将一小块钠投入到硫酸铜溶液中,反应的离子方程式为______________________________________ ,观察到的现象为_____________ (填写标号)。
(2)实验室制氯气的化学反应方程式为_________________________________ ;氯气为有毒气体,需用氢氧化钠溶液进行尾气处理,请完成该离子方程式____________ , 该原理还可用于工业制______________ 。
(3)下列物质既能与盐酸反应,又能与烧碱溶液反应的是________________________________
a.钠浮在液面上四处游动 b.钠融成了一个闪亮的小球
c.溶液中有蓝色沉淀生成 d.溶液中有红色固体析出
(2)实验室制氯气的化学反应方程式为
(3)下列物质既能与盐酸反应,又能与烧碱溶液反应的是
a. Al b. Mg c. CH3COONH4 d. NaHCO3 e. Al2O3
16-17高一下·黑龙江牡丹江·开学考试 查看更多[2]
更新时间:2017/03/01 11:26:53
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】新冠疫情的发生,消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一,而氯气是制取消毒液的重要原料之一。
请回答下列问题:
(1)请写出舍勒发现氯气的化学反应方程式___________________________________ ,若收集到标准状况下3.36LCl2,则被氧化的HCl的物质的量为_____________ mol。
(2)84消毒液(主要成分是NaClO)是常用的消毒剂,工业上将氯气通入烧碱溶液中制取84消毒液,写出此反应的离子方程式_______________________________________ ,若要制取1.5L 2 mol/L的84消毒液,则需要标准状况下___________ L 氯气。
(3)新冠疫情下,人们对杀菌消毒特别重视,曾有报道某居民将84消毒液与洁厕灵(主要成分是浓盐酸)混合使用而中毒,请解释原因__________________________________ (用化学方程式表示), 该反应中氧化剂是______________ 。
请回答下列问题:
(1)请写出舍勒发现氯气的化学反应方程式
(2)84消毒液(主要成分是NaClO)是常用的消毒剂,工业上将氯气通入烧碱溶液中制取84消毒液,写出此反应的离子方程式
(3)新冠疫情下,人们对杀菌消毒特别重视,曾有报道某居民将84消毒液与洁厕灵(主要成分是浓盐酸)混合使用而中毒,请解释原因
您最近一年使用:0次
【推荐2】自舍勒发现氯气可以作为消毒剂以来,人们陆续发现和使用了形形色色的消毒剂。
(1)舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一。请写出实验室用 和浓盐酸制氯气的化学反应方程式,并用双线桥表示电子的转移
和浓盐酸制氯气的化学反应方程式,并用双线桥表示电子的转移_______ 。反应中盐酸表现出的性质有_______ 。
(2)根据世界环保联盟的要求,二氧化氯(ClO2)消毒剂将逐渐取代 成为水的消毒剂。工业上常用
成为水的消毒剂。工业上常用 和
和 (已知
(已知 具有很强的还原性,易被氧化成
具有很强的还原性,易被氧化成 )溶液混合并加入稀
)溶液混合并加入稀 酸化后制得
酸化后制得 ,反应的离子方程式为:
,反应的离子方程式为:_______ 。
(3)高铁酸钾 是新型高效、多功能、绿色消毒剂。
是新型高效、多功能、绿色消毒剂。
①湿法制备高铁酸钾的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、
、 ,写出湿法制备高铁酸钾的离子方程式
,写出湿法制备高铁酸钾的离子方程式_______ 。
②如下图所示,用 氧化
氧化 也可以制备高铁酸钾,反应原理为:
也可以制备高铁酸钾,反应原理为: 。
。
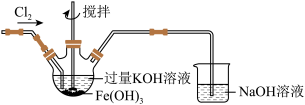
反应后取出三口瓶中的溶液于试管中,加入稀 ,后产生黄绿色气体
,后产生黄绿色气体 ,同时检测到溶液中存在
,同时检测到溶液中存在 ;制备高铁酸钾的实验中,氧化性:
;制备高铁酸钾的实验中,氧化性:
_______  (填“>”、“<”或“=”),试管中发生反应再次产生
(填“>”、“<”或“=”),试管中发生反应再次产生 的实验中,氧化性:
的实验中,氧化性:
_______  (填“>”“<”或“=”),试说明影响
(填“>”“<”或“=”),试说明影响 和
和 氧化性强弱的因素
氧化性强弱的因素_______ 。
(1)舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一。请写出实验室用
 和浓盐酸制氯气的化学反应方程式,并用双线桥表示电子的转移
和浓盐酸制氯气的化学反应方程式,并用双线桥表示电子的转移(2)根据世界环保联盟的要求,二氧化氯(ClO2)消毒剂将逐渐取代
 成为水的消毒剂。工业上常用
成为水的消毒剂。工业上常用 和
和 (已知
(已知 具有很强的还原性,易被氧化成
具有很强的还原性,易被氧化成 )溶液混合并加入稀
)溶液混合并加入稀 酸化后制得
酸化后制得 ,反应的离子方程式为:
,反应的离子方程式为:(3)高铁酸钾
 是新型高效、多功能、绿色消毒剂。
是新型高效、多功能、绿色消毒剂。①湿法制备高铁酸钾的反应体系中有六种微粒:
 、
、 、
、 、
、 、
、 、
、 ,写出湿法制备高铁酸钾的离子方程式
,写出湿法制备高铁酸钾的离子方程式②如下图所示,用
 氧化
氧化 也可以制备高铁酸钾,反应原理为:
也可以制备高铁酸钾,反应原理为: 。
。
反应后取出三口瓶中的溶液于试管中,加入稀
 ,后产生黄绿色气体
,后产生黄绿色气体 ,同时检测到溶液中存在
,同时检测到溶液中存在 ;制备高铁酸钾的实验中,氧化性:
;制备高铁酸钾的实验中,氧化性:
 (填“>”、“<”或“=”),试管中发生反应再次产生
(填“>”、“<”或“=”),试管中发生反应再次产生 的实验中,氧化性:
的实验中,氧化性:
 (填“>”“<”或“=”),试说明影响
(填“>”“<”或“=”),试说明影响 和
和 氧化性强弱的因素
氧化性强弱的因素
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】完成下列填空:
(1)标况下,0.66g某气态氧化物RO2体积为336mL,此氧化物的摩尔质量为_______ ,R的相对原子质量为_______ 。
(2)相同质量的CO和CO2,它们所含的原子数之比为_______ 。
(3)同温同压下,A容器中充满O2,B容器中充满O3。若两容器中所含原子总数相等,则A容器和B容器的容积比是_______ ,密度之比为_______ ,质量之比为_______ 。
(4)写出实验室制氯气的化学方程式_______ ,在此过程中呈酸性的HCl与参加反应的总HCl的质量之比为_______ ,每产生1mol氯气转移电子数为 _______ 。
(5)配平化学方程式:_______ 。
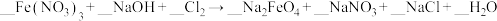
(1)标况下,0.66g某气态氧化物RO2体积为336mL,此氧化物的摩尔质量为
(2)相同质量的CO和CO2,它们所含的原子数之比为
(3)同温同压下,A容器中充满O2,B容器中充满O3。若两容器中所含原子总数相等,则A容器和B容器的容积比是
(4)写出实验室制氯气的化学方程式
(5)配平化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】化学与我们的生活、生产、环境等息息相关。回答下列问题:
(1)明矾的化学式为KAl(SO4)2·12H2O,它常用于净水。明矾放入水中起净水作用的物质是_______ 。明矾与过量NaOH溶液反应的离子方程式是_______ 。
(2)维生素C能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有_______ 性,该转化反应中 Fe3+作_______ 剂。
(3)某无土栽培用的营养液中,c( ):c(
):c( ):c(K+):c(Cl-)=8:4:9:9.若用NH4Cl、KCl、K2SO4 来配制该营养液,则这三种盐的物质的量之比为
):c(K+):c(Cl-)=8:4:9:9.若用NH4Cl、KCl、K2SO4 来配制该营养液,则这三种盐的物质的量之比为_______ 。
(4)某化工厂的贮氯罐意外发生泄漏,消防员向贮氯罐周围空气中喷洒稀NaOH溶液,目的是(用离子方程式表示)_______ 。 为了厂区和周围群众安全,组织群众疏散的地方应是_______ (填序号)。
A.顺风高坡处 B.逆风高坡处 C.顺风低洼处 D.逆风低洼处
(5)在鲜活鱼的长途运输中,需在水中加入供氧剂。Na2O2(易溶于水)、CaO2 (微溶于水)都可与水发生反应生成碱和氧气。7.8 g Na2O2中阴离子的物质的量为_______ ,当它 与CO2完全反应时,转移的电子数目为_______ 。这两种物质中选_______ 作为供氧剂更好,理由是_______ 。
(1)明矾的化学式为KAl(SO4)2·12H2O,它常用于净水。明矾放入水中起净水作用的物质是
(2)维生素C能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
(3)某无土栽培用的营养液中,c(
 ):c(
):c( ):c(K+):c(Cl-)=8:4:9:9.若用NH4Cl、KCl、K2SO4 来配制该营养液,则这三种盐的物质的量之比为
):c(K+):c(Cl-)=8:4:9:9.若用NH4Cl、KCl、K2SO4 来配制该营养液,则这三种盐的物质的量之比为(4)某化工厂的贮氯罐意外发生泄漏,消防员向贮氯罐周围空气中喷洒稀NaOH溶液,目的是(用离子方程式表示)
A.顺风高坡处 B.逆风高坡处 C.顺风低洼处 D.逆风低洼处
(5)在鲜活鱼的长途运输中,需在水中加入供氧剂。Na2O2(易溶于水)、CaO2 (微溶于水)都可与水发生反应生成碱和氧气。7.8 g Na2O2中阴离子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】“84消毒液”的有效成分为 ,不可与酸性清洁剂混用的原因是
,不可与酸性清洁剂混用的原因是__________________________ (用离子方程式表示)。
 ,不可与酸性清洁剂混用的原因是
,不可与酸性清洁剂混用的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】“84消毒液”是家居常用的防疫用品,某化学小组同学查看包装说明,得到如下信息:
【有效成分】NaClO
【规格】1000mL
【浓度】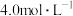
【使用说明】i.按一定比例稀释后使用。
ii.不得与酸性产品(如洁厕灵)同时使用。
小组同学进行了如下实验,回答下列问题:
(1)稀释:将“84消毒液”原液稀释配制成 的溶液。
的溶液。
①稀释时,需要取用___________ mL“84消毒液”原液。
②下列操作会使溶液中NaClO浓度偏低的是___________ (填标号)
A.取用久置的“84消毒液“原液进行稀释
B.量取“84消毒液“原液时,仰视读数
C.定容时,俯视刻度线
D.定容摇匀后,液面低于刻度线,再加水至刻度线
(2)已知:洁厕灵的主要化学成分是盐酸。同学们利用示装置探究84消毒液与洁厕灵不能混用的原因。___________ ,淀粉KI试纸上发生反应的离子反应方程式为___________ 。
②棉花团蘸取的溶液A是___________ ,用离子方程式说明其作用是___________ 。
(3)某同学设计实验探究84消毒液(主要成分为次氯酸钠)的漂白性。
I.在2mL84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
II.在2mL84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
III.在不同温度时,测得84消毒液ORP值随时间的变化曲线如图所示。
①实验I、II现象不同的原因是为___________ 。
②实验III的结论及可能原因是___________ 。
【有效成分】NaClO
【规格】1000mL
【浓度】
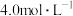
【使用说明】i.按一定比例稀释后使用。
ii.不得与酸性产品(如洁厕灵)同时使用。
小组同学进行了如下实验,回答下列问题:
(1)稀释:将“84消毒液”原液稀释配制成
 的溶液。
的溶液。①稀释时,需要取用
②下列操作会使溶液中NaClO浓度偏低的是
A.取用久置的“84消毒液“原液进行稀释
B.量取“84消毒液“原液时,仰视读数
C.定容时,俯视刻度线
D.定容摇匀后,液面低于刻度线,再加水至刻度线
(2)已知:洁厕灵的主要化学成分是盐酸。同学们利用示装置探究84消毒液与洁厕灵不能混用的原因。
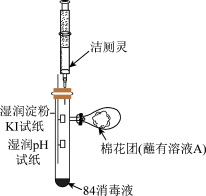
②棉花团蘸取的溶液A是
(3)某同学设计实验探究84消毒液(主要成分为次氯酸钠)的漂白性。
I.在2mL84消毒液中加入2mL水后,放入红色纸片,观察到纸片慢慢褪色。
II.在2mL84消毒液中加入2mL白醋后,放入红色纸片,观察到纸片迅速褪色。
III.在不同温度时,测得84消毒液ORP值随时间的变化曲线如图所示。
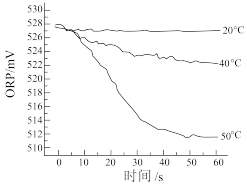
①实验I、II现象不同的原因是为
②实验III的结论及可能原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下列各组物质:①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与FeCl3溶液 ⑤Cl2与NaOH溶液 ⑥Fe与HNO3溶液 ⑦Fe与H2SO4溶液 ⑧Na与O2
(1)由于浓度不同而发生不同氧化还原反应的是_______ (填序号,下同)。
(2)由于温度不同而发生不同氧化还原反应的是_______ 。
(3)氧化还原反应不受浓度、温度影响的是_______ 。
(1)由于浓度不同而发生不同氧化还原反应的是
(2)由于温度不同而发生不同氧化还原反应的是
(3)氧化还原反应不受浓度、温度影响的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按照要求写出下列相关方程式
(1)写出相应电解质在水中的电离方程式
①碳酸氢钠___________ 。
②硫酸氢钠___________ 。
(2)写出相应离子方程式
①钠与水的反应___________ 。
②过氧化钠与水的反应___________ 。
③已知氧化性: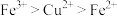 ,将足量Cu投入至FeCl3溶液中
,将足量Cu投入至FeCl3溶液中___________
④向Ba(OH)2溶液中滴加NaHSO4溶液至Ba2+沉淀完全___________ 。继续向上述溶液中滴加NaHSO4溶液至过量___________
⑤已知还原性: ,向FeBr2溶液中通入少量Cl2
,向FeBr2溶液中通入少量Cl2___________ ;向FeI2溶液中通入和Fe2+等数目的Cl2___________ 。
(3)写出相应化学方程式
①钠在空气中加热___________ 。
②制备氢氧化铁胶体的反应___________ 。
(4)用双线桥法表示下列反应的电子转移方向和数目___________ 。
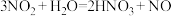
(5)用单线桥法表示下列反应的电子转移方向和数目___________ 。

(6)配平下列方程式
①超氧化钾(KO2)与水的反应:___________ 。
___________KO2+___________H2O→___________KOH+___________O2↑+___________H2O2
②___________ 。
___________ +___________ClO-→N2↑+Cl-+___________+___________
+___________ClO-→N2↑+Cl-+___________+___________
(1)写出相应电解质在水中的电离方程式
①碳酸氢钠
②硫酸氢钠
(2)写出相应离子方程式
①钠与水的反应
②过氧化钠与水的反应
③已知氧化性:
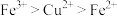 ,将足量Cu投入至FeCl3溶液中
,将足量Cu投入至FeCl3溶液中④向Ba(OH)2溶液中滴加NaHSO4溶液至Ba2+沉淀完全
⑤已知还原性:
 ,向FeBr2溶液中通入少量Cl2
,向FeBr2溶液中通入少量Cl2(3)写出相应化学方程式
①钠在空气中加热
②制备氢氧化铁胶体的反应
(4)用双线桥法表示下列反应的电子转移方向和数目
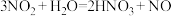
(5)用单线桥法表示下列反应的电子转移方向和数目

(6)配平下列方程式
①超氧化钾(KO2)与水的反应:
___________KO2+___________H2O→___________KOH+___________O2↑+___________H2O2
②
___________
 +___________ClO-→N2↑+Cl-+___________+___________
+___________ClO-→N2↑+Cl-+___________+___________
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有下列物质:
①KCl ②CH4 ③NH4NO3 ④I2 ⑤Na2O2 ⑥HClO4 ⑦N2 ⑧CO ⑨SO2 ⑩金刚石 ⑪CH3CH2OH ⑫MgO ⑬MgCl2 ⑭KOH ⑮HCl ⑯Al2O3
请回答下列问题。
(1)两性氧化物是___ (填序号),其电子式为___ 。
(2)最简单的有机化合物是___ (填序号),用电子式表示其形成过程:___ 。
(3)属于共价化合物的是___ (填序号),含有共价键的离子化合物是___ (填序号)。
(4)由两种元素组成,且含有离子键和共价键的化合物为___ (填序号),这两种元素的单质反应生成该化合物的化学方程式为___ 。
①KCl ②CH4 ③NH4NO3 ④I2 ⑤Na2O2 ⑥HClO4 ⑦N2 ⑧CO ⑨SO2 ⑩金刚石 ⑪CH3CH2OH ⑫MgO ⑬MgCl2 ⑭KOH ⑮HCl ⑯Al2O3
请回答下列问题。
(1)两性氧化物是
(2)最简单的有机化合物是
(3)属于共价化合物的是
(4)由两种元素组成,且含有离子键和共价键的化合物为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】完成下列化学用语:
(1)书写电离方程式: NaClO:__________ ,一水合氨:__________ 。
(2)某金属氯化物MCl240.5g含有0.6mlCl-,MCl2的摩尔质量__________ 。
(3)工业上用电解饱和食盐水制Cl2,写出该反应的化学方程式:__________
(4)小块钠投入到水中,写出该反应的化学方程式:__________
(5)工厂里常用浓氨水来检验氯气管道是否泄漏,其原理为:8NH3+3Cl2=6NH4Cl+N2,请指出此反应中还原剂为__________ (化学式)。
(6)相同温度和体积的A和B两容器,A容器中充满O2,B容器中充满O3,若密度相同,则氧气和臭氧的物质的量之比为:__________
(1)书写电离方程式: NaClO:
(2)某金属氯化物MCl240.5g含有0.6mlCl-,MCl2的摩尔质量
(3)工业上用电解饱和食盐水制Cl2,写出该反应的化学方程式:
(4)小块钠投入到水中,写出该反应的化学方程式:
(5)工厂里常用浓氨水来检验氯气管道是否泄漏,其原理为:8NH3+3Cl2=6NH4Cl+N2,请指出此反应中还原剂为
(6)相同温度和体积的A和B两容器,A容器中充满O2,B容器中充满O3,若密度相同,则氧气和臭氧的物质的量之比为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】元素的价——类二维图是我们学习元素及其化合物相关知识的重要模型和工具,图为钠的价——类二维图。请回答以下问题:

(1)从核心元素价态的视角看,NaH中H元素的化合价为_______ ,从H元素的价态分析,NaH常用作_______ (填“氧化剂”或“还原剂”)。已知NaH与水的反应为: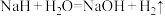 ,则标准状况下生成4.48L
,则标准状况下生成4.48L 时转移电子物质的量是
时转移电子物质的量是_______ 。
(2)钠是一种活泼性很强的金属,钠单质通常保存在_______ 中。
(3)二维图中缺失① 中某种淡黄色固体能做供氧剂,该固体的化学式为_______ ,其中阴阳离子的个数比为_______
(4)金属钠与水反应的离子方程式是_______ 。
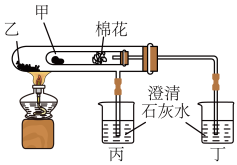
(5)利用如图实验比较碳酸钠和碳酸氢钠的热稳定性,甲试管内放的是碳酸氢钠,写出实验过程中反应的化学方程式:_______ 。

(1)从核心元素价态的视角看,NaH中H元素的化合价为
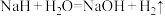 ,则标准状况下生成4.48L
,则标准状况下生成4.48L 时转移电子物质的量是
时转移电子物质的量是(2)钠是一种活泼性很强的金属,钠单质通常保存在
(3)二维图中缺失① 中某种淡黄色固体能做供氧剂,该固体的化学式为
(4)金属钠与水反应的离子方程式是
(5)利用如图实验比较碳酸钠和碳酸氢钠的热稳定性,甲试管内放的是碳酸氢钠,写出实验过程中反应的化学方程式:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据物质及其化合物的性质填空。
(1)为检验市售煤油中是否掺有水,可向煤油样品中加少许白色粉末_______ (填试剂化学式);也可向煤油样品中加入一小块金属钠,若观察到_______ 现象,就可说明煤油中掺有水,写出相关的离子反应方程式_______ 。
(2)镁着火不能用二氧化碳来灭火,理由是_______ (用化学方程式表示)。
(3)铝是应用最广泛的金属之一,铝的化合物在生产和生活中也有许多用途。
①铝是是一种既能与酸反应又能与碱反应的金属,请写出铝与氢氧化钠溶液反应的离子反应方程式:_______ 。
②将7.8g过氧化钠投入500mL0.1mol/L氯化铝溶液中,可观察到的现象是_______ 。
A.放出无色无味的气体,生成大量白色沉淀
B.放出无色无味的气体,生成白色沉淀后恰好溶解
C.放出无色无味的气体,生成白色沉淀后部分溶解
D.无任何现象
(1)为检验市售煤油中是否掺有水,可向煤油样品中加少许白色粉末
(2)镁着火不能用二氧化碳来灭火,理由是
(3)铝是应用最广泛的金属之一,铝的化合物在生产和生活中也有许多用途。
①铝是是一种既能与酸反应又能与碱反应的金属,请写出铝与氢氧化钠溶液反应的离子反应方程式:
②将7.8g过氧化钠投入500mL0.1mol/L氯化铝溶液中,可观察到的现象是
A.放出无色无味的气体,生成大量白色沉淀
B.放出无色无味的气体,生成白色沉淀后恰好溶解
C.放出无色无味的气体,生成白色沉淀后部分溶解
D.无任何现象
您最近一年使用:0次



