下列实验操作或做法正确且能达到目的的是
| 选项 | 操作或做法 | 目的 |
| A | 向盛有Na2SO3固体的锥形瓶中滴加稀盐酸,产生无色气体 | 证明氯元素的非金属性强于硫元素 |
| B | 实验室将生成的乙酸乙酯导入饱和的Na2CO3溶液中 | 可使产品更加纯净 |
| C | 向2支盛有5mL不同浓度Na2HSO3溶液的试管中同时加入2mL5%H2O2溶液,观察实验现象 | 探究浓度对反应速率的影响 |
| D | 向硝酸酸化的A溶液中滴加BaCl2溶液 | 检验A溶液中含有SO |
| A.A | B.B | C.C | D.D |
更新时间:2022-06-29 10:20:48
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某研究小组用下图装置探究NaCl溶液对钢铁腐蚀的影响。

实验Ⅰ:向烧杯a、b中各加入30mL3.5%的NaCl溶液,闭合K,指针未发生偏转。加热烧杯a,指针向右偏转。
取a、b中溶液少量,滴加K3[Fe(CN)6]溶液,a中出现蓝色沉淀,b中无变化。改变NaCl溶液的浓度继续实验,记录如下:
查阅资料:在饱和NaCl溶液中O2浓度较低,钢铁不易被腐蚀。
下列说法不正确 的是:

实验Ⅰ:向烧杯a、b中各加入30mL3.5%的NaCl溶液,闭合K,指针未发生偏转。加热烧杯a,指针向右偏转。
取a、b中溶液少量,滴加K3[Fe(CN)6]溶液,a中出现蓝色沉淀,b中无变化。改变NaCl溶液的浓度继续实验,记录如下:
| 实验 | a | b | 指针偏转方向 |
| Ⅱ | 0.1% | 0.01% | 向右 |
| Ⅲ | 0.1% | 3.5% | 向左 |
| Ⅳ | 3.5% | 饱和溶液 | 向右 |
下列说法
| A.实验Ⅰ加热后,指针发生偏转的原因可能是温度升高,Fe还原性增强,反应速率加快 |
| B.实验Ⅱ中b作正极 |
| C.甲同学由实验Ⅱ、Ⅲ、Ⅳ得出结论NaCl溶液的浓度越大,Fe越容易被腐蚀 |
| D.根据上述实验,对钢铁腐蚀有影响的因素是:温度、NaCl溶液的浓度、O2的浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】硫酸的工业用途非常广泛,可用于制造化肥、除铁锈、作电解液等。工业制硫酸的关键一步是将SO2氧化为SO3,该反应为2SO2+O2 2SO3。但该反应速率小,无法投入工业化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造硫酸的生产工艺。材料中的反应为放热反应,下列说法正确的是
2SO3。但该反应速率小,无法投入工业化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造硫酸的生产工艺。材料中的反应为放热反应,下列说法正确的是
 2SO3。但该反应速率小,无法投入工业化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造硫酸的生产工艺。材料中的反应为放热反应,下列说法正确的是
2SO3。但该反应速率小,无法投入工业化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造硫酸的生产工艺。材料中的反应为放热反应,下列说法正确的是| A.断开化学键放出能量 |
| B.放热反应都不需要加热 |
| C.及时移走部分产物能加快反应速率 |
| D.该反应的反应物总能量大于生成物的总能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列措施一定能使化学反应速率增大的是
| A.增大反应物的量 | B.升高温度 | C.增大压强 | D.减少反应的量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】利用如图装置制备乙酸乙酯粗产品,再经除杂、干燥、蒸馏收集74~80℃的馏分,获得较高纯度乙酸乙酯。分馏柱可以分离沸点差异较小的组分。相关物质及组成共沸体系的沸点如下。

下列说法错误的是

| 物质 | 沸点/℃ | 共沸体系 | 沸点/℃ |
| 水 | 100.0 | 乙醇-水 | 78.2 |
| 乙醇 | 78.5 | 乙醇-乙酸乙酯 | 72.0 |
| 乙酸 | 117.9 | 乙酸乙酯-水 | 70.4 |
| 乙酸乙酯 | 77.0 | 乙醇-水-乙酸乙酯 | 70.2 |
| A.选择合适长度的分馏柱可减少乙醇损失 |
| B.原料中水的作用是为了形成含水共沸体系利于乙酸乙酯蒸出 |
| C.反应温度控制在120℃左右,可减少副反应发生 |
| D.粗产品除杂后直接蒸馏将导致收集到的产物质量偏大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】丙酸乙酯(CH3CH2COOCH2CH3)是常用的食品加香剂,常温下呈液态,不溶于水,实验室中以丙酸和过量乙醇在无水氧化钙作用下制备丙酸乙酯的实验装置如图所示(加热和夹持装置略去)。下列说法错误的是


| A.盛放丙酸的仪器名称为恒压滴液漏斗 |
| B.应从球形冷凝管的下口向冷凝管中通入冷却水 |
| C.加入无水氯化钙和过量乙醇均可提高丙酸的平衡转化率 |
| D.反应后的混合液经过滤、饱和Na2CO3溶液洗涤、结晶,得到丙酸乙酯 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】根据元素周期表和元素周期律,判断下列叙述不正确的是( )
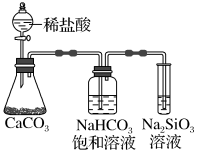

| A.气态氢化物的稳定性:H2O>NH3 |
| B.钠元素的金属性比镁元素的强 |
| C.如图所示实验不能证明元素的非金属性:Cl>C>Si |
| D.铊(81Tl)与Al同主族,其单质既能与盐酸反应又能与氢氧化钠溶液反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】用下图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是
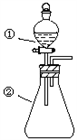

| 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 草酸溶液 | 酸性高锰酸钾溶液 | 溶液逐渐褪色 |
| B | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
| C | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
| D | 氯化铝溶液 | 浓氢氧化钠溶液 | 立即产生大量白色沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验“操作和现象”与“结论"对应且都正确的是
| 操作和现象 | 结论 | |
| A | 向紫色石蕊溶液中通入SO2至过量,溶液先变红后褪色。 | SO2的水溶液具有酸性和漂白性 |
| B | 向含有淀粉的KI溶液中滴加FeCl3溶液,溶液变蓝。 | Fe3+可以和淀粉发生显色反应 |
| C | 用pH传感器测得形同温度下Na2SiO3溶液的pH值大于Na2CO3溶液的pH值。 | 证明C元素的非金属性强于Si元素 |
| D | 取少量Na2O2于试管中,加适量水。待固体完全溶解后,滴加几滴紫色石蕊溶液,溶液先变蓝色后褪色。再加入适量MnO2粉末,产生能使带火星木条复燃的气体。 | Na2O2与水反应过程中有H2O2生成,且H2O2具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次





 漂白性
漂白性

