1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下,它是无色液体,密度为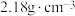 ,沸点为131.4℃,熔点为9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。实验室用乙醇和必要的无机试剂制取1,2-二溴乙烷的装置如图所示:
,沸点为131.4℃,熔点为9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。实验室用乙醇和必要的无机试剂制取1,2-二溴乙烷的装置如图所示:

回答下列问题:
(1)向装置A的烧瓶中装入乙醇和浓硫酸的混合液后还需加入___________ ,烧瓶内发生反应的化学方程式为___________ 。
(2)装置B的作用是___________ ;实验进行时若装置D中长导管发生堵塞,此时装置B中的现象为___________ 。
(3)装置C中盛有10%的NaOH溶液,其作用是___________ 。
(4)开始反应时需向装置D中的烧杯里加入冰水,这是为了___________ ;烧杯中试管内发生反应的化学方程式是___________ 。
(5)装置D中试管内观察到的主要现象是___________ 。
(6)进行此实验时装置D中试管内的橡皮塞最好用锡箔包住,用橡皮管连接的两玻璃管口要相互紧靠,这是因为___________ 。
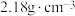 ,沸点为131.4℃,熔点为9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。实验室用乙醇和必要的无机试剂制取1,2-二溴乙烷的装置如图所示:
,沸点为131.4℃,熔点为9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。实验室用乙醇和必要的无机试剂制取1,2-二溴乙烷的装置如图所示:
回答下列问题:
(1)向装置A的烧瓶中装入乙醇和浓硫酸的混合液后还需加入
(2)装置B的作用是
(3)装置C中盛有10%的NaOH溶液,其作用是
(4)开始反应时需向装置D中的烧杯里加入冰水,这是为了
(5)装置D中试管内观察到的主要现象是
(6)进行此实验时装置D中试管内的橡皮塞最好用锡箔包住,用橡皮管连接的两玻璃管口要相互紧靠,这是因为
更新时间:2022-06-30 09:06:50
|
相似题推荐
【推荐1】实验室制取乙烯的装置如下图所示,请根据图示回答下列问题:
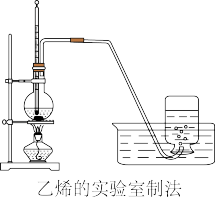
(1)实验室制乙烯的化学方程式为_____ 在这个反应中,浓硫酸的作用是_____________________ 和______________ 。
(2)某化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫, 老师启发他们并由他们自己设计了下列实验图以确认上述混合气体中有 C2H4 和 SO2。
回答下列问题:
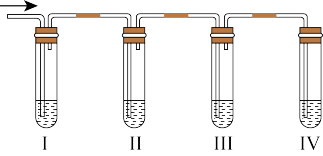
品红溶液 NaOH 溶液 品红溶液酸性KMnO4溶液
①能说明 SO2气体存在的现象是____________________ 。
②确定含有乙烯的现象是_____________

(1)实验室制乙烯的化学方程式为
(2)某化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫, 老师启发他们并由他们自己设计了下列实验图以确认上述混合气体中有 C2H4 和 SO2。
回答下列问题:

品红溶液 NaOH 溶液 品红溶液酸性KMnO4溶液
①能说明 SO2气体存在的现象是
②确定含有乙烯的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】在实验室制取乙烯时,其反应为CH3CH2OH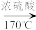 CH2=CH2↑+H2O,该实验常因温度控制不当而发生副反应生成SO2、CO2、水蒸气等。实验室设计如图实验装置以验证上述反应生成的混合气体中含己烯、SO2和水蒸气。
CH2=CH2↑+H2O,该实验常因温度控制不当而发生副反应生成SO2、CO2、水蒸气等。实验室设计如图实验装置以验证上述反应生成的混合气体中含己烯、SO2和水蒸气。
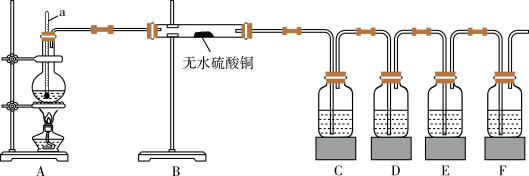
限用试剂(试剂均足量):乙醇、浓硫酸、品红溶液、氢氧化钠溶液、酸性高锰酸钾溶液、溴水。
(1)仪器a的名称为_________ 。
(2)请根据实验的要求完成下列填空:
①D中试剂的作用为_________ 。
②E中的试剂为_________ 。
③F中的试剂为_________ ,可能的实验现象为_________ 。
(3)简述装置B置于装置A、C之间的理由:_________ 。
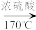 CH2=CH2↑+H2O,该实验常因温度控制不当而发生副反应生成SO2、CO2、水蒸气等。实验室设计如图实验装置以验证上述反应生成的混合气体中含己烯、SO2和水蒸气。
CH2=CH2↑+H2O,该实验常因温度控制不当而发生副反应生成SO2、CO2、水蒸气等。实验室设计如图实验装置以验证上述反应生成的混合气体中含己烯、SO2和水蒸气。
限用试剂(试剂均足量):乙醇、浓硫酸、品红溶液、氢氧化钠溶液、酸性高锰酸钾溶液、溴水。
(1)仪器a的名称为
(2)请根据实验的要求完成下列填空:
①D中试剂的作用为
②E中的试剂为
③F中的试剂为
(3)简述装置B置于装置A、C之间的理由:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】设计实验,对下列物质所含官能团进行检验。
(1)为了证明溴乙烷中存在溴原子,某同学设计如下实验:
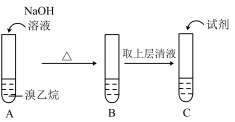
① 将试管C中加入的试剂及相应的实验现象补充完整:_______ 。
② 溴乙烷在NaOH水溶液中反应的化学方程式是______ 。
(2)用化学方法检验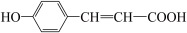 含有的官能团。
含有的官能团。
① 完成下表:
② 不能用溴水检验是否含有碳碳双键,简述理由:_______ 。
(1)为了证明溴乙烷中存在溴原子,某同学设计如下实验:

① 将试管C中加入的试剂及相应的实验现象补充完整:
② 溴乙烷在NaOH水溶液中反应的化学方程式是
(2)用化学方法检验
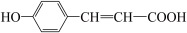 含有的官能团。
含有的官能团。① 完成下表:
| 官能团 | 检验试剂 | 实验现象 | 化学方程式 |
| —OH | FeCl3溶液 | 溶液呈紫色 |  |
| —COOH | | 有无色气泡产生 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】苯甲酸广泛应用于制药和化工行业.某化学小组用甲苯作主要原料制备苯甲酸,反应过程如下:

甲苯、苯甲酸钾、苯甲酸的部分物理性质见下表:
(1)将步骤①得到混合物加少量水,分离有机相和水相,有机相在______________ (填“上”或“下”)层;实验操作的名称是______________ 。
(2)步骤②用浓盐酸酸化的目的是______________ 。
(3)减压过滤装置所包含的仪器除减压系统外,还有______________ (填仪器名称).
(4)已知温度越低苯甲酸的溶解度越小,但为了得到更多的苯甲酸晶体,重结晶时并非温度越低越好,理由是______________ 。
(5)重结晶时需要趁热过滤,目的是______________ 。

甲苯、苯甲酸钾、苯甲酸的部分物理性质见下表:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 在水中溶解性 |
| 甲苯 | -95 | 110.6 | 0.8669 | 难溶 |
| 苯甲酸钾 | 121.5~123.5 | 易溶 | ||
| 苯甲酸 | 122.4 | 248 | 1.2659 | 微溶 |
(2)步骤②用浓盐酸酸化的目的是
(3)减压过滤装置所包含的仪器除减压系统外,还有
(4)已知温度越低苯甲酸的溶解度越小,但为了得到更多的苯甲酸晶体,重结晶时并非温度越低越好,理由是
(5)重结晶时需要趁热过滤,目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】苯甲酸乙酯(C9H10O2)是一种重要的有机合成中间体,有香味,广泛用于配制香水、香精和食品工业中。某兴趣小组设计制备苯甲酸乙酯的实验步骤如下:
①在250mL带有分水器的烧瓶中加入24.4g苯甲酸、50mL苯、18.4g乙醇和0.8g硫酸,按如图所示装好仪器,控制温度在65~70℃加热回流至分水器无水分出来为止。
②将烧瓶内反应液倒入盛有适量水的烧杯中,加入Na2CO3至溶液呈中性。分液后水层用乙醚萃取,然后合并至有机层,加入少量无水MgSO4固体,静置,过滤。
③对滤液进行蒸馏,低温蒸出乙醚和苯后,继续升温到一定温度后,即得约25.7mL产品。
实验原理、装置和有关数据如下:

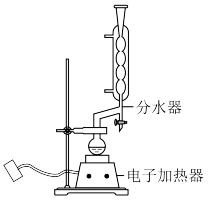
∗苯甲酸在100℃会迅速升华。
回答下列问题:
(1)在该实验中,分离得到苯甲酸乙酯操作时必需的主要仪器是___ (填入字母)。
A.分液漏斗 B.漏斗 C.蒸馏烧瓶 D.直形冷凝管 E.蒸发皿 F.温度计
(2)步骤①中使用分水器不断分离水的目的是___ 。
(3)步骤③中蒸馏操作温度计的水银球位置应处在___ ,温度计的最大量程应为___ 。
A.100℃ B.150℃ C.200℃ D.250℃
(4)本实验中加入过量乙醇的目的是___ 。
(5)步骤②加入Na2CO3的作用是___ 。
(6)计算本实验的产率为___ 。
(7)步骤②若加入Na2CO3的量不足,最后蒸馏产品时蒸馏烧瓶瓶口内壁上有晶体附着,产生该现象的原因___ 。
①在250mL带有分水器的烧瓶中加入24.4g苯甲酸、50mL苯、18.4g乙醇和0.8g硫酸,按如图所示装好仪器,控制温度在65~70℃加热回流至分水器无水分出来为止。
②将烧瓶内反应液倒入盛有适量水的烧杯中,加入Na2CO3至溶液呈中性。分液后水层用乙醚萃取,然后合并至有机层,加入少量无水MgSO4固体,静置,过滤。
③对滤液进行蒸馏,低温蒸出乙醚和苯后,继续升温到一定温度后,即得约25.7mL产品。
实验原理、装置和有关数据如下:


| 名称 | 相对分子质量 | 颜色,状态 | 沸点(℃) | 密度(g/cm3) |
| 苯甲酸* | 122 | 无色片状晶体 | 249 | 1.2659 |
| 苯甲酸乙酯 | 150 | 无色澄清液体 | 212.6 | 1.05 |
| 乙醇 | 46 | 无色澄清液体 | 78.3 | 0.7893 |
| 苯 | 78 | 无色澄清液体 | 80.1 | 0.88 |
回答下列问题:
(1)在该实验中,分离得到苯甲酸乙酯操作时必需的主要仪器是
A.分液漏斗 B.漏斗 C.蒸馏烧瓶 D.直形冷凝管 E.蒸发皿 F.温度计
(2)步骤①中使用分水器不断分离水的目的是
(3)步骤③中蒸馏操作温度计的水银球位置应处在
A.100℃ B.150℃ C.200℃ D.250℃
(4)本实验中加入过量乙醇的目的是
(5)步骤②加入Na2CO3的作用是
(6)计算本实验的产率为
(7)步骤②若加入Na2CO3的量不足,最后蒸馏产品时蒸馏烧瓶瓶口内壁上有晶体附着,产生该现象的原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
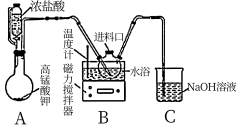
【推荐3】二氯异氰尿酸钠(简称DCCNa)是一种高效、安全的消毒剂,常温下性质稳定,受热易分解,难溶于冰水。实验室通过以下原理和装置(夹持仪器已略去)可以制取DCCNa。
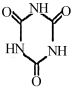 +2NaClO(浓)
+2NaClO(浓) 
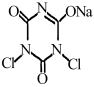 +2NaOH+H2O
+2NaOH+H2O
实验步骤如下:
Ⅰ.制备高浓度NaClO溶液
从进料口加入10mL 30% NaOH溶液,在10℃左右水浴,搅拌条件下通入Cl2至溶液pH约为8;再加入10mL 40% NaOH溶液,继续通入Cl2至溶液pH约为8。
(1)用烧碱固体配制40%的NaOH溶液,下列仪器中不需要的是___________ (写名称)。

(2)“步骤I”测定溶液pH的方法是___________ 。
(3)水浴降温可以减少NaClO3副产物的生成,该副反应的离子方程式为___________ 。
(4)通过改进实验装置,可以提高B中NaOH的利用率,可行的方法是___________ (写一种)。
Ⅱ.制备二氯异氰尿酸钠
待步骤Ⅰ结束后,从进料口加入氰尿酸,在搅拌状态下继续通入Cl2,在10℃左右下反应30min,此时三颈瓶内有DCCNa白色晶体析出,停止反应。
(5)为了使晶体充分析出并分离,需要的操作为___________ 、___________ 洗涤、干燥。
(6)继续通入Cl2的目的是___________ 。
Ⅲ.二氯异氰尿酸钠有效氯含量测定
称取0.1000g样品,用100mL蒸馏水于碘量瓶中溶解后,依次加入20mL 0.3mol·L-1醋酸溶液和过量的KI溶液。用0.1000 mol·L-1 Na2S2O3溶液滴定至溶液呈浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗Na2S2O3溶液16.00mL。
(已知: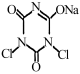
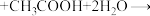
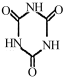
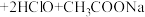 ,
, )
)
(7)滴定终点的现象为___________ 。
(8)样品有效氯=___________ 。( )
)

 +2NaClO(浓)
+2NaClO(浓) 
 +2NaOH+H2O
+2NaOH+H2O实验步骤如下:
Ⅰ.制备高浓度NaClO溶液
从进料口加入10mL 30% NaOH溶液,在10℃左右水浴,搅拌条件下通入Cl2至溶液pH约为8;再加入10mL 40% NaOH溶液,继续通入Cl2至溶液pH约为8。
(1)用烧碱固体配制40%的NaOH溶液,下列仪器中不需要的是




(2)“步骤I”测定溶液pH的方法是
(3)水浴降温可以减少NaClO3副产物的生成,该副反应的离子方程式为
(4)通过改进实验装置,可以提高B中NaOH的利用率,可行的方法是
Ⅱ.制备二氯异氰尿酸钠
待步骤Ⅰ结束后,从进料口加入氰尿酸,在搅拌状态下继续通入Cl2,在10℃左右下反应30min,此时三颈瓶内有DCCNa白色晶体析出,停止反应。
(5)为了使晶体充分析出并分离,需要的操作为
(6)继续通入Cl2的目的是
Ⅲ.二氯异氰尿酸钠有效氯含量测定
称取0.1000g样品,用100mL蒸馏水于碘量瓶中溶解后,依次加入20mL 0.3mol·L-1醋酸溶液和过量的KI溶液。用0.1000 mol·L-1 Na2S2O3溶液滴定至溶液呈浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗Na2S2O3溶液16.00mL。
(已知:

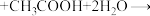

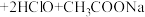 ,
, )
)(7)滴定终点的现象为
(8)样品有效氯=
 )
)
您最近一年使用:0次



