甲、乙两位同学探究外界条件对化学反应速率的影响。
【实验原理】反应:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,反应过程中溶液出现乳白色浑浊和有刺激性气味的气体。
【实验用品】0.1mol/LNa2S2O3溶液、0.1mol/LH2SO4溶液、蒸馏水。
试管、烧杯、量筒、胶头滴管等。
实验一:甲同学利用如图装置测定化学反应速率。_______ 。除如图所示的实验用品外,还需要的实验仪器是_______ 。
(2)若在2min时收集到224mL(已折算成标准状况)气体,可计算出在2min内的反应速率v(H+)=0.02mol/(L·min),而该速率值比实际值偏小,其原因是_______ 。
实验二:乙同学得到各组实验数据如下表。
(3)实验Ⅰ、Ⅱ探究_______ 对化学反应速率的影响。
①a=_______ 。
②V=_______ ,加入VmL水的目的是_______ 。
(4)实验Ⅱ、Ⅲ探究温度对化学反应速率的影响。实验表明,实验Ⅲ的反应速率最快,支持这一结论的实验现象是_______ 。
【实验原理】反应:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,反应过程中溶液出现乳白色浑浊和有刺激性气味的气体。
【实验用品】0.1mol/LNa2S2O3溶液、0.1mol/LH2SO4溶液、蒸馏水。
试管、烧杯、量筒、胶头滴管等。
实验一:甲同学利用如图装置测定化学反应速率。
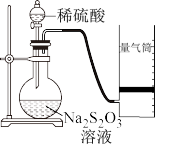
(2)若在2min时收集到224mL(已折算成标准状况)气体,可计算出在2min内的反应速率v(H+)=0.02mol/(L·min),而该速率值比实际值偏小,其原因是
实验二:乙同学得到各组实验数据如下表。
| 实验编号 | Na2S2O3溶液 | H2SO4溶液 | 蒸馏水 | ||||
| 浓度/ (mol/L) | 体积/mL | 浓度/ (mol/L) | 体积/mL | 体积/mL | 温度/℃ | ||
| Ⅰ | 0.1 | 1.5 | 0.1 | 1.5 | V | 20 | |
| Ⅱ | 0.1 | 2.5 | 0.1 | 1.5 | 8 | a | |
| Ⅲ | 0.1 | 2.5 | 0.1 | 1.5 | 8 | 30 | |
①a=
②V=
(4)实验Ⅱ、Ⅲ探究温度对化学反应速率的影响。实验表明,实验Ⅲ的反应速率最快,支持这一结论的实验现象是
21-22高一下·北京东城·期末 查看更多[5]
北京市东城区2021-2022学年高一下学期期末考试化学试题河北省元氏县第四中学2022-2023学年高二上学期开学考试化学试卷北京市第一七一中学2022-2023学年高一下学期期中考试化学试题(已下线)重难点02 速率与平衡综合题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)(已下线)专题03 化学反应的速率与限度-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)
更新时间:2022-07-12 19:57:05
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】某温度时,在2L恒容密闭容器中发生A、B两种气体间的转化反应,A、B物质的量随时间变化的曲线如下图所示,请分析图中数据,回答下列问题。

(1)由图可知,M点的坐标为_______ ,该反应的化学方程式为_______ 。
(2)反应从开始至4min时,用B的浓度变化来表示的反应速率为_______ ,反应达平衡时,A的转化率为_______ 。
(3)下列能作为该反应达到平衡状态标志的是_______(填字母)。
(4)比较M、N两点该反应的正反应速率的相对大小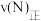
_______ 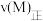 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。

(1)由图可知,M点的坐标为
(2)反应从开始至4min时,用B的浓度变化来表示的反应速率为
(3)下列能作为该反应达到平衡状态标志的是_______(填字母)。
| A.容器中B的体积分数不变 | B.体系的压强不再变化 |
| C.每消耗1molA的同时生成0.5molB | D.体系内混合气体的密度不再变化 |
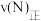
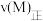 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某小组学生设计了如下定性探究影响化学反应速率因素的实验。
依据可选试剂: 溶液、
溶液、 溶液、蒸馏水、
溶液、蒸馏水、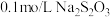 溶液、
溶液、
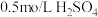 溶液、
溶液、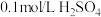 溶液
溶液
请按要求回答下列问题。
(1)小组确定实验探究的反应原理及其对应的预期现象(填充空白)
(2)学生甲选择原理i,探究催化剂对该反应速率的因素,必选试剂除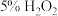 溶液外,还应选
溶液外,还应选_______ 。
(3)学生乙设计下图所示对比实验,探究硫酸浓度对反应ii速率的影响
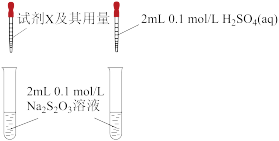
试剂X及其用量:_______ 。
(4)学生丙设计对比实验,探究影响反应ii速率的因素,数据如下表所示:
①对比实验Ⅰ、Ⅱ,为探究_______ 对该反应速率的影响。
②a=_______ ℃
③V=_______ mL,加入V mL水的目的是_______ 。
④对比上述实验数据,推测反应速率最快的是_______ (填实验编号)。
依据可选试剂:
 溶液、
溶液、 溶液、蒸馏水、
溶液、蒸馏水、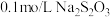 溶液、
溶液、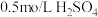 溶液、
溶液、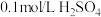 溶液
溶液请按要求回答下列问题。
(1)小组确定实验探究的反应原理及其对应的预期现象(填充空白)
| 实验 | 化学方程式 | 预期观察的现象 |
| 原理i | 产生气泡快慢 | |
| 原理ii | 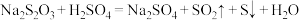 |
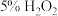 溶液外,还应选
溶液外,还应选(3)学生乙设计下图所示对比实验,探究硫酸浓度对反应ii速率的影响

试剂X及其用量:
(4)学生丙设计对比实验,探究影响反应ii速率的因素,数据如下表所示:
| 实验编号 |  溶液 溶液 |  溶液 溶液 | 蒸馏水 | |||
| 浓度/(mol/L) | 体积/mL | 浓度(mol/L) | 体积/mL | 体积/mL | 温度/℃ | |
| Ⅰ | 0.1 | 1 | 0.5 | 1 | V | 30 |
| Ⅱ | 0.1 | 2 | 0.5 | 1 | 7 | a |
| Ⅲ | 0.1 | 2 | 0.5 | 1 | 7 | 40 |
②a=
③V=
④对比上述实验数据,推测反应速率最快的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据在298K时,实验测得溶液中的反应H2O2+2HI=2H2O+I2在不同浓度时的速率表,请与同学们交流研讨:
(1)补充表中的相应数据:
(2)找出化学反应速率与H2O2浓度、HI浓度之间的关系,并尝试写出相应的数学表达式____ 。
(1)补充表中的相应数据:
| 试验编号 | 1 | 2 | 3 | 4 | 5 |
| c(HI)/(mol/L) | 0.100 | 0.200 | 0.300 | 0.100 | 0.100 |
| c(H2O2)/(mol/L) | 0.100 | 0.100 | 0.100 | 0.200 | 0.300 |
| v/(mol·L-1·s-1) |
(2)找出化学反应速率与H2O2浓度、HI浓度之间的关系,并尝试写出相应的数学表达式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.实验室利用下列方案探究影响化学反应速率的因素。请回答相关问题:
(1)实验时,分别量取 溶液和酸性
溶液和酸性 溶液,迅速混合并开始计时,通过测定
溶液,迅速混合并开始计时,通过测定_______ 来判断反应的快慢。
(2)实验①、②、③所加 溶液均要过量,理由是
溶液均要过量,理由是_______ 。
(3)实验①和实验②是探究_______ 对化学反应速率的影响,实验②和③是探究_______ 对化学反应速率的影响。
(4)实验①和②起初反应均很慢,过了一会儿速率突然增大,可能原因是_______ 。
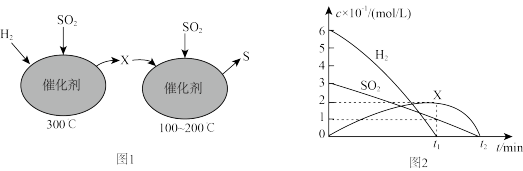
II.在恒容密闭容器中,用H2还原SO2,生成S的反应分两步完成(如图1所示),该过程中相关物质的物质的量浓度随时间的变化关系如图2所示,请分析并回答如下问题:
(5)分析可知X为_______ (填化学式)。
(6) 时间段的温度为
时间段的温度为_______ 。
(7) 时间段用SO2表示的化学反应速率为
时间段用SO2表示的化学反应速率为_______ 。
| 编号 | 温度/℃ |  溶液 溶液 | 酸性 溶液 溶液 | ||
浓度/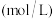 | 体积/ | 浓度/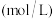 | 体积/ | ||
| ① | 25 | 0.10 | 2.0 | 0.010 | 4.0 |
| ② | 25 | 0.20 | 2.0 | 0.010 | 4.0 |
| ③ | 50 | 0.20 | 2.0 | 0.010 | 4.0 |
 溶液和酸性
溶液和酸性 溶液,迅速混合并开始计时,通过测定
溶液,迅速混合并开始计时,通过测定(2)实验①、②、③所加
 溶液均要过量,理由是
溶液均要过量,理由是(3)实验①和实验②是探究
(4)实验①和②起初反应均很慢,过了一会儿速率突然增大,可能原因是
II.在恒容密闭容器中,用H2还原SO2,生成S的反应分两步完成(如图1所示),该过程中相关物质的物质的量浓度随时间的变化关系如图2所示,请分析并回答如下问题:

(5)分析可知X为
(6)
 时间段的温度为
时间段的温度为(7)
 时间段用SO2表示的化学反应速率为
时间段用SO2表示的化学反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在密闭容器中的可逆反应CO(g)+NO2(g)  CO2(g)+NO(g) △H<0达到平衡后:
CO2(g)+NO(g) △H<0达到平衡后:
(1)扩大容器体积,平衡__________________ 移动(填“正向”“逆向”或“不”,下同),C(NO2)将 ______________ (填“变大”“变小”或“不变”),反应混合物的颜色 _______________ (填“变深”或“变浅”)
(2)升高温度,正反应速率__________________ (填“变大”“变小”或“不变”,下同),平衡常数K ____________________
(3)加入催化剂,NO的物质的量____________________
 CO2(g)+NO(g) △H<0达到平衡后:
CO2(g)+NO(g) △H<0达到平衡后:(1)扩大容器体积,平衡
(2)升高温度,正反应速率
(3)加入催化剂,NO的物质的量
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:

(1)写出该反应的化学方程式____ 。
(2)从开始到10s用Z表示该反应的速率为____ 。
(3)下列叙述中能说明上述反应达到平衡状态的是____ 。
(4)为加快该反应的反应速率,可采取的措施是____ 。
(5)某兴趣小组为研究原电池原理,设计如图装置。
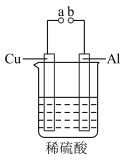
a和b用导线连接,Cu极为原电池____ 极(填“正”或“负”),电极反应式是:____ ;Al极发生____ (填“氧化”或“还原”)反应,溶液中SO 移向
移向____ (填“Cu”或“Al”极)。

(1)写出该反应的化学方程式
(2)从开始到10s用Z表示该反应的速率为
(3)下列叙述中能说明上述反应达到平衡状态的是
| A.X、Y、Z的反应速率之比为1:1:2 |
| B.在混合气体中X的体积分数保持不变 |
| C.混合气体的平均摩尔质量不随时间的变化而变化 |
| D.混合气体的压强不随时间的变化而变化 |
| A.适当升高温度 | B.恒容时充入Ne使压强增大 |
| C.增大容器的体积 | D.选择高效催化剂 |

a和b用导线连接,Cu极为原电池
 移向
移向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.某实验小组对H2O2的分解做了如下探究。下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同的粉末状和块状的MnO2分别加入盛有15 ml 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
(1)写出上述实验中发生反应的化学方程式:______ 。
(2)实验结果表明,催化剂的催化效果与_____ 有关。
(3)某同学在10 mL H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的反应速率最慢的是_____ 。
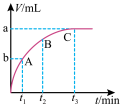
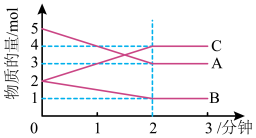
Ⅱ.某反应在体积为5L的恒容密闭容器中进行, 在0-3分钟内各物质的量的变化情况如图所示(A,B,C均为气体,且A气体有颜色)。
(4)该反应的的化学方程式为__________ 。
(5)反应开始至2分钟时,B的平均反应速率为____ 。
(6)能说明该反应已达到平衡状态的是____ 。
a.v(A)= 2v(B) b.容器内各物质的物质的量相等
c.v逆(A)=v正(C) d.容器内气体的颜色保持不变
(7)由图求得平衡时A的体积分数______ 。
| MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5min |
| 块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30min |
(1)写出上述实验中发生反应的化学方程式:
(2)实验结果表明,催化剂的催化效果与
(3)某同学在10 mL H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如图所示,则A、B、C三点所表示的反应速率最慢的是

Ⅱ.某反应在体积为5L的恒容密闭容器中进行, 在0-3分钟内各物质的量的变化情况如图所示(A,B,C均为气体,且A气体有颜色)。
(4)该反应的的化学方程式为
(5)反应开始至2分钟时,B的平均反应速率为
(6)能说明该反应已达到平衡状态的是
a.v(A)= 2v(B) b.容器内各物质的物质的量相等
c.v逆(A)=v正(C) d.容器内气体的颜色保持不变
(7)由图求得平衡时A的体积分数

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】硝酸铜晶体[Cu(NO3)2·6H2O],是一种重要的化工原料,常用于农药、镀铜、搪瓷等工业。以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备硝酸铜晶体的某工艺如图所示。回答下列问题:
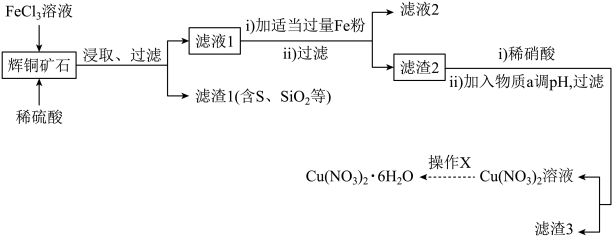
“浸取”时,为了提高浸取率可采取的措施有___________ (任写一点)

“浸取”时,为了提高浸取率可采取的措施有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某化学小组利用硫代硫酸钠进行了相关的实验。
Ⅰ.已知:Na2S2O3+H2 SO4 Na2SO4+SO2↑+S↓+H2O,某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
(1)该实验①、②可探究温度对反应速率的影响,因此V1=V2=____ ,V3=___ ;
(2)若V4=10.0,V5=6.0,则实验①、③可探究_____ 对反应速率的影响。
Ⅱ.利用反应:I2+2Na2S2O3 Na2S4O6+2NaI可定量测定硫代硫酸钠(Mr=158)的纯度,现在称取wg硫代硫酸钠固体样品,配成250mL的溶液,取25.00mL置于锥形瓶中,加入指示剂,用amol/L的碘水滴定,消耗碘水b mL,则:
(3)滴定时,将碘水注入___ (填“酸式”或“碱式”)滴定管中,滴定应选择的指示剂是____ ,滴定终点的现象为________ 。
(4)对于该滴定实验的有关操作或误差分析正确的是____ 。
a.滴定前,要用对应装入的溶液润洗锥形瓶和滴定管
b.滴定过程中,标准液滴到锥形瓶外,会使所测得的结果偏大
c.滴定开始时滴定管尖嘴有气泡,滴定结束后气泡消失,测得纯度将偏小
d.滴定前仰视读数而滴定结束时平视读数,则所测得的纯度将会偏小
(5)样品中硫代硫酸钠纯度的表达式为____ 。
Ⅰ.已知:Na2S2O3+H2 SO4 Na2SO4+SO2↑+S↓+H2O,某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
| 实验序号 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
| V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
| ① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
| ② | 40 | V1 | 0.10 | V2 | 0.50 | V3 |
| ③ | 20 | V4 | 0.10 | 4.0 | 0.50 | V5 |
(1)该实验①、②可探究温度对反应速率的影响,因此V1=V2=
(2)若V4=10.0,V5=6.0,则实验①、③可探究
Ⅱ.利用反应:I2+2Na2S2O3 Na2S4O6+2NaI可定量测定硫代硫酸钠(Mr=158)的纯度,现在称取wg硫代硫酸钠固体样品,配成250mL的溶液,取25.00mL置于锥形瓶中,加入指示剂,用amol/L的碘水滴定,消耗碘水b mL,则:
(3)滴定时,将碘水注入
(4)对于该滴定实验的有关操作或误差分析正确的是
a.滴定前,要用对应装入的溶液润洗锥形瓶和滴定管
b.滴定过程中,标准液滴到锥形瓶外,会使所测得的结果偏大
c.滴定开始时滴定管尖嘴有气泡,滴定结束后气泡消失,测得纯度将偏小
d.滴定前仰视读数而滴定结束时平视读数,则所测得的纯度将会偏小
(5)样品中硫代硫酸钠纯度的表达式为
您最近一年使用:0次



