18. 甲、乙两位同学探究外界条件对化学反应速率的影响。
【实验原理】反应:Na
2S
2O
3+H
2SO
4=Na
2SO
4+SO
2↑+S↓+H
2O,反应过程中溶液出现乳白色浑浊和有刺激性气味的气体。
【实验用品】0.1mol/LNa
2S
2O
3溶液、0.1mol/LH
2SO
4溶液、蒸馏水。
试管、烧杯、量筒、胶头滴管等。
实验一:甲同学利用如图装置测定化学反应速率。
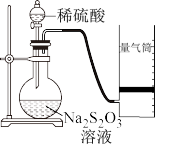
(1)为保证实验的准确性和可靠性,利用该装置进行实验前应先进行的操作是
_______。除如图所示的实验用品外,还需要的实验仪器是
_______。
(2)若在2min时收集到224mL(已折算成标准状况)气体,可计算出在2min内的反应速率v(H
+)=0.02mol/(L·min),而该速率值比实际值偏小,其原因是
_______。
实验二:乙同学得到各组实验数据如下表。
| 实验编号 | Na2S2O3溶液 | H2SO4溶液 | 蒸馏水 | | |
浓度/
(mol/L) | 体积/mL | 浓度/
(mol/L) | 体积/mL | 体积/mL | 温度/℃ |
| Ⅰ | 0.1 | 1.5 | 0.1 | 1.5 | V | 20 |
| Ⅱ | 0.1 | 2.5 | 0.1 | 1.5 | 8 | a |
| Ⅲ | 0.1 | 2.5 | 0.1 | 1.5 | 8 | 30 |
(3)实验Ⅰ、Ⅱ探究
_______对化学反应速率的影响。
①a=
_______。
②V=
_______,加入VmL水的目的是
_______。
(4)实验Ⅱ、Ⅲ探究温度对化学反应速率的影响。实验表明,实验Ⅲ的反应速率最快,支持这一结论的实验现象是
_______。