贵州省平塘民族中学2021-2022学年高二上学期第一次月考化学试题
贵州
高二
阶段练习
2021-10-31
142次
整体难度:
适中
考查范围:
化学反应原理、有机化学基础、化学与STSE、认识化学科学、物质结构与性质、常见无机物及其应用、化学实验基础
贵州省平塘民族中学2021-2022学年高二上学期第一次月考化学试题
贵州
高二
阶段练习
2021-10-31
142次
整体难度:
适中
考查范围:
化学反应原理、有机化学基础、化学与STSE、认识化学科学、物质结构与性质、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
单选题
|
较易(0.85)
名校
解题方法
1. 化学与人类生产、生活、社会可持续发展密切相关。下列说法正确的是
| A.煤、石油、天然气都是可再生能源 |
| B.气象环境报告中的”PM2.5”是对一种新分子的描述 |
| C.由于 Al 的活泼性强,故工业上采用电解熔融 AlCl3的方法生产 Al |
| D.“一带一路”是“丝绸之路经济带”和“21世纪海上丝绸之路”的简称。丝绸的主要成分是蛋白质,属于高分子化合物 |
您最近一年使用:0次
2021-02-01更新
|
139次组卷
|
4卷引用:广西河池市2020-2021学年高二上学期期末教学质量检测化学试题
单选题
|
适中(0.65)
名校
解题方法
2. 下列化学用语正确的是
| A.HClO 的结构式为 H—O—Cl |
B.核数 中质子数为116,中子数为 293 中质子数为116,中子数为 293 |
C.S2-的离子结构示意图为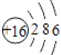 |
| D.Cl2的电子式为 Cl:Cl |
【知识点】 化学用语综合判断
您最近一年使用:0次
2021-02-01更新
|
306次组卷
|
5卷引用:广西河池市2020-2021学年高二上学期期末教学质量检测化学试题
广西河池市2020-2021学年高二上学期期末教学质量检测化学试题(已下线)专题07 物质结构与元素周期律-备战2021届高考化学二轮复习题型专练广西来宾市2020-2021学年高二上学期期末教学质量检测化学试题贵州省平塘民族中学2021-2022学年高二上学期第一次月考化学试题内蒙古自治区阿拉善盟第一中学2021-2022学年高二下学期期末考试化学试题
单选题
|
适中(0.65)
名校
3. 用NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.44 g CO2与 28g CO所含有的原子数均为NA |
| B.24gMg与足量的稀盐酸反应转移的电子数为2NA |
| C.NA个氧分子和 NA个氢分子的质量比为8:1 |
| D.常温常压下,NA个 Cl2分子所占有的体积为22.4L |
您最近一年使用:0次
2021-02-01更新
|
162次组卷
|
4卷引用:广西河池市2020-2021学年高二上学期期末教学质量检测化学试题
单选题
|
适中(0.65)
名校
解题方法
4. 下列表示对应化学反应的离子方程式正确的是
A.向稀硫酸中加入铁粉: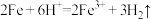 |
B.NO2与水的反应: |
C.冷的氢氧化钠溶液中通入氯气: 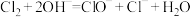 |
D.醋酸溶液与水垢中的CaCO3反应: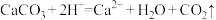 |
【知识点】 离子方程式的正误判断解读
您最近一年使用:0次
2021-02-01更新
|
127次组卷
|
4卷引用:广西河池市2020-2021学年高二上学期期末教学质量检测化学试题
单选题
|
容易(0.94)
名校
解题方法
5. 下列离子在指定的分散系中能大量共存的一组是
A.透明的溶液中: |
B.碱性溶液中: |
C.氢氧化铁胶体: |
D.酸性溶液中: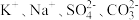 |
【知识点】 离子共存 限定条件下的离子共存解读
您最近一年使用:0次
2021-02-01更新
|
203次组卷
|
6卷引用:广西河池市2020-2021学年高二上学期期末教学质量检测化学试题
单选题
|
适中(0.65)
名校
6. 高铁酸钠(Na2FeO4)易溶于水,是一种新型多功能水处理剂。已知反应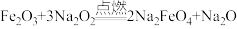 ,下列说法不正确的是
,下列说法不正确的是
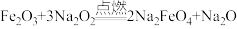 ,下列说法不正确的是
,下列说法不正确的是A. 是还原剂 是还原剂 |
B. 既是氧化产物又是还原产物 既是氧化产物又是还原产物 |
C. 具有强氧化性,能消毒杀菌 具有强氧化性,能消毒杀菌 |
| D.1 mol Na2O2发生反应,有4 mol发生电子转移 |
您最近一年使用:0次
2021-02-01更新
|
146次组卷
|
4卷引用:广西河池市2020-2021学年高二上学期期末教学质量检测化学试题
单选题
|
适中(0.65)
名校
解题方法
7. 已知X、Y、Z、W 四种元素分别是元素周期表中连续三个短周期的元素,且原子序数依次增大。X、W 同主族,Y、Z为同周期的相邻元素。W 原子的质子数等于Y、Z原子最外层电子数之和。Y与X形成的分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。下列说法正确的是
| A.简单离子半径大小:W>Z |
| B.简单气态氢化物的稳定性:Y>Z |
| C.Y 的氧化物对应的水化物为强酸 |
| D.Z、W可组成 W2Z、W2Z2型化合物 |
您最近一年使用:0次
2021-02-01更新
|
123次组卷
|
4卷引用:广西河池市2020-2021学年高二上学期期末教学质量检测化学试题
单选题
|
较易(0.85)
名校
解题方法
8. 如图有a、b 两种物质,下列说法正确的是


A.a 的分子式为  | B.a、b 都属于芳香化合物 |
| C.a、b 均可以发生加成反应 | D.a 中所有原子均在同一平面上 |
您最近一年使用:0次
2021-02-01更新
|
88次组卷
|
5卷引用:广西河池市2020-2021学年高二上学期期末教学质量检测化学试题
单选题
|
容易(0.94)
名校
解题方法
9. 可逆反应 在不同条件下的反应速率如下,其中反应速率最快的是
在不同条件下的反应速率如下,其中反应速率最快的是
 在不同条件下的反应速率如下,其中反应速率最快的是
在不同条件下的反应速率如下,其中反应速率最快的是A.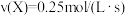 | B.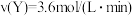 |
C. | D. |
您最近一年使用:0次
2021-10-30更新
|
661次组卷
|
22卷引用:广西河池市2020-2021学年高二上学期期末教学质量检测化学试题
广西河池市2020-2021学年高二上学期期末教学质量检测化学试题广西来宾市2020-2021学年高二上学期期末教学质量检测化学试题河北省衡水市第十四中学2020-2021学年高二下学期摸底考试化学试题辽宁省阜新市第二高级中学2020-2021学年高二下学期第一次月考化学试题湖北省黄冈市麻城市麻城二中2020-2021学年高一下学期期中考试化学试题吉林省“BEST合作体”2020-2021学年高一下学期期中化学试题河南省周口市中英文学校2020-2021学年高一下学期期中考试化学试题四川省雅安中学2020-2021学年高一下学期期中考试化学试题湖北省华中师范大学潜江附属中学2020-2021学年高一下学期5月月考化学试题江苏省宿迁市2020-2021学年高一下学期期末考试化学试题吉林省长春市2020-2021学年高一下学期期末联考化学试题贵州省平塘民族中学2021-2022学年高二上学期第一次月考化学试题江苏省苏州市相城区陆慕高级中学2021-2022学年高二上学期第一次月考化学试题新疆生产建设兵团第二师八一中学2021-2022学年高二上学期期中考试化学试题黑龙江省齐齐哈尔市恒昌中学校2021-2022学年高一下学期期中考试化学试题黑龙江省大庆市大庆中学2021-2022学年高一下学期期中考试化学试题辽宁省营口市普通高中2021-2022学年高一下学期期末化学试题吉林省长春市农安县2021-2022学年高一下学期期末考试化学试题河北省元氏县第四中学2022-2023学年高二上学期开学考试化学试卷河南省南乐县第一高级中学2022-2023学年高二上学期第二次月考化学试题江苏省常熟中学2023-2024学年高二上学期10月阶段性学业水平调研化学试题江苏省苏州市常熟中学2023-2024学年高二上学期10月月考化学试题
单选题
|
容易(0.94)
名校
11. 1mol固态碳和1mol水蒸气反应生成1moLCO和1molH2并吸收131.3kJ热量,则表示该反应的热化学方程式正确的是
A. |
B. |
C. |
D. |
【知识点】 热化学方程式 热化学方程式书写及正误判断解读
您最近一年使用:0次
2021-10-30更新
|
402次组卷
|
6卷引用:贵州省平塘民族中学2021-2022学年高二上学期第一次月考化学试题
单选题
|
适中(0.65)
名校
12. 一定条件下,在2L密闭容器中发生如下反应 ,反应过程中测得的有关数据如下表所示;
,反应过程中测得的有关数据如下表所示;
下列说法不正确的是
 ,反应过程中测得的有关数据如下表所示;
,反应过程中测得的有关数据如下表所示;| 时间/min | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
| n(CH3OH)/mol | 0 | 0.05 | 0.08 | 0.10 | 0.12 | 0.12 | 0.12 |
| A.使用催化剂能够改变反应速率 |
| B.达到 8s 时,反应达到动态平衡 |
| C.用 O2表示 0~4min内该反应的平均反应速率为0.01mol·L-1·min-1 |
| D.生成 CH3OH的平均反应速率:0~2s的平均速率比 2~4s的大 |
您最近一年使用:0次
2021-02-01更新
|
137次组卷
|
4卷引用:广西河池市2020-2021学年高二上学期期末教学质量检测化学试题
单选题
|
较易(0.85)
13. 分别取50mL 0.5mol/L的盐酸溶液与50mL 0.55mol/L的氢氧化钠溶液进行中和热测定实验。下列操作和说法不正确的是


| A.稍过量的氢氧化钠是确保盐酸完全反应 |
| B.向盛装盐酸的烧杯中小心缓慢地加入氢氧化钠溶液 |
| C.仪器A的名称是环形玻璃搅拌棒 |
| D.在实验过程中,把温度计上的酸用水冲洗干净后再测量氢氧化钠溶液的温度 |
【知识点】 中和热的测定与误差分析解读
您最近一年使用:0次
2018-01-27更新
|
278次组卷
|
2卷引用:河北省张家口市2017-2018学年高二上学期期末考试化学试题
单选题
|
适中(0.65)
14. 根据如下能量关系示意图,可知反应2C(s)+O2(g)=2CO(g)的△H为


| A.-110.6 kJ·mol-1 | B.-221.2 kJ·mol-1 | C.-393.5 kJ·mol-1 | D.-676.4 kJ·mol-1 |
您最近一年使用:0次
2020-12-28更新
|
67次组卷
|
2卷引用:河南省开封市五县2020-2021学年高二上学期期中联考化学试题
单选题
|
适中(0.65)
名校
15. 在一定条件下,将X和Y两种物质按不同的比例放入密闭容器中反应,平衡后测得X,Y的转化率与起始时两物质的物质的量之比 的关系如图所示,则X,Y的反应方程式可表示为( )
的关系如图所示,则X,Y的反应方程式可表示为( )

 的关系如图所示,则X,Y的反应方程式可表示为( )
的关系如图所示,则X,Y的反应方程式可表示为( )
A.2X+Y 3Z 3Z | B.3X+2Y 2Z 2Z |
C.X+3Y Z Z | D.3X+Y Z Z |
【知识点】 化学平衡的有关计算
您最近一年使用:0次
2012-06-26更新
|
554次组卷
|
8卷引用:2011-2012学年浙江省台州中学高二下学期期中考试化学试卷
(已下线)2011-2012学年浙江省台州中学高二下学期期中考试化学试卷(已下线)2012-2013学年福建省上杭一中高三第一次诊断测试化学试卷2015-2016学年山东省武城县第二中学高二上学期第一次月考化学试卷甘肃省会宁县第一中学2017-2018学年高二上学期期中考试(理)化学试题湖南省衡阳市26中2017-2018学年高二上学期期中考试化学试题湖南省衡阳二十六中2017-2018学年高二上学期期中考试化学试题青海省西宁市普通高中五校2020-2021学年高二上学期期末联考化学试题贵州省平塘民族中学2021-2022学年高二上学期第一次月考化学试题
单选题
|
较易(0.85)
名校
16. 在一定的条件下,向2 L密闭容器中进行一定量MgSO4和CO的反应:MgSO4(s)+CO(g)⇌MgO(s)+CO2(g)+SO2(g)。反应时间与残留固体的质量关系如图所示。下列说法正确的是


| A.升高温度时,正反应速率增大,逆反应速率减小 |
| B.随着反应的进行,混合气体的平均相对分子质量增大 |
| C.增加硫酸镁的质量时,正反应速率增大 |
| D.在0~10 min内,v(CO)=0.01 mol·L-1·min-1 |
您最近一年使用:0次
2021-09-05更新
|
1115次组卷
|
10卷引用:课时38 化学平衡常规图像-2022年高考化学一轮复习小题多维练(全国通用)
(已下线)课时38 化学平衡常规图像-2022年高考化学一轮复习小题多维练(全国通用)安徽省芜湖市华星学校2021-2022学年高二上学期第一次月考化学试卷黑龙江省鹤岗市第一中学2021-2022学年高二上学期第一次月考化学试题贵州省平塘民族中学2021-2022学年高二上学期第一次月考化学试题2021年广东省高考化学试卷变式题11-21吉林油田高级中学2021-2022学年高二上学期期初考试化学试题云南省丽江市第一高级中学2021-2022学年高二上学期期中考试化学试题(已下线)第20讲 化学反应速率(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)【2023】【高一下】【其他】【杭十一】【高中化学】【刘尼尼收集】(已下线)章末综合评价(七)
二、解答题 添加题型下试题
解答题-工业流程题
|
容易(0.94)
17. 某化学兴趣小组以废铁屑(含有碳、Fe2O3杂质)为原料制备 晶体。具体的流程如下:
晶体。具体的流程如下:

试回答下列问题:
(1)请写出“酸溶”时发生反应的离子方程式: 、
、___________ 。
(2)过滤时,需要用到的玻璃仪器有___________ 。
(3)“氧化”过程中发生反应的化学方程式为___________ ,该反应中氧化剂是___________ ,每消耗22.4LCl2 (标准状况下),转移的电子数为___________ 。
(4)蒸发过程中需要用到玻璃棒,此时玻璃棒的作用是___________ 。
 晶体。具体的流程如下:
晶体。具体的流程如下:
试回答下列问题:
(1)请写出“酸溶”时发生反应的离子方程式:
 、
、(2)过滤时,需要用到的玻璃仪器有
(3)“氧化”过程中发生反应的化学方程式为
(4)蒸发过程中需要用到玻璃棒,此时玻璃棒的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
18. 某学习小组设计实验探究 与铜粉的反应并检验
与铜粉的反应并检验 ,实验装置如图所示(夹持装置略)。已知在溶液中:
,实验装置如图所示(夹持装置略)。已知在溶液中: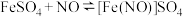 (棕色),该反应可用于检验
(棕色),该反应可用于检验 。
。
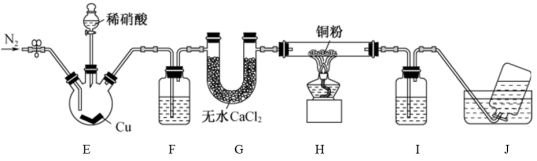
(1)实验开始前,向装置中通入一段时间的 ,目的是
,目的是_______ 。
(2)请写出装置E中反应的离子方程式:_______ 。
(3)装置F中盛放的是水,作用是_______ ;装置Ⅰ中盛放的试剂是_______ ,作用是_______ 。
(4)若观察到装置H中红色粉末变黑色,则NO与Cu发生了反应,同时生成一种单质,请写出该反应的化学方程式:_______ 。
 与铜粉的反应并检验
与铜粉的反应并检验 ,实验装置如图所示(夹持装置略)。已知在溶液中:
,实验装置如图所示(夹持装置略)。已知在溶液中: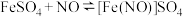 (棕色),该反应可用于检验
(棕色),该反应可用于检验 。
。
(1)实验开始前,向装置中通入一段时间的
 ,目的是
,目的是(2)请写出装置E中反应的离子方程式:
(3)装置F中盛放的是水,作用是
(4)若观察到装置H中红色粉末变黑色,则NO与Cu发生了反应,同时生成一种单质,请写出该反应的化学方程式:
您最近一年使用:0次
2021-03-10更新
|
334次组卷
|
2卷引用:广西来宾市2020-2021学年高二上学期期末教学质量检测化学试题
三、填空题 添加题型下试题
填空题
|
较易(0.85)
名校
19. 红磷和Cl2发生反应生成PCl3或PCl5。反应过程和能量关系如右图所示(图中的 表示生成1mol产物的数据)。
表示生成1mol产物的数据)。

回答下列问题:
(1)1molPCl3所具有的总能量比1molP和1.5molCl2所具有的总能量___________ (填“高”或“低”)___________ kJ。
(2)PCl3和Cl2化合成PCl5的热化学方程式是___________ 。
(3)P和Cl2反应生成1molPCl5的 =
=___________ 。
(4)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是___________ 。
(5)红磷的同素异形体白磷在氧气中燃烧有如下转化关系。
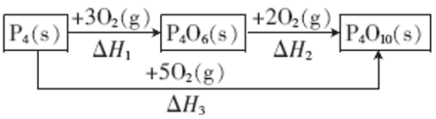
其中 =
=___________ (用含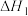 和
和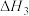 的代数式表示)。
的代数式表示)。
 表示生成1mol产物的数据)。
表示生成1mol产物的数据)。
回答下列问题:
(1)1molPCl3所具有的总能量比1molP和1.5molCl2所具有的总能量
(2)PCl3和Cl2化合成PCl5的热化学方程式是
(3)P和Cl2反应生成1molPCl5的
 =
=(4)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是
(5)红磷的同素异形体白磷在氧气中燃烧有如下转化关系。

其中
 =
=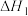 和
和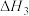 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2021-10-31更新
|
146次组卷
|
4卷引用:贵州省平塘民族中学2021-2022学年高二上学期第一次月考化学试题
填空题
|
适中(0.65)
名校
解题方法
20. 在一体积固定的密闭容器中,某化学反应2A(g) B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如表:
B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如表:
根据上述数据,完成下列填空:
(1)实验1中,在10~20min内,用A表示的该反应的平均速率为________ mol·L-1·min-1。
(2)实验2中c2=________ ,反应经20min就达到平衡,可推测实验2中还隐含的条件是________ 。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3______ (填“>”“<”或“=”,下同)v1,且c3_____ 1.0。
(4)请根据以上实验指出要加快该反应速率可采取的方法:________ 。(至少列举2种方法)
 B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如表:
B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如表:| 实验序号 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800 | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800 | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上述数据,完成下列填空:
(1)实验1中,在10~20min内,用A表示的该反应的平均速率为
(2)实验2中c2=
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3
(4)请根据以上实验指出要加快该反应速率可采取的方法:
您最近一年使用:0次
2020-03-12更新
|
117次组卷
|
4卷引用:河南省开封市五县联考2019-2020学年高二上学期期末考试化学试题
试卷分析
整体难度:适中
考查范围:化学反应原理、有机化学基础、化学与STSE、认识化学科学、物质结构与性质、常见无机物及其应用、化学实验基础
试卷题型(共 20题)
题型
数量
单选题
16
解答题
2
填空题
2
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 电解原理的应用 蛋白质 大气污染 | |
| 2 | 0.65 | 化学用语综合判断 | |
| 3 | 0.65 | 结合气体物质与NA相关推算 结合氧化还原反应知识与NA相关推算 | |
| 4 | 0.65 | 离子方程式的正误判断 | |
| 5 | 0.94 | 离子共存 限定条件下的离子共存 | |
| 6 | 0.65 | 氧化还原反应定义、本质及特征 氧化还原反应的规律 电子转移计算 | |
| 7 | 0.65 | 根据原子结构进行元素种类推断 根据物质性质进行元素种类推断 “位构性”关系理解及应用 | |
| 8 | 0.85 | 有机官能团的性质及结构 有机分子中原子共面的判断 多官能团有机物的结构与性质 | |
| 9 | 0.94 | 化学反应的速率 化学反应速率计算 化学反应速率与化学计量数之间的关系 | |
| 10 | 0.85 | 化学平衡状态 化学平衡状态本质及特征 化学平衡状态的判断方法 | |
| 11 | 0.94 | 热化学方程式 热化学方程式书写及正误判断 | |
| 12 | 0.65 | 化学反应速率含义、单位 化学反应速率计算 催化剂对化学反应速率的影响 化学平衡状态本质及特征 | |
| 13 | 0.85 | 中和热的测定与误差分析 | |
| 14 | 0.65 | 化学反应热的计算 盖斯定律的应用 | |
| 15 | 0.65 | 化学平衡的有关计算 | |
| 16 | 0.85 | 化学反应速率计算 影响化学反应速率的外因 温度对化学反应速率的影响 | |
| 二、解答题 | |||
| 17 | 0.94 | 有关铁及其化合物转化的流程题型 物质分离、提纯综合应用 常见无机物的制备 | 工业流程题 |
| 18 | 0.65 | 氧化还原反应的规律 一氧化氮的化学性质 硝酸的强氧化性 | 实验探究题 |
| 三、填空题 | |||
| 19 | 0.85 | 盖斯定律及其有关计算 热化学方程式书写及正误判断 盖斯定律与热化学方程式 | |
| 20 | 0.65 | 化学反应速率计算 影响化学反应速率的外因 化学平衡的移动及其影响因素 化学平衡题中基于图表数据的相关计算 | |

 。下列叙述中不能说明该反应已达到化学平衡状态的是
。下列叙述中不能说明该反应已达到化学平衡状态的是

